细胞免疫疗法迎来"活药" 时代!一针清除癌细胞?这些晚期癌症临床突破让五年生存率翻倍
细胞治疗迎来"活药"时代!一针清除癌细胞?这些晚期癌症临床突破让五年生存率翻倍
近些年来,众多细胞免疫疗法纷纷崛起,发展迅猛,无疑掀起了一场癌症治疗的热潮。
曾在2012年成功“治愈”白血病女孩Emily的CAR-T细胞疗法,成为医学界继PD-1后,又一炙手可热的明星疗法。
MelindaBachini作为第一个接受肿瘤浸润淋巴细胞治疗的胆管癌患者,至今已幸存近15年,这款“古老”的TILs细胞疗法让她从生存期仅剩几个月到重获新生,展示了细胞免疫疗法强大的杀癌能力。
曾经被视作“最后选择”的CAR-T细胞疗法,如今已让超过40%的晚期弥漫大B细胞淋巴瘤患者活过5年大关,且三分之一的患者无进展生存超过3年,而在传统治疗时代,这一数字不足20%。
这些突破标志着癌症治疗正式迈入“活药物时代”——通过改造人体免疫细胞,使其成为精准识别并持续剿灭癌细胞的“智能导弹”。
数据颠覆:五年生存率翻倍的临床革命
在弥漫大B细胞淋巴瘤(DLBCL)领域,CAR-T疗法使复发难治患者的5年总生存率从传统化疗的20%跃升至41%,其中部分亚型患者甚至实现长期治愈。以同济大学C-CAR066研究为例,14例患者的总缓解率高达92.9%,中位生存期长达34.8个月,远超历史数据。多发性骨髓瘤领域,西达基奥仑赛(Carvykti)的CARTITUDE-1研究显示,98%的患者实现客观缓解,78%达到严格意义上的完全缓解,中位缓解持续时间达21.8个月,让晚期患者看到“根治”希望。
实体瘤治疗同样迎来曙光。TIL疗法GT201在非小细胞肺癌(NSCLC)中实现100%疾病控制率,部分缓解率达42.9%,其中一位患者肿瘤缩小69%。NK细胞联合肝动脉灌注化疗(HAIC)在晚期肝癌中客观缓解率达63.6%,12个月和36个月的生存率分别为72.7%和54.5%,远超传统末线治疗的6个月。更令人振奋的是,古巴肺癌疫苗CIMAvax-EGF使晚期NSCLC患者的5年生存率从5%提升至20%,部分患者生存期延长至7年以上。
四大革命性疗法,重塑癌症治疗格局
细胞免疫治疗是一种利用患者自身的免疫细胞來对抗癌细胞的疗法。这种疗法通常涉及以下步骤:抽取患者的血液,分离出周边血液单核细胞,然后在实验室进行体外培养、活化扩增。最后,这些增强的免疫细胞亚群会被回输患者体内,以补充免疫细胞的数量,增强其免疫系统对抗癌细胞的能力。依据扩增的免疫细胞亚群的不同,会被赋予不同的命名。
不同于手术(切除病灶)、化疗(对微转移有效)、放疗(局部有效改善)的是,细胞免疫治疗侧重的是提高人体的应对能力,通过增加免疫细胞的数量、质量和装备,来精准识别、绞杀敌人,避免无差别攻击。
今天,小编将从CAR-T疗法、TCR-T疗法、TIL疗法、CAR-NK疗法等这几种免疫细胞疗法入手,深入探讨它们在血液肿瘤、实体瘤治疗中的应用与突破。
CAR-T疗法:从血液瘤到实体瘤的破壁者
T细胞是人体内极为重要的免疫细胞类型,通常而言T细胞寿命可达数年以上。CAR-T(嵌合抗原受体T细胞)疗法的核心,是将患者自身的T细胞改造成“抗癌特种兵”。通过基因工程技术,科学家为T细胞装上人工设计的“导航雷达”CAR,使其能精准识别肿瘤细胞表面的特定靶点(如CD19、CD20、BCMA),并激活强大的杀伤机制。
与传统化疗“无差别轰炸”不同,CAR-T实现了癌症治疗的“精准斩首”。截至2025年7月,全球已有13款CAR-T产品上市,在复发难治性白血病、淋巴瘤、多发性骨髓瘤等血液肿瘤中,将原本不足10%的生存率提升至65%以上。
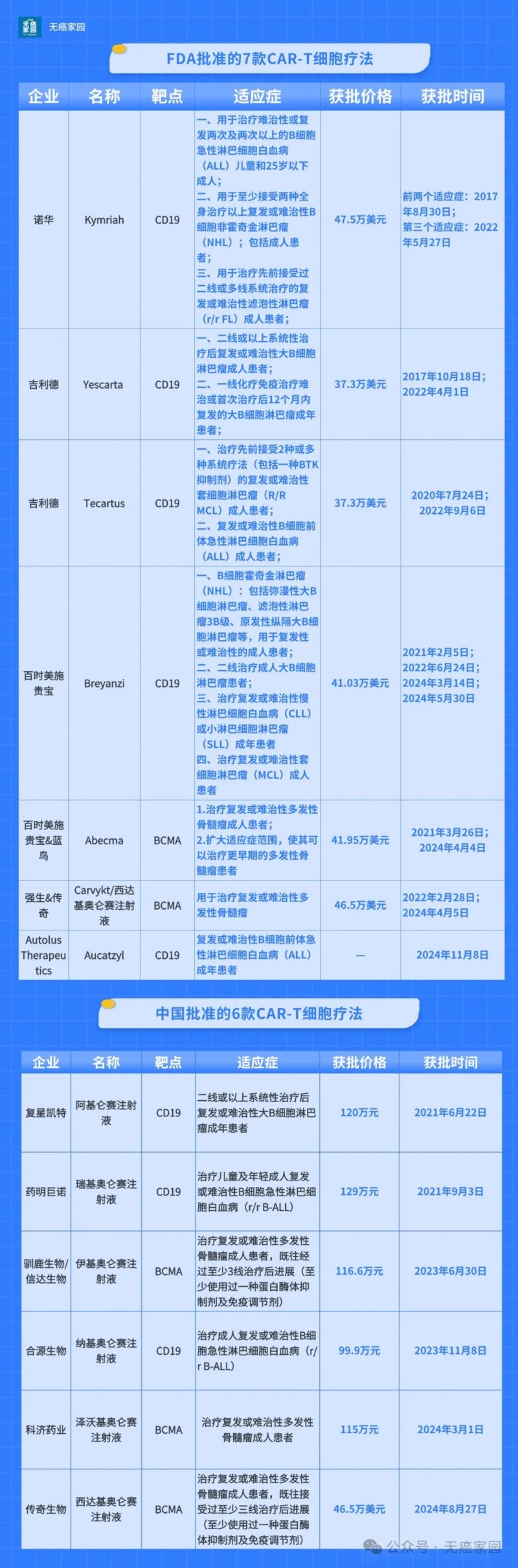
目前国内外已上市的CAR-T细胞疗法
胃癌、胰腺癌:靶点Claudin18.2
近日,实体瘤CAR-T领域再次传来捷报!2025年6月25日,科济药业宣布,其自体Claudin18.2CAR-T细胞产品舒瑞基奥仑赛注射液(Satri-cel,CT041)的新药上市申请(NDA)已正式提交至中国国家药品监督管理局(NMPA)药品审评中心(CDE),拟用于治疗Claudin18.2表达阳性、至少二线治疗失败的晚期胃/食管胃结合部腺癌(G/GEJA)患者。如果一切顺利的话,舒瑞基奥仑赛即将成为全球首款针对实体瘤的CAR-T产品,早日惠及广大胃癌患者。
作为国际上首个针对Claudin18.2的CAR-T细胞,Satri-cel从2019年首次亮相就惊艳世界,其显著的疗效展现出对消化系统肿瘤的良好治疗前景。
最新临床试验结果已在国际知名医学期刊《Lancet》和2025年ASCO学会上正式公布。
中位总生存期显著延长,死亡风险显著降低
在所有随机人群(ITT)中,基于独立评审委员会(IRC)评价,satri-cel组的mPFS显示出显著改善(3.25个月vs1.77个月,患者疾病进展/死亡风险显著下降达63%,并且mOS明显趋于延长(7.92个月vs5.49个月)优于TPC组。简单来说,相比标准疗法,satri-cel组患者中位总生存期延长了44%。
在实际用药人群(mITT)中,共有136例接受研究药物治疗(satri-cel88例+TPC48例),IRC预测的中位PFS分别为4.37个月vs1.84个月,患者疾病进展/死亡风险下降70%,中位OS分别为8.61个月vs5.49个月,死亡风险下降40%。
值得注意的是,接受satri-cel治疗的TPC组患者(n=20)的中位OS为9.20个月。在所有接受satri-cel治疗的患者(n=108)中,与未接受satri-cel治疗的TPC患者(n=28)相比,中位OS分别为9.17个月vs3.98个月,患者疾病进展/死亡风险显著下降约72%。
客观缓解率22%,疾病控制率63%
经独立审查委员会(IRC)评估,satri-cel组确诊客观缓解率为22%(23/104),TPC组为4%(2/52);satri-cel组疾病控制率为63%(65/104),TPC组为25%(13/52)。
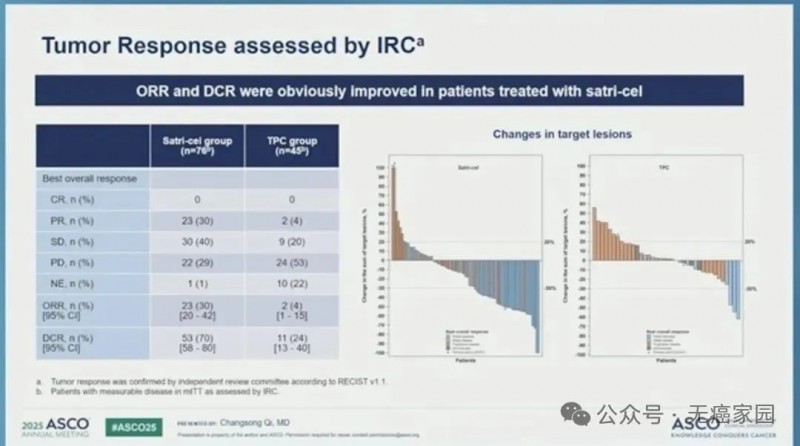
研究结果显示,在Claudin18.2表达阳性、至少二线治疗失败的胃/食管胃结合部癌患者中,舒瑞基奥仑赛对比标准治疗可显著改善无进展生存期(PFS),并能够显著延长总生存期(OS),同时安全性可控。
除此之外,还有多款靶向CLDN18.2的CAR-T细胞疗法。例如,由传奇生物研发的LB-1904,用于治疗胃癌或者胰腺癌,目前已经进入临床I期试验。此外,我国还有多款针对Claudin18.2的临床试验正在进行临床试验招募中,有意向的患者可咨询医学部了解详情。
肝癌:靶点GPC3(磷脂酰肌醇蛋白多糖3)
2025年ASCO会议上公布了原启生物Ori-CAR-001(Ori-C101)疗法治疗GPC3阳性肝细胞癌的最新试验数据,截至2024年12月17日,共有10例符合条件的患者接受了3个剂量水平(DLs)的Ori-C101输注。
在9例可评估疗效的患者中,6例患者(66%)在DL2或更高水平上实现了疾病控制。值得一提的是,DL3的所有患者均实现了客观反应,即肿瘤体积明显缩小。特别是1例患者达到完全缓解(CR),在9个月的随访评估中表现出令人鼓舞的持久性,无复发迹象。
早在2021年ASCO年会上就公布过Ori-C101治疗复发难治性肝细胞癌的临床试验数据,截至2021年3月10日,11例多线治疗失败(化疗、TACE、靶向治疗)患者中,9例患者可评估疗效,客观缓解率44.4%(4/9),疾病控制率77.8%(7/9)。其中1例患者部分缓解持续超6个月,肿瘤体积在细胞输注后1个月缩小超80%,疾病控制超8个月。
结直肠癌:靶点GCC/GUCY2C/CEA
2022年4月19日,上海斯丹赛生物宣布,其开发的实体瘤CAR-T产品GCC19CART被美国食品和药物管理局(FDA)授予快速通道资格。
在ASGCT会议上,斯丹赛介绍了关于21例患者的最新临床数据,其中13患者以1级剂量(1x106cells/kg)入组,8名患者以2级剂量(2x106cells/kg)入组。根据实体肿瘤疗效评价标准(RECIST1.1),1级剂量组客观缓解率(ORR)为15.4%(2/13),2级剂量组客观缓解率为50%(4/8)。
除了靶点GCC外,结直肠癌另外一个有效靶点CEA也是近期研究热门。
约75%的结直肠癌肝转移患者因循环肿瘤细胞和微小残留病灶,在术后两年内复发。CAR-T细胞疗法对血液肿瘤有效,也可能用于治疗复发性结直肠癌肝转移。2025年ASCO大会上公布了CAR-T疗法在结直肠癌肝转移术后患者中的安全性和有效性。

该研究选取2021年12月至2024年12月期间,共12例接受CAR-T细胞输注(1×10^6/kg组和3×10^6/kg组各2例,6×10^6/kg组8例)的患者。
研究结果显示,在6×10^6/kg剂量组中,4例受试者在输注后分别维持了5个月、7个月、10个月和15个月的无复发生存,目前仍在随访中。通过CAR-T细胞输注,6×10^6/kg剂量组中57.14%的受试者在根治性切除术后两年内未复发。
这是首个探索抗CEACAR-T疗法延长结直肠癌肝转移术后患者无复发生存期的临床试验,结果显示该疗法无严重不良事件,且高剂量治疗可显著降低复发风险。
在此之前,第三军医大学钱程教授团队曾报道了CEACAR-T细胞在10例晚期结直肠癌患者中的临床效果,其中7例患者疾病稳定,2例出现明显肿瘤缩小,所有患者均观察到血清CEA不同程度下降。
在之前的新闻稿中报道,临床前小鼠体内研究结果显示,C-13-60具有明显的有效性,有望帮助更多的胃癌、结直肠癌、食管癌患者成功摆脱病痛的折磨。
间皮瘤、卵巢癌:靶点MSLN
间皮瘤
2021年11月,来自美国的医学研究者们发布了一项CAR-T联合PD-1抑制剂的临床试验的I期结果在知名《CancerDiscovery》杂志上,主要阐述了以间皮素为靶点的自体CAR-T细胞与帕博利珠单抗(pembrolizumab,商品名Keytruda)联用治疗恶性胸膜间皮瘤(MPM)的临床疗效。
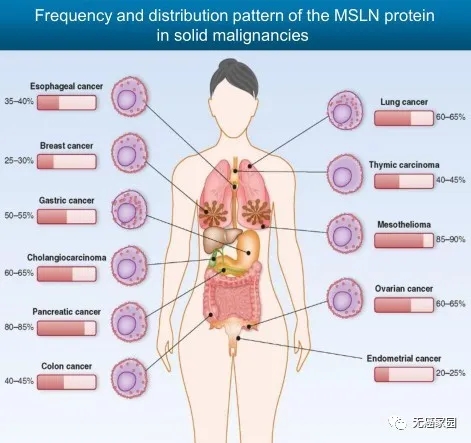
间皮素高表达于多种肿瘤组织,比如胰腺癌、卵巢癌、乳腺癌、子宫内膜癌、前列腺癌以及胆管癌等(图片来源PNAS)在此项临试验中,共纳入27例患有胸腔肿瘤的患者接受治疗,其中转移性肺腺癌1例,转移性乳腺癌1例,其余均为恶性胸膜间皮瘤患者。
27例患者中,有23例恶性胸膜间皮瘤患者在CAR-T治疗前进行环磷酰胺预处理,其中有18例患者接受CAR-T联合pembrolizumab治疗,5例仅接受CAR-T治疗。值得一提的是,所有患者均接受过一轮既往治疗,33%的患者接受过≥3轮的既往治疗。
需要指出的是,恶性胸膜间皮瘤是一种PD-L1表达及肿瘤突变负荷均较低的恶性肿瘤,前期的临床试验也证明患者不能受益于PD-1/PD-L1免疫抑制剂的单药治疗。
在确保安全性和持续性良好的细胞制品的前提下,临床效果也让人格外惊艳!
23例接受治疗的恶性胸膜间皮瘤患者中,CAR-T治疗后的中位生存期为17.7个月,一年存活率为74%。而在18名接受了CAR-T+帕博利珠单抗联合治疗的患者中,中位生存期达到了23.9个月,一年存活率为83%。
更惊人的发现是,靶向间皮素的CAR-T疗法有望在恶性胸膜间皮瘤患者中实现长期的疾病缓解。在治疗后第4~6周的影像检查中(n=16),有12.5%的患者的疗效达到了部分缓解,56.3%的患者为疾病稳定。在疾病稳定或部分缓解的患者中,有8名患者能够维持疾病状态超过6个月。
卵巢癌
2018年7月,MaxCyte宣布,公司基于mRNA非病毒技术开发的治疗实体瘤的CAR细胞疗法已被FDA批准开始临床试验,同时,这也是MaxCyte全资拥有的第一个CAR项目MCY-M11,靶点正是间皮素(MSLN),通过腹腔内注射治疗复发/难治性卵巢癌和腹膜间皮瘤患者。
目前免疫临床试验急招肝癌、胃癌、卵巢癌、食管鳞癌、急性淋巴细胞白血病、非霍奇金淋巴瘤、间皮瘤、多发性骨髓瘤等癌种!
除了上述提到的癌种外,其他实体瘤癌友在经济条件允许的情况下可以尝试CAR-T项目进行治疗。
具体流程可将病理报告、治疗经历及出院小结等提交至医学部进行初步评估!
TCR-T疗法:深入细胞核的"精准猎手"
CAR-T和TCR-T都属于经基因工程技术改造的T细胞疗法,与CAR-T相比,TCR-T疗法能够识别肿瘤内外多种抗原靶点,可广泛用于治疗包括实体瘤在内的多种恶性肿瘤细胞,因此被寄予厚望。
乙型肝炎病毒相关肝细胞癌
星汉德生物公司首次公布了其靶向乙肝病毒表面抗原(HBsAg)的TCR-T疗法SCG101的临床试验中期数据,此次试验主要是治疗乙型肝炎病毒相关肝细胞癌患者。
其数据显示,在3例HLA-A*02:01阳性的晚期乙肝病毒相关性肝细胞癌患者中,三分之二的观察到病灶缩小的患者的肿瘤生长得到控制。值得一提的是,这些患者曾接受过至少两种癌症治疗。研究表明,SCG101具有显著的抗病毒和抗肿瘤活性,疾病控制率可达66%!
这是首个靶向HBsAg细胞治疗获得临床概念验证,是TCR-T细胞治疗在病毒相关实体瘤领域的一个重要里程碑。
乙肝病毒相关的成人肝细胞癌
FDA授予来恩生物医药有限公司(LionTCR)研发的LioCyx-M004快速通道指定,这是一种T细胞受体T细胞疗法,用于治疗乙肝病毒相关的成人肝细胞癌(HCC)。
在接受治疗的患者中没有出现细胞因子释放综合征(CRS),也没有神经毒性的迹象。疾病控制率为60%,缓解持续时间为27.7个月。患者的中位OS为33.1个月(典型案例如图所示)。
和索拉非尼的历史数据比较,来恩的LioCyx-M产品的中位生存期的临床数据获得显著提升,翻了3倍!
该研究将是首个使用HBV特异性TCR-T细胞疗法治疗乙肝相关肝癌的研究。
宫颈癌、肛门癌、头颈部肿瘤
TCR-T疗法KITE-439治疗HPV阳性实体瘤的临床1期试验的数据表明,靶向16型HPV(HPV-16)的E7蛋白的TCR疗法能够在部分HPV-16阳性癌症患者身上实现肿瘤部分缓解。
结果显示,在7例可评估的患者中,3例部分缓解,2例患者疾病稳定。截止数据发布时,缓解期最长可以达到9个月,获得部分缓解的患者分别为外阴癌、口咽癌和肛门癌患者。
到目前为止,TCR-T细胞免疫疗法已在部分实体肿瘤的治疗中取得了较好的疗效,特别是对肝癌、黑素瘤、滑膜细胞肉瘤的治疗效果很明显,但是对食管癌和多发性骨髓瘤等其他实体瘤的疗效尚有待进一步临床验证。
如何寻求TCR-T疗法及其他疗法?>>
目前正有几款研发的TCR-T疗法在招募乙型肝炎病毒相关肝细胞癌患者、一款针对HPV16阳性的TCR-T疗法,主要癌种:晚期宫颈癌、肛门癌、头颈部肿瘤(口腔癌、喉癌等),想要参加的患者可提交病理报告、治疗经历、出院小结等资料至医学部初步评估病情。
此外,若想咨询其他细胞疗法(CAR-T、NK、CAR-NK、CTL、TILs等疗法)的患者,同样可将病理报告及治疗经历、出院小结等资料提交至医学部,详细评估病情。
TIL疗法:实体瘤的"自体护卫队"
TILs是一种对实体肿瘤有着天然归巢优势的细胞免疫疗法,即从患者的肿瘤中分离出淋巴细胞,将分离的细胞在体外激活扩增或加以改造,然后再回输到患者体内。通俗点讲,这款疗法相当于直接从战场上拉回有战斗经验的老兵,经过一轮“政治审查”和业务能力“大比拼”,把内奸、叛徒尽量剔除出去,留下战斗力最强的,提供补给,再重新送回战场继续战斗。
与其他免疫疗法(例如,CAR-T、PD-1/PD-L1抗体)相比,TIL具有多靶点、肿瘤趋向和浸润能力强、副作用小等优势;是实体瘤治疗的理想选择,前景广阔。
2024年2月16日,IovanceBiotherapeutics公司宣布Lifileucel(LN-144)获得美国食品和药物管理局(FDA)加速批准上市(PDUFA日期为2月24日),用于治疗PD-1抗体治疗后进展的晚期黑色素瘤,商品名为Amtagvi。根据新闻稿可知,这也是全球首款获批上市的TIL疗法,更是首款获批的治疗实体瘤的T细胞疗法,具有里程碑的意义!
除了黑色素瘤外,TILs疗法在非小细胞肺癌、宫颈癌、胆管癌、结直肠癌、乳腺癌、头颈部、肉瘤、胆囊癌等恶性肿瘤中均显示出巨大潜力。已经发展的各项研究表明,TILs治疗将有待不断改进和发展,最终将成为人类抗癌的新武器。
CAR-NK疗法:攻克实体瘤的"希望之光"
CAR-T细胞疗法取得的成功激发了人们对用CAR基因修饰NK细胞来增强其杀肿瘤能力的热情。
CAR-NK就是利用基因工程给NK细胞加入一个能识别肿瘤细胞,并且同时激活NK细胞杀死肿瘤细胞的嵌合抗体。2020年,CAR-NK免疫细胞治疗曾被权威学术期刊《自然-医学》纳入度生物医学领域的十代瞩目进展之一。
越来越多的体外和体内研究验证了CAR-NK细胞对实体瘤的活性,其中大多数临床前数据可用于胃癌、结直肠癌、肝癌、非小细胞肺癌、胶质母细胞瘤、乳腺癌、卵巢癌和胰腺癌。这些结果促成了首个用于实体瘤治疗的CAR-NK细胞临床试验的启动。
小编有话说
细胞免疫疗法理论上可以对应任何阶段的癌症,比如:
●肿瘤手术前体质较差,术后恢复慢,且害怕隐匿性癌细胞没有被彻底根除的患者。
●放疗、化疗后,免疫力低下,副作用反应明显(如食欲减退、恶心、脱发、皮肤炎症等),期望增加化放化疗效果的患者。
●由于害怕放化疗的毒副作用,希望利用各种治疗手段实现治疗效果的患者。
●肿瘤晚期癌细胞已经全身扩散,但常规治疗方法已无能为力,期望延长生存期,提高生活质量的患者。
需要注意的是,细胞免疫疗法对于晚期癌症患者肿瘤的缩小效果不明显,针对晚期癌症的患者在保持生活品质的同时有延长寿命的效果;作为术后的辅助治疗法可以抑制复发,治疗效果可维持较长时间;与化疗、靶向药、PD1抑制剂等其它疗法联合治疗,效果会更佳。
主要适用于实体肿瘤:头颈部肿瘤、食道癌、肺癌、胃癌、乳腺癌、肝癌、胰腺癌、结直肠癌、卵巢癌、子宫癌、肾癌、前列腺癌、恶性黑色素瘤、肉瘤、部分恶性淋巴瘤。
扫描进患者病友群

肺癌|胃癌|肝癌|结直肠癌|胰腺癌
乳腺癌|脑瘤|淋巴瘤|儿童肿瘤等

相关推荐

癌症治疗本就不应千篇一律,揭秘mRNA癌
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
“不限癌种”新突破,NTRK基因融合的靶
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
肺癌疫苗重大突破,晚期患者多了一个新的选
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

“手术成功”不等于万事大吉,新型癌症疫苗
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

2026年靶向治疗抗癌风暴,突破困境,普
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

2026年这些肺癌疫苗正悄然改变患者的生
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05






![[field:title/]](/uploads/allimg/20200224/1-2002241I5262J.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241I3461D.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H94LK.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241HKW34.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H619327.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H34H52.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H22IH.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241G93O18.jpg)




