癌细胞28天清零!中国自研CAR-T疗法震撼突破,开启淋巴瘤、胰腺癌、结直肠癌等治疗新篇章
中国自研CAR-T细胞疗法震撼突破,癌细胞28天清零!开启淋巴瘤、胰腺癌、结直肠癌等治疗新篇章
28天,全身癌细胞消失!”这个曾经只存在于科幻想象中的场景,如今已成为中国自主研发CAR-T疗法创造的医学奇迹!
2025年4月30日,健科瑞生物科技公布了其体内给药的CD19 CAR-T疗法针对复发/难治性弥漫大B细胞淋巴瘤(R/R DLBCL)的突破性临床数据:在同济医院血液科牵头的研究者发起临床试验(IIT)中,一名经多线治疗失败的晚期R/R DLBCL患者接受该疗法28天内,达到完全缓解(CR)!更令人振奋的是,这份生命的馈赠仍在延续——治疗效果持续稳固超过3个月!这不仅是一个患者个体的生命逆袭,更是中国抗癌创新疗法跻身国际第一梯队的里程碑!

▲截图源自“PR Newswire”
中国CAR-T疗法颠覆传统:无需体外培养+摒弃化疗预处理,一位晚期淋巴瘤患者的重生之路——28天实现完全缓解,90天持久抗癌
复发/难治性弥漫大B细胞淋巴瘤(R/R DLBCL)作为恶性程度极高的血液系统肿瘤,曾让无数患者陷入生命绝境。但医学创新从未止步:近年来,CAR-T细胞疗法以“改造免疫细胞精准杀癌”的突破性机制横空出世,为晚期肿瘤患者点燃重生希望,尤其在在血液系统恶性肿瘤(包括复发/难治性非霍奇金淋巴瘤、B细胞急性淋巴细胞白血病和多发性骨髓瘤)的治疗中取得了显著成功,多项临床试验的治愈率超过80%。
在同济医院血液科牵头的研究者发起临床试验(IIT)中,一名经多线治疗失败的R/R DLBCL患者,接受新型体内CD19 CAR-T疗法仅28天即达完全缓解(CR),且疗效持续超过90天。流式细胞术分析显示,该疗法无需传统淋巴细胞清除预处理,即可实现体内CAR-T细胞的强劲扩增与持久存续。
相较于传统CAR-T疗法约50%患者面临的细胞因子释放综合征(CRS)、神经毒性(ICANS)及淋巴细胞清除相关感染风险,这一创新方案实现了关键突破:上述并发症在治疗中完全未出现,安全性优势显著。其核心技术平台攻克两大行业难题:
1、颠覆体外操作流程:传统疗法需耗时3-4周体外采集、修饰并扩增患者T细胞,伴随高达40万美元的成本;该平台通过专有载体直接向体内循环T细胞递送CAR有效载荷,原位生成功能性CAR-T细胞,大幅简化治疗流程。
2、 摒弃预处理化疗:无需高强度化疗进行免疫重置,不仅减少住院需求与治疗相关并发症,更实现了CAR-T细胞的自然高效扩增。
这种融合自体CAR-T特异性与通用疗法便捷性的创新模式,正推动癌症治疗迈向“普惠时代”。随着“无并发症、低成本、高效率”优势的落地,全球患者有望迎来从“天价疗法”到“可及治愈”的历史性跨越——这不仅是技术革新,更是人类对抗血液肿瘤的重要里程碑。
中国患者如何寻求CAR-T细胞疗法帮助
好消息是,目前CAR-T疗法已启动临床招募,主要针对胃癌、胰腺癌、肠癌、脑胶质瘤、淋巴瘤、骨髓瘤、白血病等多款癌种。阅读原文了解详情:百万疗法免费申请机会来啦!十大CAR-T疗法启动招募,惠及胃癌,肠癌,淋巴瘤等
想寻求CAR-T或其他抗癌新技术帮助的病友,也可将治疗经历、病理检查结果、近期检查报告(如影像学检查、血液检查等)、基因检测报告等资料,提交至医学部,初步评估能否有机会接受CAR-T疗法的帮助。
CD30.CAR-T改写难治性霍奇金淋巴瘤治疗格局,1年总生存率高达94%
大多数经典型霍奇金淋巴瘤(HL)患者可通过一线疗法治愈,但约15%的患者在初次治疗后会出现原发性难治性疾病或复发。对于一线疗法失败的患者,标准治疗方案为高剂量化疗联合自体干细胞移植(aSCT),然而约一半患者在移植后仍会复发。这类患者预后较差,尽管异基因干细胞移植(alloSCT)曾被视为实现持续缓解的最佳手段,但其伴随较高的发病率和死亡率。因此,探索新的治疗方法迫在眉睫。
近期,《临床肿瘤学杂志》公布了两项利用CD30特异性CAR-T细胞(CD30.CAR-T)治疗霍奇金淋巴瘤(HL)的I/II期临床试验(NCT02690545和NCT02917083)的惊艳数据。
该研究共纳入41例患者接受CD30.CAR-T细胞疗法。这些患者中位年龄为35岁(范围:17-69岁),既往接受过的治疗方案中位数达7种(范围:2-23),涵盖布妥昔单抗维多汀、检查点抑制剂,以及自体或异基因干细胞移植。
结果显示:37位可评估患者的客观缓解率(ORR)为62%。在32例接受以氟达拉滨为基础的淋巴细胞清除疗法的活动性疾病患者中,总缓解率(ORR)达72%,其中19例(59%)实现完全缓解(CR),且有1名患者在治疗3年后仍维持完全缓解状态。
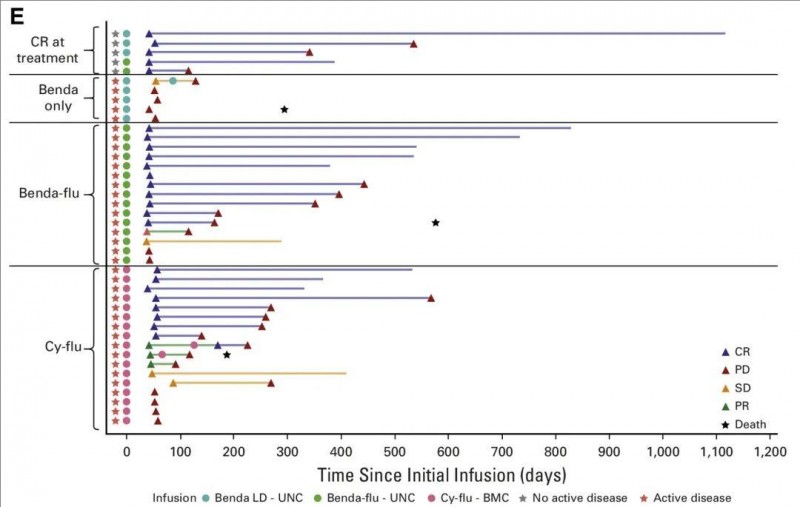
▲图源“JCO”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
注:灰色星号表示达到完全缓解(CR)的患者。
中位随访时间为533天,所有可评估患者的1年总生存(OS)率高达94%(95%CI,79%-99%,详见下图A),1年无进展生存(PFS)率为36%(95%CI,21%-51%,详见下图B)。
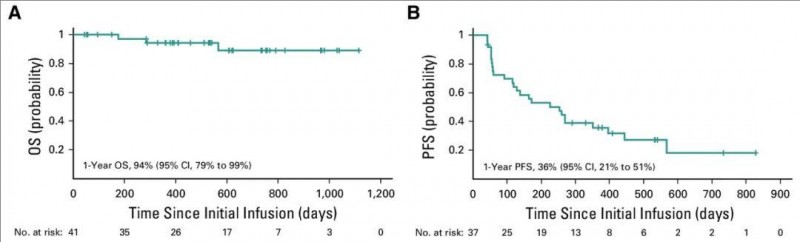
▲图源“JCO”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
值得关注的是,一名治疗前存在颈部、右腋窝、纵隔、门腔静脉及腹膜后等多处高代谢淋巴结的患者,在输注CD30.CAR-T细胞6周后,经正电子发射断层扫描(PET-CT)评估达到完全缓解(Deauville2)。
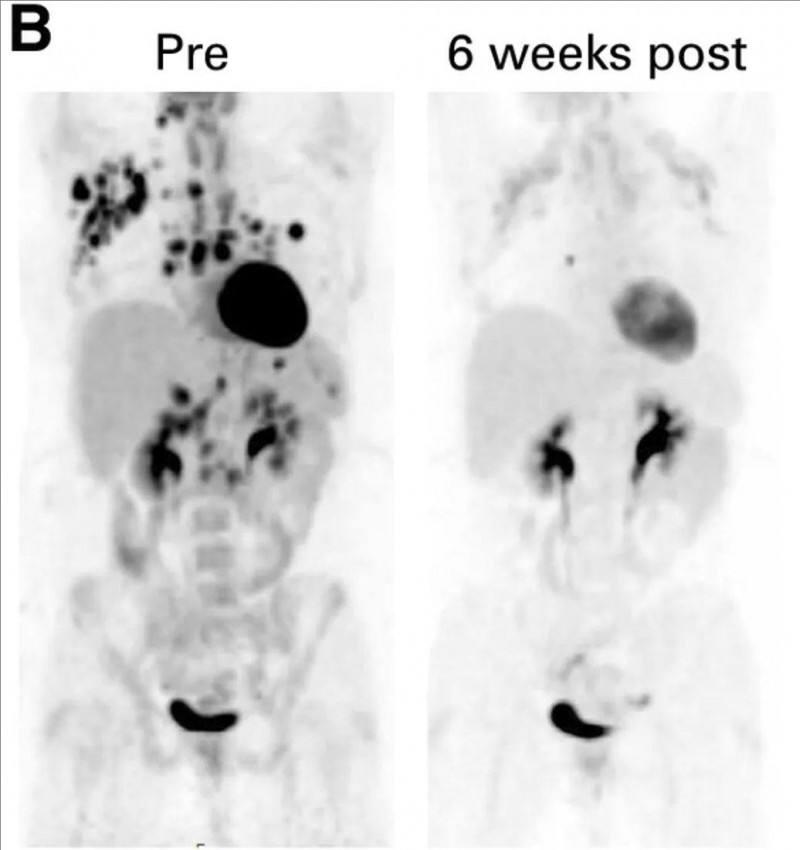
▲图源“JCO”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
综上,对于接受过大量治疗的复发或难治性经典型霍奇金淋巴瘤(HL)患者,先采用以氟达拉滨为基础的淋巴细胞清除治疗,再进行CD30.CAR-T治疗,不仅展现出较高的持久缓解率,且安全性良好。这一成果充分证明,将CAR-T细胞疗法应用于典型B细胞恶性肿瘤以外的疾病具有切实可行性。
Claudin18.2靶向CAR-T细胞疗法:助一例晚期胰腺癌患者达完全缓解
胰腺癌(PC)是消化系统高度侵袭性的恶性肿瘤,因早期筛查手段有限,多数患者确诊时已处于晚期或发生转移。尽管当前治疗方案包括手术、化疗、放疗及免疫检查点抑制剂等,但临床疗效普遍不佳——即使接受根治性手术,肿瘤仍易复发转移,而晚期患者对常规治疗应答率低,导致胰腺癌整体预后极差。因此,迫切需要开发新的、更有效的治疗策略。
近年来,CAR-T细胞疗法在血液肿瘤中展现出突破性疗效,其在实体瘤领域的应用也进入探索阶段。《免疫前沿》近期报道了一例令人振奋的临床案例:一名晚期胰腺癌患者,在接受Claudin18.2靶向CAR-T细胞疗法治疗后,奇迹般获得完全缓解。
该患者是一位72岁男性,于2021年6月确诊Ⅲ期胰腺导管腺癌(pT2N2M0,Ⅲ期),接受胰十二指肠切除术后,先后进行8周期吉西他滨联合卡培他滨辅助化疗。2022年8月因血清CA19-9持续升高,经MRI检查发现肝及腹膜转移,随后更换为替吉奥方案(替加氟、吉美嘧啶和奥替拉西钾联合用药)化疗,但2022年9月进一步出现颈部淋巴结转移。患者转用FOLFIRINOX方案(氟尿嘧啶、亚叶酸钙、伊立替康和奥沙利铂)后,因严重不良反应(乏力、恶心、呕吐、中性粒细胞减少等)被迫终止治疗。
鉴于该患者多线治疗失败且肿瘤广泛转移(肝、腹膜、颈部淋巴结),经检测肿瘤组织Claudin18.2高表达(阳性细胞率≥70%),患者遂入组CAR-T细胞临床试验(NCT05620732),在接受淋巴细胞清除化疗后,单次输注Claudin18.2靶向CAR-T细胞。
结果显示:患者在CAR-T细胞输注1个月后即达到完全缓解(CR),肿瘤标志物CA19-9从1100U/mL显著降至25.85U/mL,恢复到正常范围(详见下图),且CA19-9在治疗5个月后仍保持正常水平。
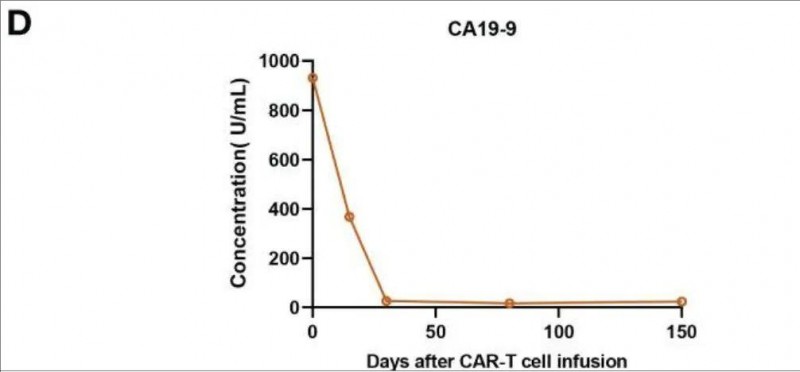
▲图源“Front Immunol”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
此外,PET-CT扫描显示颈部淋巴结、肺部及其他转移病灶完全消失,且CAR-T细胞治疗后8个月,颈部及肺部病灶未复发(详见下图)。
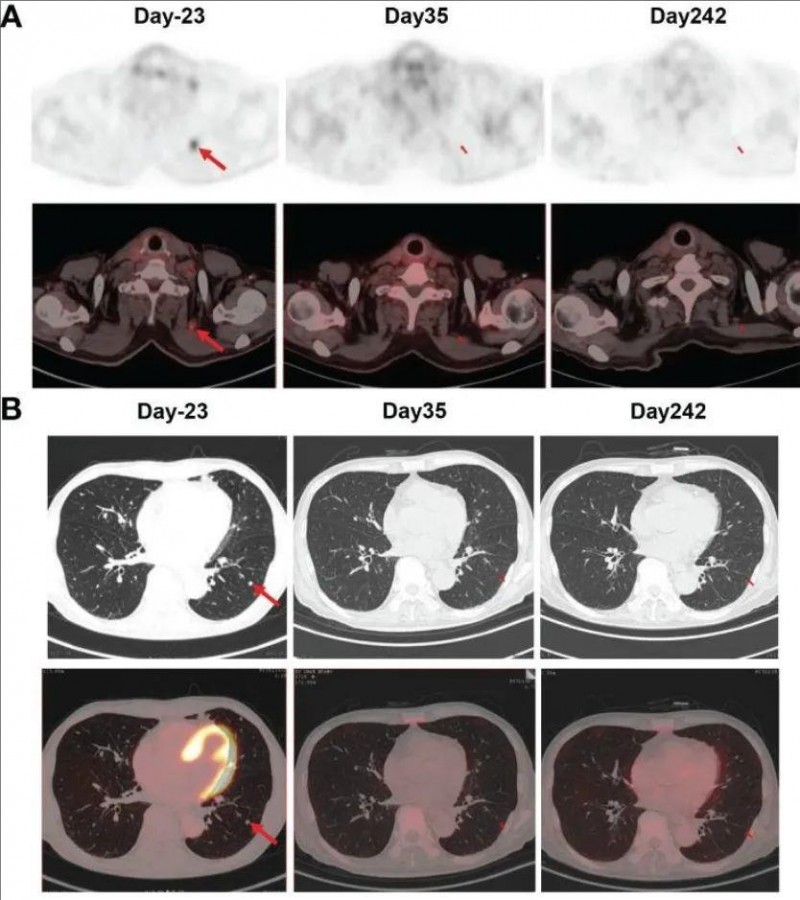
▲图源“Front Immunol”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
注:
①图A:PET/CT显示claudin18.2靶向CAR-T细胞治疗后1个月颈部淋巴结转移消失,CAR-T细胞输注后8个月仍处于缓解状态。
②图B:PET/CT显示claudin18.2靶向CAR-T细胞治疗后1个月肺转移消失,CAR-T细胞输注后8个月仍处于缓解状态。
全球首个ICAM-1靶向CAR-T疗法首秀告捷,难治性甲状腺癌疾病控制率高达56%
新诊断或复发/难治性(R/R)间变性甲状腺癌(ATC)与低分化甲状腺癌(PDTC)患者,往往面临治疗选择有限、总体预后差的困境。细胞间粘附分子-1(ICAM-1,CD54)在甲状腺癌等多种肿瘤中过表达,参与肿瘤发生发展,成为潜在治疗靶点。AIC100作为全球首个靶向ICAM-1的第三代CAR-T细胞疗法,通过亲和力调节技术选择性杀伤肿瘤细胞,在前期研究中已显示出针对ATC和PDTC的可接受安全性。
令人振奋的是,在2025年AACR大会上,公布了AIC100的Ⅰ期剂量递增试验(NCT04420754)的最新数据。该研究共纳入24例患者,其中包括8例间变性甲状腺癌(ATC)、7例低分化甲状腺癌(PDTC)患者,中位年龄为59岁(范围:47-69岁),既往接受过中位2线全身治疗(范围:1-4),入组后在4个剂量组(DL)中接受了AIC100输注。

▲截图源自“AACR”
结果显示:在DL2和DL3剂量组(n=9)的可评估患者中,客观缓解率(ORR)为22%,疾病控制率[DCR,客观缓解(ORR)+病情稳定(SD)]高达56%。对于DL2-DL3期的ATC患者(n=4),ORR达50%[DL2期和DL3期分别有1例部分缓解(PR)和完全缓解(CR)]。对于DL2-DL3期的PDTC患者(n=5),DCR为60%。
综上,AIC100在DL2和DL3剂量组中展现出持久缓解潜力,不仅为侵袭性甲状腺癌患者提供了新的治疗希望,更通过概念验证证实了其在晚期癌症中的应用可行性。
国研CEA CAR-T疗法剑指转移性结直肠癌,70%达病情稳定
癌胚抗原(CEA)作为胃肠道癌症的高敏感性标志物,在结直肠癌(CRC)组织及患者血清中广泛表达,因其特异性成为CAR-T疗法的理想靶点。
我国开展过一项针对CEA阳性结直肠癌(CRC)患者的I期临床试验(NCT02349724),共纳入10例中位年龄为58岁(48.8-67岁)且伴肝、肺转移的难治性患者:其中80%(8/10)合并肝转移,50%(5/10)合并肺转移。入组后,接受静脉输注CEA CAR-T细胞治疗。
结果显示:10 例既往治疗中均出现疾病进展(PD)的患者,经CAR-T治疗后,有7例达到病情稳定(SD),肿瘤直径略有变化。其中两例患者(Ps3和Ps5)持续稳定超30周。
值得一提的是,一例代表性病例尤为振奋人心。该患者(患者P10)经DL4剂量CEA CAR-T细胞治疗后,MRI影像学证实肝内单个病灶体积缩小,展现出CAR-T疗法对实体瘤的局部控制潜力(详见下图)。
▼P10患者在CAR-T输注前(左图)和4周后(右图)的MRI评估
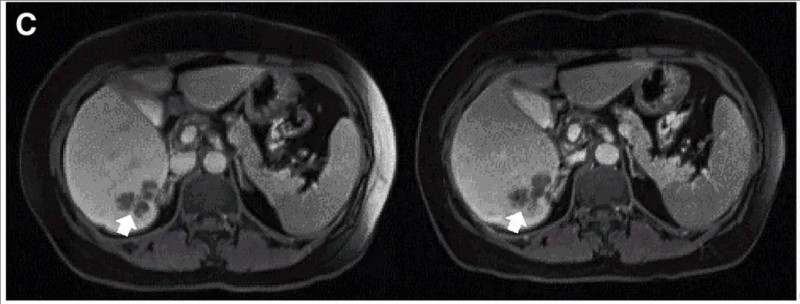
▲图源“Molecular Therapy”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
小编寄语
在现代医学的漫长探索之路上,CAR-T细胞疗法宛如一颗璀璨新星,在恶性肿瘤,尤其是血液肿瘤治疗领域成功实现重大突破,为众多饱受病痛折磨的患者带来希望曙光,使他们得以重获新生,开启全新人生篇章。
令人振奋的是,当前我国CAR-T研发事业开展得如火如荼,呈现出“百家争鸣”的蓬勃景象。以驯鹿医疗、复星凯特、科济生物、传奇生物等一众领军企业,积极投身CAR-T的研发浪潮,且已取得令人瞩目的成果。如果您也想寻求CAR-T细胞疗法,或其他前沿抗癌技术(如TIL、TCR-T、NK细胞等)的帮助,可将治疗经历、近期病理报告、影像学资料等,提交至医学部,进行初步评估或申请国内外抗癌专家会诊。
参考资料
[1]Ramos C A,et al. Anti-CD30 CAR-T cell therapy in relapsed and refractory Hodgkin lymphoma[J]. Journal of clinical oncology, 2020, 38(32): 3794-3804.
https://ascopubs.org/doi/10.1200/JCO.20.01342
[2]Zhong G,et al.Complete remission of advanced pancreatic cancer induced by claudin18.2-targeted CAR-T cell therapy: a case report. Front Immunol. 2024 Feb 29;15:1325860.
https://pmc.ncbi.nlm.nih.gov/articles/PMC10937427/
[3]Srour S A,et al.Abstract CT206: ICAM-1 directed chimeric antigen receptor (CAR) T cells (AIC100) in patients with advanced thyroid cancers: Clinical and translational data from the phase 1 dose escalation study[J]. Cancer Research, 2025, 85(8_Supplement_2): CT206-CT206.
https://www.abstractsonline.com/pp8/#!/20273/presentation/10430
扫描进患者病友群

肺癌|胃癌|肝癌|结直肠癌|胰腺癌
乳腺癌|脑瘤|淋巴瘤|儿童肿瘤等

相关推荐

癌症治疗本就不应千篇一律,揭秘mRNA癌
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
“不限癌种”新突破,NTRK基因融合的靶
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
肺癌疫苗重大突破,晚期患者多了一个新的选
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

“手术成功”不等于万事大吉,新型癌症疫苗
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

2026年靶向治疗抗癌风暴,突破困境,普
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

2026年这些肺癌疫苗正悄然改变患者的生
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05






![[field:title/]](/uploads/allimg/20200224/1-2002241I5262J.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241I3461D.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H94LK.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241HKW34.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H619327.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H34H52.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H22IH.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241G93O18.jpg)




