14天肿瘤极速消退!MHH团队创新疫苗下达"免疫追杀令",横扫肺癌、结直肠癌、胃癌、卵巢癌等
MHH团队创新癌症疫苗下达"免疫追杀令",14天肿瘤极速消退,横扫肺癌、结直肠癌、胃癌、卵巢癌等
人体自身的防御系统堪称生命的“钢铁长城”,不仅能骁勇善战般清除细菌和病毒,更能化身抗癌卫士与癌细胞殊死搏斗!然而狡猾的肿瘤细胞如同擅长伪装的“潜伏者”,通过不断变异变换“身份标签”,屡屡逃脱免疫系统的“火眼金睛”。当传统治疗遭遇瓶颈,人类向癌症宣战的新号角已然吹响——全球医学精英正锚定治疗性癌症疫苗这一战略高地,构筑对抗肿瘤的免疫新防线!
这种充满智慧的免疫疗法,如同给免疫系统配备“精准导航仪”:通过疫苗接种,让免疫大军学会识别肿瘤细胞表面独一无二的“特征密码”(肿瘤抗原),继而精准锁定、全面围剿,其原理恰似人类用疫苗攻克天花、麻疹等顽疾的伟大智慧传承。
而今,汉诺威医学院(MHH)实验室传来振奋全球的医学捷报!一支由顶尖科学家组成的“抗癌突击队”,成功破译肿瘤免疫的关键密码,研发出一种新型强效治疗性疫苗,仅需皮下注射两次(间隔一周),即可在14天内激活免疫系统靶向攻击肿瘤细胞,这一突破性成果已在《细胞与分子免疫学》杂志发表,为癌症患者点亮了新的希望之光——人类距离“以免疫之力终结癌症”的伟大梦想,从未如此接近!

▲截图源自“nature”
从"被动防御"到"主动清零":MHH顶尖团队创新疫苗两针激活免疫风暴,14天精准围剿癌细胞
自2010年黑色素瘤患者III期临床试验首次证实免疫疗法的有效性以来,这一领域已彻底改写全球癌症治疗版图。新冠疫苗中mRNA/LNP技术的革命性突破,更将疫苗开发带入全新时代——其核心优势在于借助脂质纳米颗粒(LNP)精准递送抗原,激活树突状细胞等关键免疫“哨兵”。作为先天免疫系统的“巡逻兵”,树突状细胞通过“吞噬”外来物质(如病毒、细菌或肿瘤细胞),将其分解为肽段抗原碎片,并呈递至细胞表面,犹如举起“通缉令”引导获得性免疫系统的T细胞发动精准攻击。
近十五年来,如何高效激活树突状细胞始终是癌症疫苗研发的核心攻坚方向。如今,汉诺威医学院(MHH)研究团队带来突破性进展:其创新的“基础免疫+加强免疫”两阶段接种方案,通过差异化载体递送相同抗原,实现了免疫应答的“双重激发”:
→第一阶段(初免):将肿瘤抗原肽与免疫激活剂封装于脂质体(荷兰合作研发),皮下注射后引导树突状细胞摄取抗原并“培训”T细胞识别肿瘤特征;
→第二阶段(加强,间隔一周):引入刺激型抗体作为“免疫加速器”,促使特异性T细胞极速增殖,形成压倒性攻击火力。
相较于传统疫苗技术(如体外培养患者树突状细胞或使用肽/蛋白疫苗)存在的免疫反应弱、需频繁接种等瓶颈,该方案通过脂质体载体的靶向递送能力与激动剂的协同效应,仅需两次注射即可触发强效免疫级联反应。在结肠癌小鼠模型的临床前研究中,这一创新疗法展现出震撼疗效:两次接种后,肿瘤组织竟完全消退!此外,实验证实,脂质体的抗原递送效率与异源加强方案中刺激抗体的叠加作用,显著提升了T细胞对肿瘤的识别精度与攻击强度。其两周内起效的快速响应机制,结合可定制化肽段设计,为癌症患者抢占了宝贵的治疗时间窗。
▼异源脂质体疫苗诱导新表位特异性CD8 T细胞应答
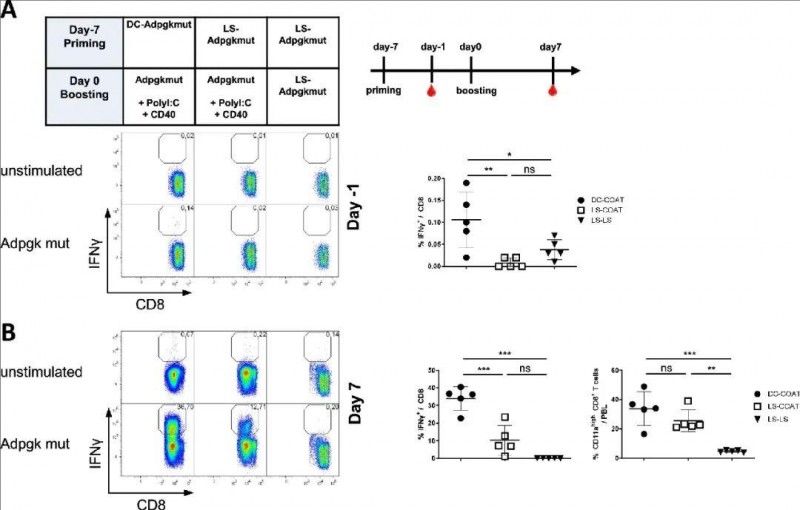
▲图源“cellular & molecular immunology”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
综上,从“被动抵御”到“主动清零”,治疗性癌症疫苗正引领肿瘤治疗向“精准免疫时代”跨越。汉诺威医学院(MHH)团队兼具高效性、速动性与定制性的创新方案,为征服癌症提供了极具潜力的全新范式。接下来的人体临床试验将进一步验证其潜力,我们期待这一技术早日惠及更多患者!
▼个性化新抗原治疗疫苗旨在教导免疫细胞(如T细胞-蓝色)专门识别肿瘤(粉黄色)
▲图源“cellular & molecular immunology”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
HER2自体树突状细胞疫苗在实体瘤中展现"全癌种"响应潜力,横扫卵巢癌、乳腺癌、胃癌、结直肠癌、食管癌等,病灶消失最长超2年
除汉诺威医学院(MHH)团队研发的这款新型强效治疗性癌症疫苗外,全球范围内多款癌症疫苗已在人体临床研究中展现潜力。以HER2表达癌症为例,尽管曲妥珠单抗等靶向药物革新了乳腺癌治疗,但针对其他HER2阳性实体瘤(如卵巢癌、胃癌)的有效疗法仍存缺口。单克隆抗体因单一表位靶向局限,面临抗原逃逸风险(如表达下调或点突变),而疫苗平台通过激活患者自身免疫系统,可诱导针对多个抗原表位的广谱免疫应答,成为破局关键。
《癌症免疫与免疫治疗》杂志曾报道一项针对HER2的自体树突状细胞(DC)疫苗——AdHER2 DC疫苗的I期临床试验(NCT01730118)。
该疫苗专为转移性癌症或高复发风险膀胱癌患者设计,主要通过单采血液成分术收集患者的单核细胞,并将淘洗的单核细胞等分试样冷冻保存,直到制造出每个疫苗剂量,其制备的具体流程如下:
在第0天:将一份等分试样解冻,并重新悬浮在含有细胞因子和血浆的培养基中,保存备用;
在第2天:更换培养基,并添加海兔血蓝蛋白作为免疫佐剂;
在第3天,用携带HER2 ECTM基因的腺病毒载体(AdHER2)转导细胞,诱导抗原表达;第4天,对产品进行审核并包装,制备成可注射的疫苗制剂,以供给药(详见下图)。
▼AdHER2DC疫苗制造示意图
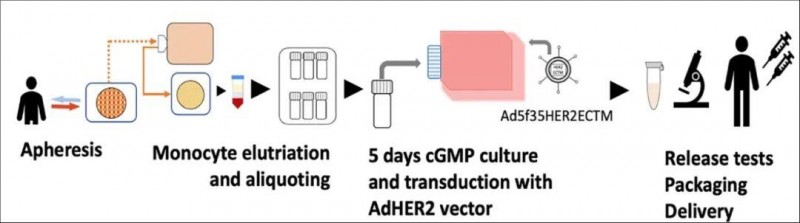
▲图源“frontiers”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
本次研究共纳入33例HER2表达转移性实体瘤患者(含乳腺癌、卵巢癌、胃癌等),其中9例曾接受抗HER2治疗(如曲妥珠单抗),所有患者均接受4个剂量水平(5×10⁶~40×10⁶ DC细胞)的疫苗注射,中位年龄为60岁(范围:36-72岁),中位随访时间为36周(范围:4-124周)。
结果显示:在21例可评估患者中,7例(33.3%)获临床获益,包括乳腺癌患者、1例食管胃交界处癌患者(详见下图)。

▲图源“frontiers”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
值得一提的是,有几则突破性临床案例,引发广泛关注:
一例高级别浆液性卵巢癌患者(患者17,HER2IHC3+,FISH1.3):入组时病变局限于阴道袖状部,在接种4剂疫苗后,病灶完全消退,缓解持续至113周(≈2.35年)。
另一例胃癌患者(患者9,HER2IHC3+,FISH2.5):基线时(治疗前)靶病灶大小为4.7×1.9cm;接种疫苗后第16周,病灶缩小至2.8×1.9cm(靶病变总数减少50%);第24周进一步缩小至1.9×1.9cm(详见下图)。尽管因非靶病灶进展未达部分缓解标准,仍体现了疫苗对HER2阳性胃癌的局部控制能力。
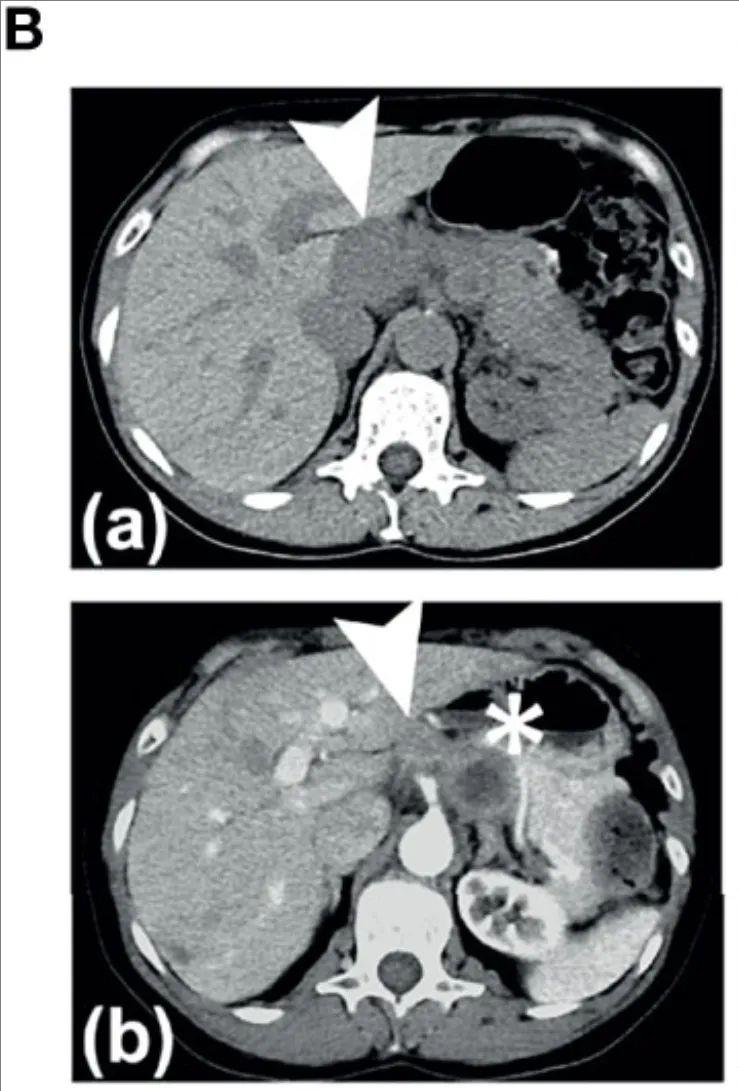
▲图源“frontiers”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
还有一例癌肉瘤型卵巢癌患者(患者21,HER21+,FISH1.0):经5线治疗后入组,疫苗治疗后,靶病灶最大缩小24.8%,并维持48周。
综上,AdHER2 DC疫苗在HER2表达癌症患者中显示出免疫原性和初步临床获益,且安全性良好。该疫苗有望进一步应用于临床,尤其是在联合方案中。
想寻求DC疫苗、古巴肺癌疫苗或其他个性化癌症疫苗帮助的患者,可将近期病理报告、出院小结、治疗经历等资料,提交至医学部,进行初步评估。
结肠癌肝转移术后辅助治疗新突破:树突状细胞疫苗显著延长无病生存期
结肠癌肝转移患者即使接受挽救性手术,仍面临高复发风险(多项研究显示复发率高达50%-60%)。尽管新辅助化疗联合辅助化疗是目前标准方案,但其降低复发的效果仍有限。
《免疫肿瘤学杂志》发表的一项随机II期临床试验(NCT01348256)为该领域带来新希望。研究纳入19例可手术切除的结肠腺癌肝转移患者,所有患者均接受新辅助化疗→肝叶/肝段切除术→辅助化疗的标准化治疗。辅助化疗结束后,15例切缘阴性患者按1∶1随机分配至树突状细胞疫苗接种组(2疗程,每日4次皮内注射)或观察组,中位随访时间为42.58个月。
结果显示:疫苗组复发风险显著降低,DC疫苗组中位无病生存期(DFS)为25.26个月(95%CI,8.74个月-未达到),而观察组仅为9.53个月(95%CI,5.32个月-18.88个月)(详见下图)。显然,疫苗组复发次数明显减少,且复发时间更晚。
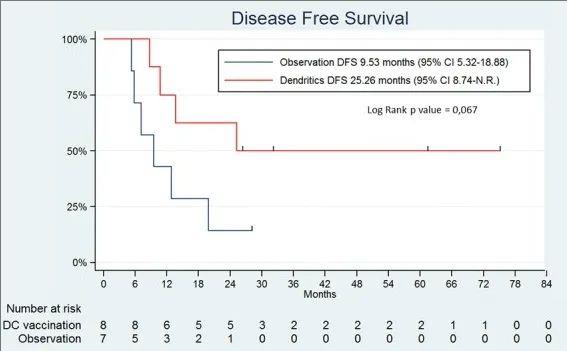
▲图源“J Immunother Cancer”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
综上,该试验首次证实,在标准化治疗基础上联合树突状细胞(DC)疫苗,可通过激活特异性免疫应答延缓结肠癌肝转移术后复发。尽管样本量有限,但其展现的疗效趋势为高危患者提供了“手术+化疗+免疫”的三阶段治疗新范式,后续III期研究值得期待。
古巴肺癌疫苗:首个针对晚期肺癌的治疗性疫苗,5年生存率从0飙升至23%
尽管免疫疗法与靶向疗法不断进步,肺癌仍是全球发病率与死亡率最高的恶性肿瘤之一,其中非小细胞肺癌(NSCLC)占比达 85%,晚期患者总体预后极差。值得关注的是,约 10%-15% 携带 EGFR 突变的患者可通过靶向治疗实现 “长期生存”,而针对无驱动突变的广泛人群,古巴研发的CIMAvax-EGF 治疗性疫苗开辟了全新治疗路径。该疫苗已相继在古巴、秘鲁、阿根廷、哥伦比亚、黑塞哥维那、波斯尼亚等国获批使用。好消息是,目前中国患者也可通过医学部,向古巴医疗部门申请肺癌疫苗,以延长生存期,改善生活质量!

全球首个非小细胞肺癌(NSCLC)治疗性疫苗:双重机制精准"饿死"癌细胞
作为全球首个获批的晚期肺癌治疗性疫苗,CIMAvax-EGF由人重组EGF与载体蛋白P64化学偶联而成,通过双重免疫机制攻击肿瘤:
1、癌细胞生长所需的“养料”——EGF:表皮生长因子(EGF)是癌细胞增殖的关键“养料”,晚期NSCLC患者血清EGF水平显著升高。疫苗诱导的特异性抗体可中和循环EGF,使依赖EGF存活的癌细胞因“营养戒断”而凋亡,正常细胞则通过其他通路维持代谢。
2、阻断EGF及其受体结合,关闭癌细胞无限增殖的“引擎”:EGF与受体(EGFR)结合会激活肿瘤细胞的无限增殖与转移通路(如血管生成、抗凋亡机制)。疫苗通过阻断EGF-EGFR结合,从源头“熄火”癌细胞的失控生长程序,抑制其侵袭能力。
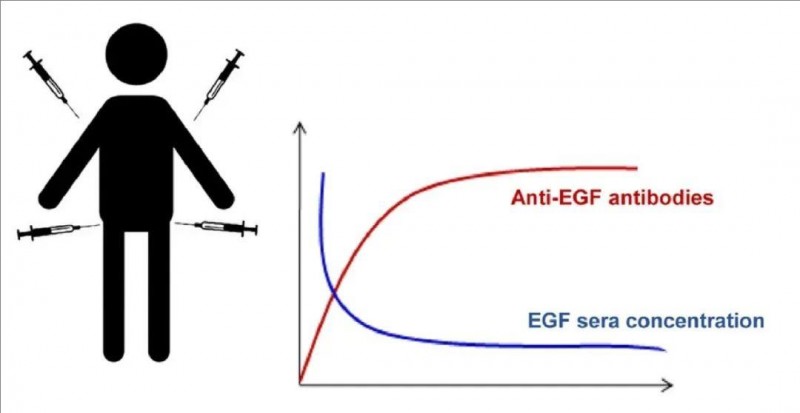
▲图源“Semin Oncol”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
CIMAvax-EGF III 期临床数据:中位生存期超1年,5年生存率提高23%
《FrontOncol》发表的III期随机对照研究(纳入405例晚期NSCLC患者)显示,一线化疗后序贯CIMAvax-EGF疫苗显著改善生存结局。
结果显示:疫苗接种组患者的中位总生存期(OS)为12.43个月,而对照组仅为9.43个月;且疫苗接种组患者的长期生存率高于对照组,2年生存率为37%(疫苗接种组)vs 20%(对照组);5年生存率为23%(疫苗接种组)vs 0%(对照组)。
下图选取了2例具有代表性的患者,在接受CIMAvax-EGF治疗前后的影像学变化,以便更直观地展示该疫苗对肺癌的长期控制效果。
▼两例代表性患者接受CIMAvax-EGF治疗前后的CT对比
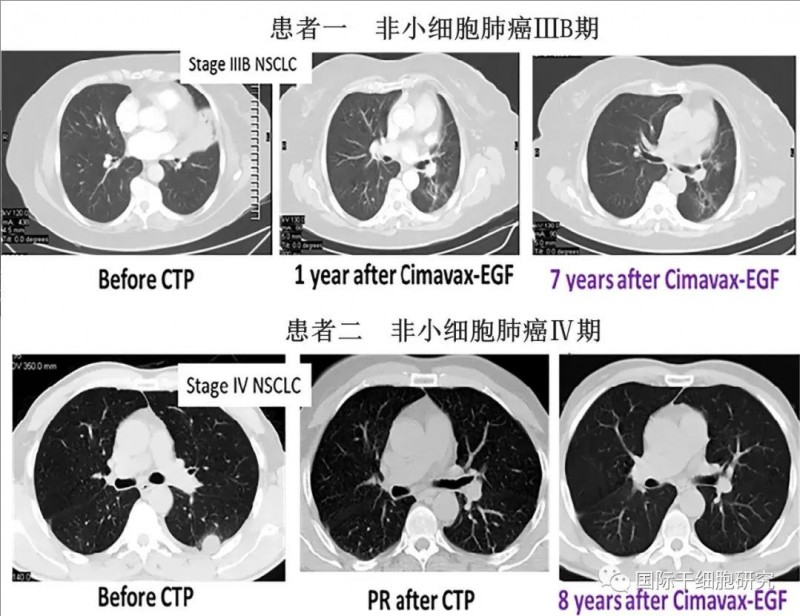
▲图源“frontiers”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
小编寄语
癌症疫苗作为癌症治疗领域的新兴力量,历经数十年的发展,逐渐从基础研究转向了临床研究阶段,近年来更是取得了突破性进展。随着研究的不断深入和技术的不断进步,我们有理由相信,癌症疫苗将在未来的癌症治疗中,发挥越来越重要的作用,还可与手术、化疗、放疗、免疫治疗等传统治疗手段相结合,形成综合治疗方案,为肿瘤患者带来更高的生存获益!小编也期望随着癌症疫苗的不断优化,未来可以创造出更多的抗癌奇迹!想寻求癌症疫苗等新型抗癌疗法帮助的患者,可将治疗经历、近期病理及影像学检查结果等,提交至医学部,进行初步评估或申请国内外抗癌专家会诊。
参考资料
[1]Ostroumov D,et al.Sequential STING and CD40 agonism drives massive expansion of tumor-specific T cells in liposomal peptide vaccines[J]. Cellular & Molecular Immunology, 2025: 1-11.
https://www.nature.com/articles/s41423-024-01249-4
[2]Maeng H M,et al.Phase I clinical trial of an autologous dendritic cell vaccine against HER2 shows safety and preliminary clinical efficacy[J]. Frontiers in Oncology, 2021, 11: 789078.
https://www.frontiersin.org/journals/oncology/articles/10.3389/fonc.2021.789078/full
[3]Rodriguez J,et al.A randomized phase II clinical trial of dendritic cell vaccination following complete resection of newline cancer liver linkstasis. J Immunother Cancer. 2018 Sep 29;6(1):96.
https://pmc.ncbi.nlm.nih.gov/articles/PMC6164167/
扫描进患者病友群

肺癌|胃癌|肝癌|结直肠癌|胰腺癌
乳腺癌|脑瘤|淋巴瘤|儿童肿瘤等

相关推荐

癌症治疗本就不应千篇一律,揭秘mRNA癌
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
“不限癌种”新突破,NTRK基因融合的靶
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
肺癌疫苗重大突破,晚期患者多了一个新的选
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

“手术成功”不等于万事大吉,新型癌症疫苗
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

2026年靶向治疗抗癌风暴,突破困境,普
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

2026年这些肺癌疫苗正悄然改变患者的生
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05






![[field:title/]](/uploads/allimg/20200224/1-2002241I5262J.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241I3461D.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H94LK.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241HKW34.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H619327.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H34H52.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H22IH.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241G93O18.jpg)




