帮免疫系统“重启”,看DC疫苗如何让“绝症”变成慢病
帮免疫系统“重启”,看DC疫苗如何让“绝症”变成慢病
一、当传统疗法“力不从心”,DC疫苗正悄然改写战局
在漫长的抗癌征途中,手术、放疗、化疗、靶向、免疫……几乎所有手段都被反复尝试,可当肿瘤变成“老油条”,学会伪装、抵抗甚至“骗过”免疫系统时,许多患者与家属陷入无力与绝望。
然而,从实验室到临床,一个新的突破方向正悄然崛起——DC疫苗(树突状细胞疫苗)。
它并非某种化学药,也不是单一“进口特效药”,而是一种基于患者自身免疫系统的个体化治疗,医学家希望通过它,让身体重新识别、记住并反击肿瘤。
DC疫苗不是“万能钥匙”,它更像“唤醒者”——让沉睡的免疫系统重新举起武器。
二、“教官”登场,DC疫苗是什么
树突状细胞(Dendritic Cell,简称DC)是一种极为重要的免疫细胞,被誉为“免疫系统的将军”。
它的主要职责是识别外来抗原,并“教导”T细胞该如何识别和攻击这些敌人。
如果将免疫系统比作军队,淋巴细胞是士兵,而树突状细胞就是负责训练他们的教官。
DC疫苗就是把这种“教官”在实验室中特别培养、训练,然后再“派回战场”。
科学家会从患者血液中提取单核细胞,用细胞因子(如GM-CSF、IL-4)诱导其分化成成熟的树突状细胞,再加载上肿瘤特异性抗原(例如癌细胞中的突变蛋白、肿瘤提取物、合成肽等)。
经过这番“军事化培训”,这些DC细胞被回输到患者体内,唤醒T细胞群去识别目标并发动免疫攻击。
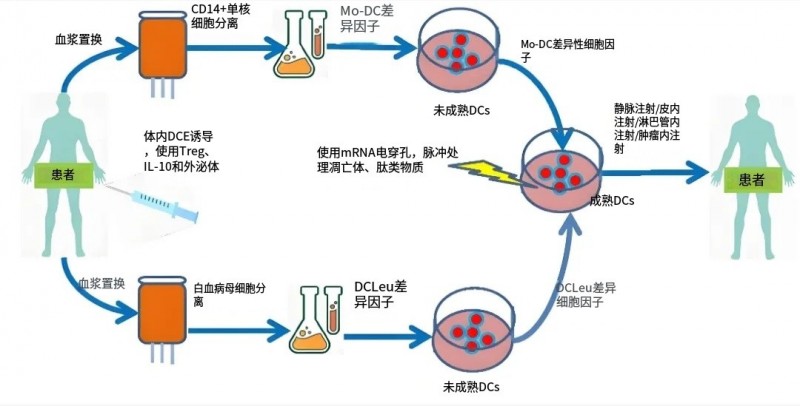
DC疫苗的治疗流程
这一理念充分体现了“以自身之力,治自身之疾”的核心。
三、多方临床证据加持,DC疫苗正在“有据可依”
1、Nature 2025:个体化新抗原疫苗点亮肾癌免疫反应
2025年,《Nature》杂志报道了由麻省总医院与达纳-法伯癌症中心联合开展的一项研究:
研究团队针对高风险肾细胞癌患者制作了个体化的新抗原疫苗(PCV),结果显示:
●所有患者都诱导出针对疫苗抗原的T细胞反应;
●7/9名患者的T细胞能精准识别自身肿瘤;
●反应性克隆能针对驱动突变如 VHL、PBRM1、BAP1、KDM5C、PIK3CA 等关键基因。
这说明个体化DC/PCV疫苗能让免疫系统真正“打到点子上”。
虽然该研究尚未直接验证长期无复发率,但它确立了“免疫系统确实能被唤醒”的坚实证据。
2、V940(mRNA-4157)与PD-1药物联手:降低复发风险近一半
Moderna与默沙东联合开发的V940(mRNA个体化肿瘤疫苗)为免疫疗法领域注入强信号。
在《柳叶刀(Lancet)》发表的Ⅱb期随机试验——KEYNOTE-942中,研究者发现:
●术后高危黑色素瘤患者使用V940 + 帕博利珠单抗(Keytruda)组,18个月无复发生存率达79%,对照组仅62%;
●经长达35个月随访,复发或死亡风险下降49%,远处转移或死亡风险下降62%。
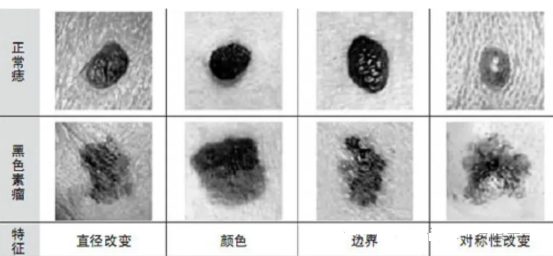
V940治疗黑色素瘤的效果
这项研究已经推进至III期,为癌症术后辅助治疗开辟了全新路径。
3、DCVax-L:让“冷肿瘤”不再冰冷
DCVax-L是最早实现商业化的DC疫苗,最初用于治疗胶质母细胞瘤(GBM)。
发表于《JAMA Oncology(2023)》的大型临床研究显示:
●新诊断GBM患者的中位总生存期提高至19.3月(对照组为16.5月);
●复发人群的中位OS从7.8月跃升至13.2月;
●48个月与60个月的长期生存比例显著提升。
在免疫环境极“冷”的脑肿瘤中,这样的提升极具临床意义——说明DC疫苗有能力改善免疫盲区型癌症的生存期。
4、《Cancer Immunology, Immunotherapy》:肠癌的“冷”被点燃
对MSS型结直肠癌(约占转移性肠癌的95%患者)而言,免疫治疗一直是难啃的“硬骨头”,传统PD-1/PD-L1药物几乎无效。
但近期的I/II期临床结果给出了惊喜——研究者将自体DC疫苗与PD-L1抑制剂Avelumab联合治疗:
●中位总生存期从传统的约5个月延长至12.2个月;
●超过20%的患者病情得到稳定控制;
●副作用温和,可耐受;
●同时揭示了肿瘤代谢重构现象——这一联合机制可能打开“免疫冷肿瘤”的防线。
5、Cureus案例:晚期患者腹水消失,四年半无进展
一位72岁晚期十二指肠癌患者在多个疗程化疗失败后,尝试WT1/MUC1-DC疫苗配合T细胞回输疗法(CAT)。
四年半过去了,他依然生活质量极高,影像学显示无进展(PFS>54月)。
这并非孤例,而是证明:对部分晚期患者而言,DC疫苗可能将“绝症”转化为可控慢病。
6、SITC 2025:小细胞肺癌患者三年生存率超33%
2025年在癌症免疫学会(SITC)公布的一项西班牙多中心临床试验(NCT04487756)报告称:
●DC疫苗+阿替利珠单抗用于广泛期小细胞肺癌(ES-SCLC);
●中位无进展生存期(PFS)4.7月,总生存期(OS)11.2月;
●33%的患者生存超过2年,其中22%在24个月时仍未进展;
●毒副作用轻微,安全性良好。
这在如此恶性癌种中堪称突破,为联合免疫策略提供了现实依据。
四、DC疫苗的独特机制,重塑免疫力的“定制疗法”
DC疫苗的魅力,在于它不是统一配方,而是私人定制:
1、取自患者自身:安全性高、无排异;
2、靶向明确:通过肿瘤突变分析,挑选“免疫显性”的新抗原;
3、可联合可叠加:与PD-1、CTLA-4抑制剂甚至放化疗、靶向疗法联合有协同效应;
4、建立免疫记忆:让免疫系统形成“长期警戒”,降低复发和转移风险。
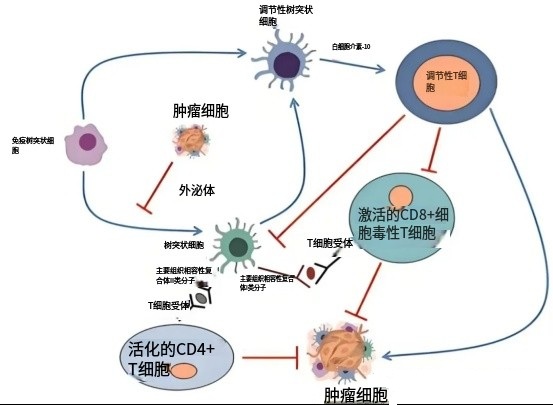
DC疫苗激发T细胞、形成免疫记忆的过程
五、谁能从DC疫苗中获益
结合国内外研究,以下几类人群可能获得更多益处:
●术后高风险患者:如黑色素瘤、肾癌、肺癌等切除后仍存微小残余病灶者;
●标准疗法失败者:经多线化疗、靶向治疗无效的患者;
●MSS型结直肠癌等免疫冷肿瘤;
●希望降低复发风险或改善生活质量者;
●不耐受传统化疗副作用的老年或体弱患者。
不过,医生会根据病理、基因检测与免疫状态综合评估是否适合。
六、前沿探索,国内外应用与未来方向
目前,日本、德国、美国等国家已将DC疫苗列为临床辅助治疗,覆盖肝癌、乳腺癌、肾癌、黑色素瘤等多种实体瘤。
我国在海南博鳌乐城、广州、上海等地,已获批启动个体化mRNA/DC疫苗的早期临床试验,其中再海南博鳌乐成医疗先行区,符合适应症的患者可以合法合规的使用疫苗,目前定价为每次15万元,属于“先行先试”范畴。
未来趋势包括:
●多抗原复合疫苗——同时针对多个突变表位,提高应答率;
●联合免疫组合疗法——与免疫检查点抑制剂协同,“点火+松刹车”;
●AI辅助抗原筛选——通过算法预测最有潜力的免疫靶点;
●DC来源优化——改善制备效率,使之更可及、更普惠。
七、现实与理性,疗效的边界与预期管理
DC疫苗的研究成果令人鼓舞,但专家普遍强调,要理性看待。
它并非“一针见效”的“神药”,而是长期免疫重塑的过程,多数研究仍处于Ⅱ期阶段,虽有部分患者达到长期带瘤生存,但总体疗效需进一步大样本验证。
临床中,医生会谨慎评估,选择最佳联合方案与给药时机(如术后、免疫重塑窗口),以达到理想效果。
八、希望正在重启,让免疫系统重新“看见”癌症
在癌症治疗这场长征中,没有哪一种疗法能包打天下。
但DC疫苗的出现,至少让我们看到了免疫新生的可能。
它不是替代,而是补全免疫拼图的重要一块——让身体重新识别敌人、建立防线、守住希望。
很多曾经走到治疗尽头的患者,如今因DC疫苗联合免疫疗法而延续生命。
这不是奇迹,而是科学的力量,时间与科研正一点点兑现信念。
临床实践证明——当我们敢于了解、敢于尝试,就已经向康复迈出关键一步。
扫描进患者病友群

肺癌|胃癌|肝癌|结直肠癌|胰腺癌
乳腺癌|脑瘤|淋巴瘤|儿童肿瘤等

相关推荐

癌症治疗本就不应千篇一律,揭秘mRNA癌
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
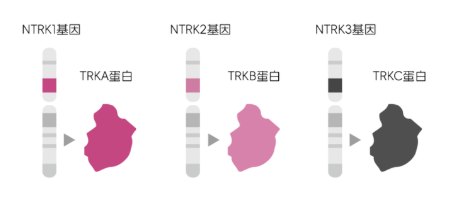
“不限癌种”新突破,NTRK基因融合的靶
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
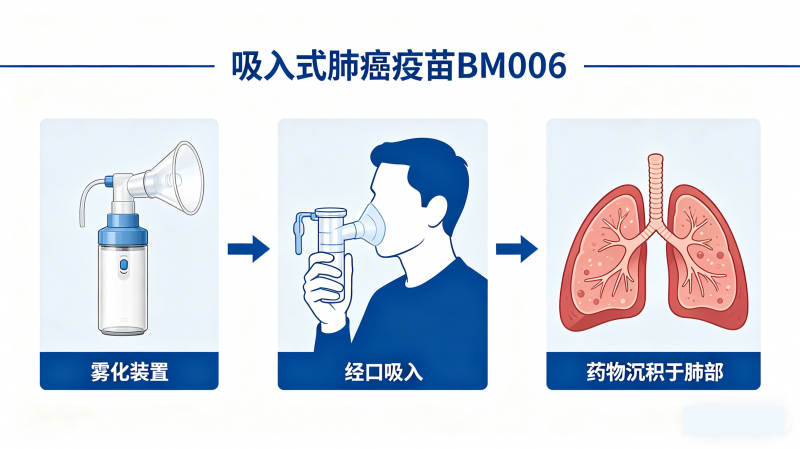
肺癌疫苗重大突破,晚期患者多了一个新的选
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

“手术成功”不等于万事大吉,新型癌症疫苗
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

2026年靶向治疗抗癌风暴,突破困境,普
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

2026年这些肺癌疫苗正悄然改变患者的生
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05






![[field:title/]](/uploads/allimg/20200224/1-2002241I5262J.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241I3461D.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H94LK.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241HKW34.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H619327.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H34H52.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H22IH.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241G93O18.jpg)




