耐药患者别放弃!粪菌移植联合免疫治疗,实体瘤控制率超46%!
PD1耐药的新克服技术,粪菌移植(FMT)联合免疫治疗,实体瘤控制率超46%
知名SCI期刊《影响因子》发表的一项临床试验(NCT04264975)证实,富含有益菌群的粪便菌群移植(FMT)联合抗PD-1抑制剂,可帮助晚期实体癌(尤其胃肠道癌)患者克服PD-1抑制剂耐药性,对耐药晚期实体癌治疗显效,且FMT能通过诱导部分应答增强免疫力。
这一突破性发现曾经陷入PD-1耐药的晚期实体癌患者,看到了延长生存、改善预后的新希望,为肿瘤免疫治疗耐药难题的攻克注入了强劲动力!
▲截图源自“Cell Host & Microbe”
FMT联合纳武单抗突破PD-1耐药困境,实体瘤疾病控制率高达46.2%,肝癌肿瘤显著缩小47.7%
该研究共纳入13例抗PD-1治疗难治性晚期实体癌患者,包括4例转移性胃癌(GC)、5例食管鳞状细胞癌(ESCC)、4例肝细胞癌(HCC),患者中位年龄为60岁(范围:38-76岁),均接受过大量既往治疗(中位10次全身治疗,范围:4-34次),且均在纳武单抗(nivolumab)单药治疗后确认病情进展。
结果显示:13例患者中,粪便菌群移植(FMT)联合纳武单抗治疗,诱导6例出现持续菌群变化及临床获益,包括1例达到部分缓解(PR)、5例达到病情稳定(SD),客观缓解率(ORR)为7.7%,疾病控制率(DCR)达46.2%。
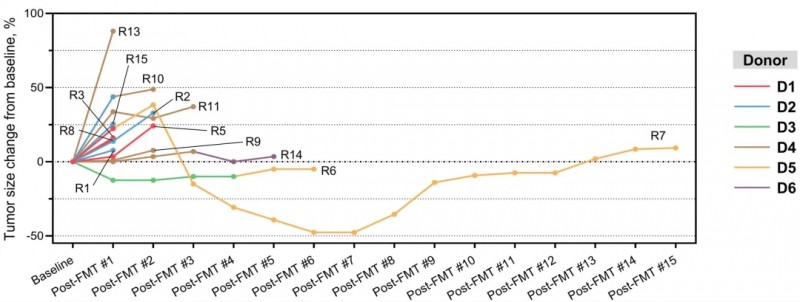
▲图源“Cell Host Microbe”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
尤为显著的是一例转移性肝细胞癌病例(患者R7):该患者对纳武单抗存在原发性耐药,在接受FMT联合持续免疫治疗后,肿瘤病灶逐步缩小,在第2次FMT后8周缩小30.5%,后续进一步缩小至47.7%,最终达到部分缓解(PR,详见下图)。同时,血清甲胎蛋白(AFP)、PIVKA-II等肿瘤标志物显著下降。
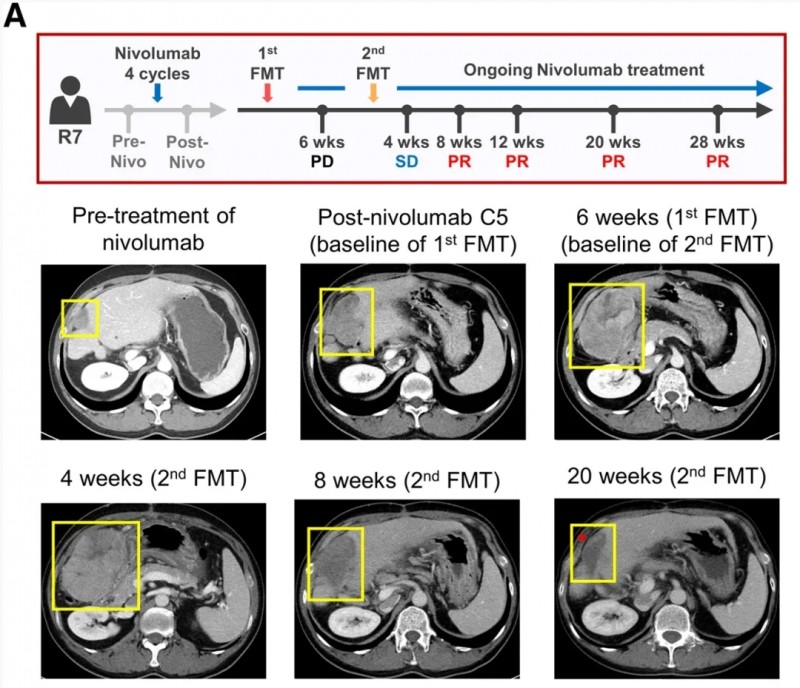
▲图源“Cell Host Microbe”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
这一案例印证了FMT联合免疫治疗可通过改变肠道微生物组产生显著临床疗效,凸显了该联合疗法的潜力。
粪便微生物移植(FMT):隐藏的超级抗癌武器
肠道作为人体最大的消化器官,也是与外界接触最广泛的器官之一,约70%的免疫细胞聚集于此。肠道内栖息着百万亿级的微生物群(包含细菌、真菌、病毒等),它们共同守护宿主健康,堪称隐藏在肠道中的“秘密抗癌武器”。
01、何谓粪便微生物移植(FMT)
粪便微生物移植(FMT)是一种直接操纵肠道微生物群的方法,从健康人身上采集的粪便样本,通过口服冻干、冷冻胶囊、结肠镜或胃镜等方式,从供体转移到患者体内,以重建具有正常功能的肠道菌群,恢复微生物的多样性(详见下图)。
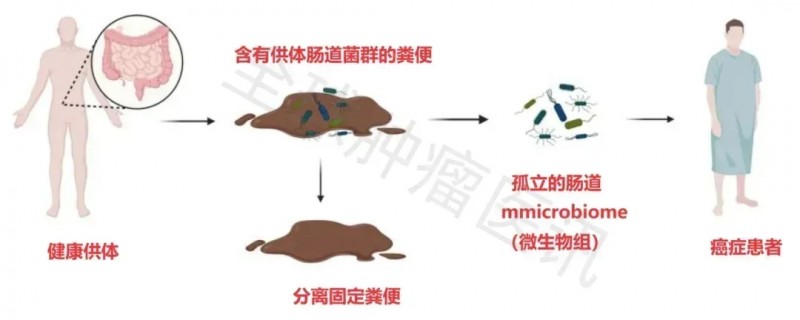
▲图源“Curr Treat Options Oncol”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
02、肿瘤患者如何检测肠道菌群
研究发现,每个人的肠道菌群组成具有独特性,癌症患者与健康人群的菌群结构差异显著。肠道菌群检测通过二代高通量基因测序技术(16S rDNA),可精确解析:菌群种类、数量及丰度分布;评估慢病进展、预警疾病风险;反映癌症患者菌群平衡情况,为个性化“养菌+种菌”方案提供依据,目标包括:平衡免疫系统、增强免疫细胞抗肿瘤活性、辅助防癌抗癌。
检测申请流程:
1、样本提交:按标准采集并提交粪便样本;
2、权威检测:由我们送专业机构进行高通量测序;
3、精准解读检测结果:如发现异常,医学部协助患者对接肿瘤免疫权威专家制定调节方案。
小编寄语
肠道菌群作为人体内部生态的关键“守护者”,与癌症防治紧密交织,恰似为抗癌之战精心构筑的一道“隐形防线”。通过科学有效的调节举措,不仅能为患者的整体健康状况筑牢根基、添砖加瓦,更能显著提升抗癌及免疫治疗的“战斗力”,巧妙化解手术与放化疗带来的诸多副作用“难题”,肠道菌群调节也称为了继免疫细胞疗法、癌症疫苗之后的又一“抗癌新星”。
对于大多数肿瘤患者来说,调节肠道菌群有助于提升机体免疫功能、增强目前抗癌药物的疗效,同时,还有助于提高患者对传统治疗方法的敏感性,降低放化疗及手术治疗的副作用。但小编也需要提醒广大癌友,若癌症患者一旦无法维持正常的营养需求和健康的体重时,需及时接受专业的营养支持,包括口服营养补充、肠外营养支持等。想了解粪菌移植、肠道菌群或定制益生菌更多讯息的患者,可将近期影像和病理检查结果、治疗经历等资料,提交至医学部,咨询权威的营养专家。
参考资料
[1]Kim Y,et al.Fecal microbiota transplantation improves anti-PD-1 inhibitor efficacy in unresectable or metastatic solid cancers refractory to anti-PD-1 inhibitor[J]. Cell Host & Microbe, 2024.
https://www.sciencedirect.com/science/article/pii/S1931312824002282?via%3Dihub
扫描进患者病友群

肺癌|胃癌|肝癌|结直肠癌|胰腺癌
乳腺癌|脑瘤|淋巴瘤|儿童肿瘤等

相关推荐

癌症治疗本就不应千篇一律,揭秘mRNA癌
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
“不限癌种”新突破,NTRK基因融合的靶
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
肺癌疫苗重大突破,晚期患者多了一个新的选
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

“手术成功”不等于万事大吉,新型癌症疫苗
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

2026年靶向治疗抗癌风暴,突破困境,普
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

2026年这些肺癌疫苗正悄然改变患者的生
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05






![[field:title/]](/uploads/allimg/20200224/1-2002241I5262J.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241I3461D.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H94LK.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241HKW34.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H619327.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H34H52.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H22IH.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241G93O18.jpg)




