33%生存超两年+控病率超91%!2025 DC疫苗在肺癌、肝癌、胰腺癌等实体瘤中斩获生存佳绩!
33%生存超两年+控病率超91%,2025年DC疫苗有望在肺癌、肝癌、胰腺癌等实体瘤中斩获新的生存佳绩
广泛期小细胞肺癌(ES-SCLC)是癌症已扩散至肺部以外器官的晚期病症,以进展迅速、治疗难度大为显著特点。尽管PD-L1抑制剂阿替利珠单抗已被纳入一线化疗方案,但这类患者的预后依旧不佳,总生存期(OS)的改善效果十分有限,因此,迫切需要探索新的治疗方法。
在2025年癌症免疫治疗学会(SITC)年会上,公布了一项1b/2期临床试验的振奋成果:树突状细胞(DC)疫苗与阿替利珠单抗的联合疗法,不仅帮助部分ES-SCLC患者实现了长期生存,更在长期生存患者群体中展现出良好的安全性。这一突破不仅为晚期小细胞肺癌患者带来了新的生存希望,更标志着免疫联合疗法在攻克难治性肿瘤的道路上又迈出了关键一步。随着研究的持续深入,相信未来会有更多创新方案涌现,为更多患者点亮生命的曙光。
▲截图源自“cancernetwork”
33%患者生存期超24个月!DC疫苗联合疗法让部分广泛期小细胞肺癌患者实现长期生存
2025年癌症免疫治疗学会(SITC)年会上,公布的这项评估树突状细胞(DC)疫苗联合阿替利珠单抗治疗广泛期小细胞肺癌(ES-SCLC)的1b/2期临床试验(NCT04487756),共纳入20例ES-SCLC患者,其中18例接受DC疫苗接种(中位接种剂量3剂,范围1-6剂),研究中位随访时间达25.7个月。
结果显示:患者的中位无进展生存期(PFS)为4.7个月(95%CI:4.2-6.9),中位总生存期(OS)为11.2个月(95%CI:6.3-17.9)。其中33%(n=6)的患者生存期超过24个月,22%(n=4)在24个月时仍处于无进展状态。
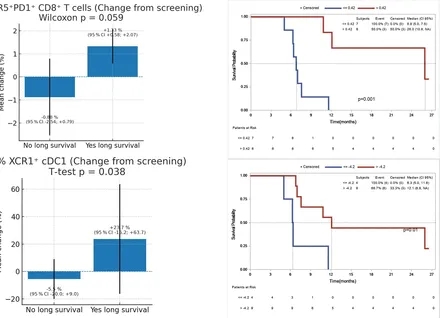
▲图源“BMJ”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
综上,对于部分ES-SCLC患者,采用化疗联合阿替利珠单抗诱导治疗,后续衔接DC疫苗接种与阿替利珠单抗维持治疗的方案,能够帮助其实现长期生存。
2025肝癌重磅突破!DC疫苗联合TACE让中晚期患者无进展生存从10.4跃升至18.6个月,疾病控制率高达91.7%
肝细胞癌(HCC)是全球第七大常见癌症,也是第三大癌症相关死亡原因。对于不适合肝移植、门静脉血供良好且肿瘤负荷明确的中晚期HCC患者,经动脉化疗栓塞术(TACE)凭借两项小型随机试验及其后续荟萃分析的证据,被推荐为一线治疗方案。但TACE并非治愈性疗法,疾病进展难以避免,因此,迫切需要探索联合新型疗法。
《临床癌症研究》2025年刊载的一项研究显示,利用体外经HepG2细胞系裂解物脉冲处理的树突状细胞(DC),可在部分晚期肝细胞癌患者中诱导抗原特异性T细胞反应。在此基础上,一项名为ImmunoTACE的Ⅱ期临床试验进一步评估了该DC疫苗联合TACE治疗中晚期HCC患者的初步疗效。
该研究共纳入55例经组织学或细胞学确诊的肝细胞癌(HCC)患者,将其随机分为两组:第1组(27例,接受TACE联合环磷酰胺预处理)、第2组(28例,接受TACE联合环磷酰胺预处理及DC输注)。最终48例患者可进行疗效评估,两组各24例。结果显示如下:
1、中位无进展生存期(PFS):依据RECIST标准,第2组患者中位无进展生存期(PFS)达18.6个月,显著优于第1组的10.4个月(HR=0.43;单侧80%置信区间上限为0.57;P=0.016,图3A)。
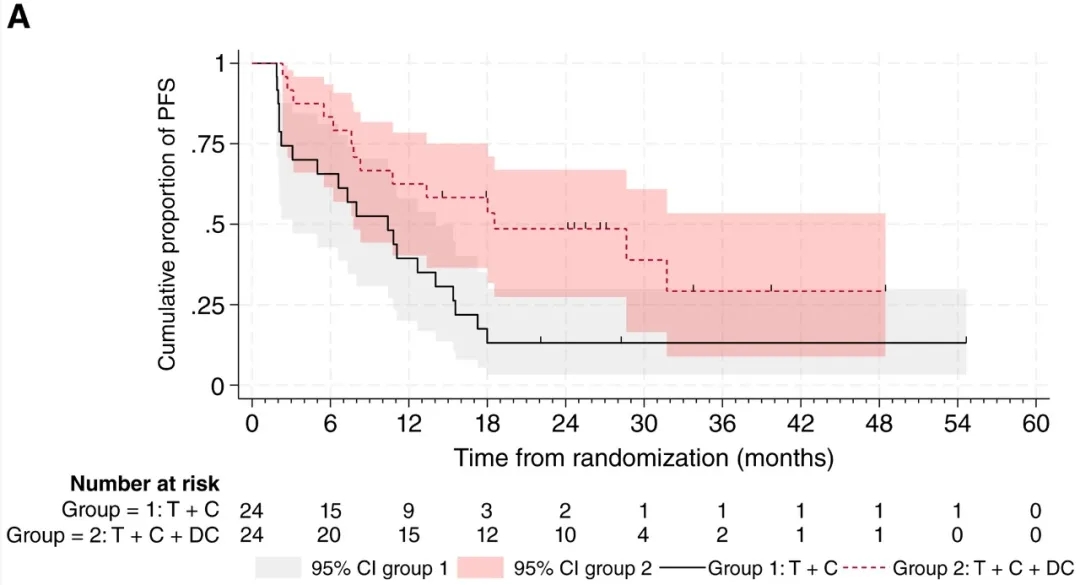
▲图源“AACR”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
2、中位总生存期(OS):第1组中位OS为21.5个月,第2组为25.7个月(HR=0.61;95%CI,0.27–1.38,图3C)。
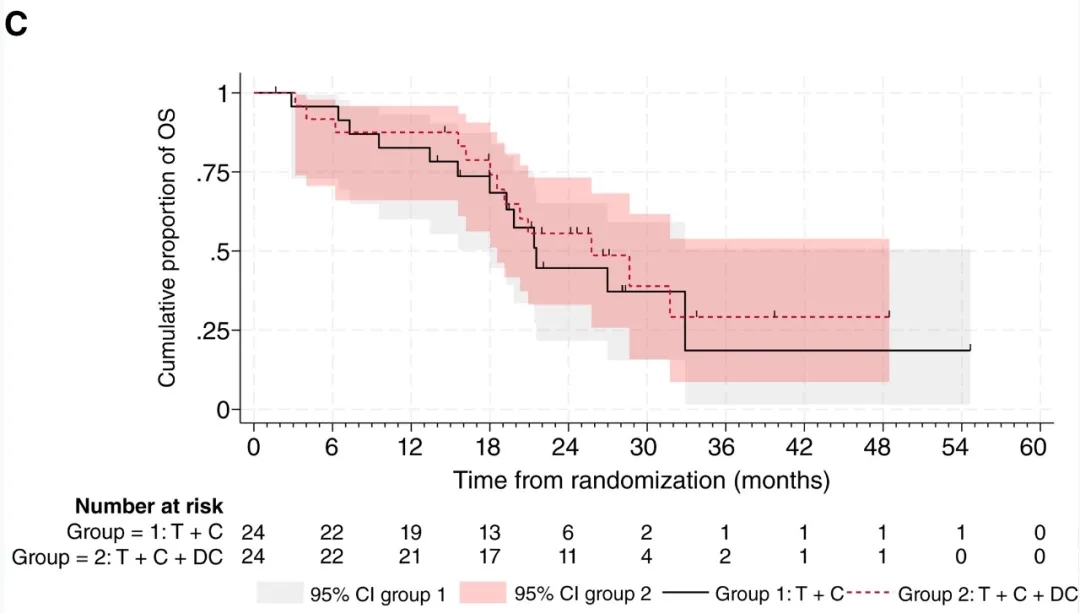
▲图源“AACR”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
3、客观缓解率(ORR):依据本地评估的RECIST1.1标准,第2组客观缓解率(ORR)为54.2%(13/24),显著高于第1组的29.2%(7/24)。
4、疾病控制率(DCR):第2组的DCR也明显优于第1组,分别为91.7%(第2组,22/24) vs 66.7%(第1组,16/24)。此外,DC输注未显著增加不良事件的发生率或严重程度,且接受DC疫苗接种的患者观察到甲胎蛋白特异性免疫反应增强。
综上,在TACE基础上联合DC输注与环磷酰胺预处理,展现出令人鼓舞的初步疗效,值得开展更大规模的随机对照试验进一步验证。
Neo-PDC疫苗攻破胰腺癌术后难关,激活81.3% T细胞诱导率,辅助治疗61个月全存活
2025年4月,《癌症免疫与免疫疗法》刊载一项回顾性研究,专门评估新抗原肽脉冲树突状细胞(Neo-PDC)疫苗在胰腺癌患者术后的安全性与有效性。研究共纳入16例胰腺癌术后患者接受该疫苗接种,其中9例为术后复发患者,7例为胰腺切除术后辅助治疗患者。
核心免疫应答数据显示,16例患者中81.3%(13例)成功诱导产生新抗原特异性T细胞,为抗肿瘤免疫应答提供了关键支撑。
进一步分层分析结果显示:该疫苗在不同治疗场景下均展现出突出疗效:在7例接受疫苗辅助治疗的患者中,中位随访61个月(范围:25-70个月)内全部存活,仅1例出现单发肝转移复发,经射频消融治疗后病灶消失,且术后50个月无新复发迹象;在9例复发后接种疫苗的患者中,7例T细胞诱导应答者的总生存期显著优于无应答者,其中3例患者复发后生存期超过36个月(详见下图),实现了长期生存的突破。
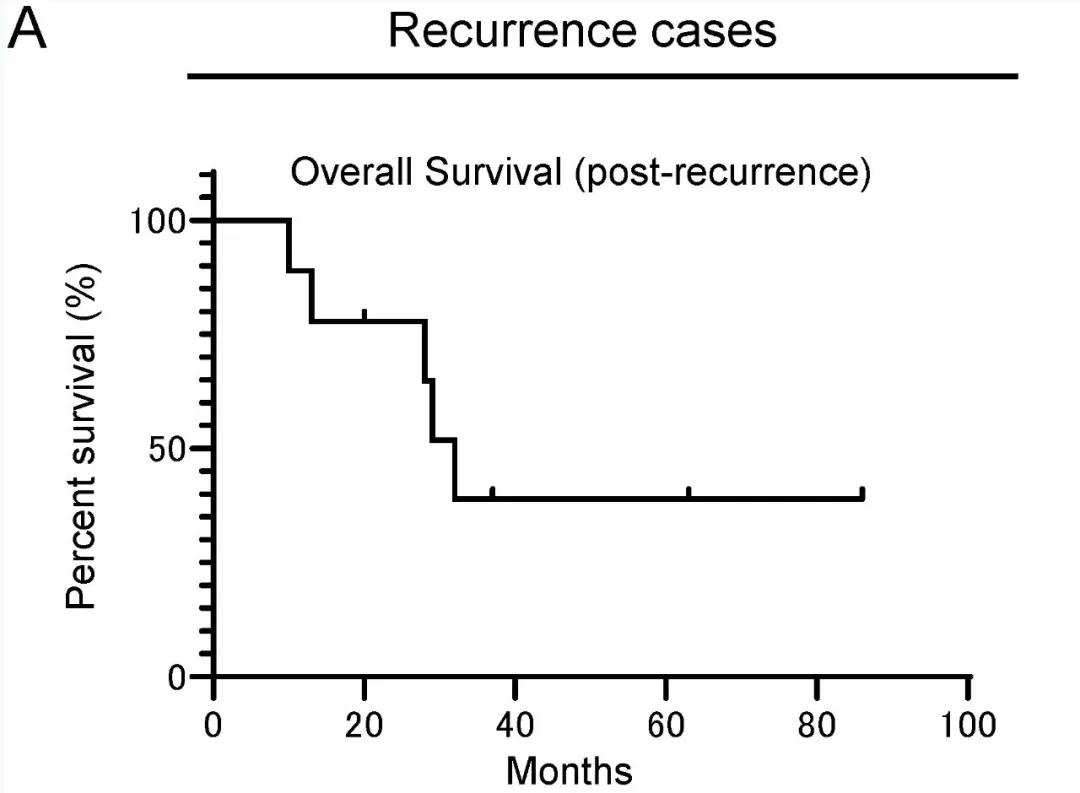
▲图源“frontiers”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
值得一提的是,一例复发患者(#8病例)更具代表性:该患者为一例ypT3N2M0Ⅲ期胰头癌术后复发者,经新辅助化疗、辅助化疗及mFFX方案全身化疗后病情仍进展,于术后31个月启动Neo-PDC疫苗联合改良FOLFIRINOX(mFFX)方案全身化疗。完成6次疫苗接种后,CT扫描证实转移灶显著缩小(详见下图),这一结果也验证了长肽在靶向CD4⁺T细胞、增强疫苗疗效中的关键作用。
▼计算机断层扫描图像显示Neo-PDC疫苗治疗前后转移病灶的变化
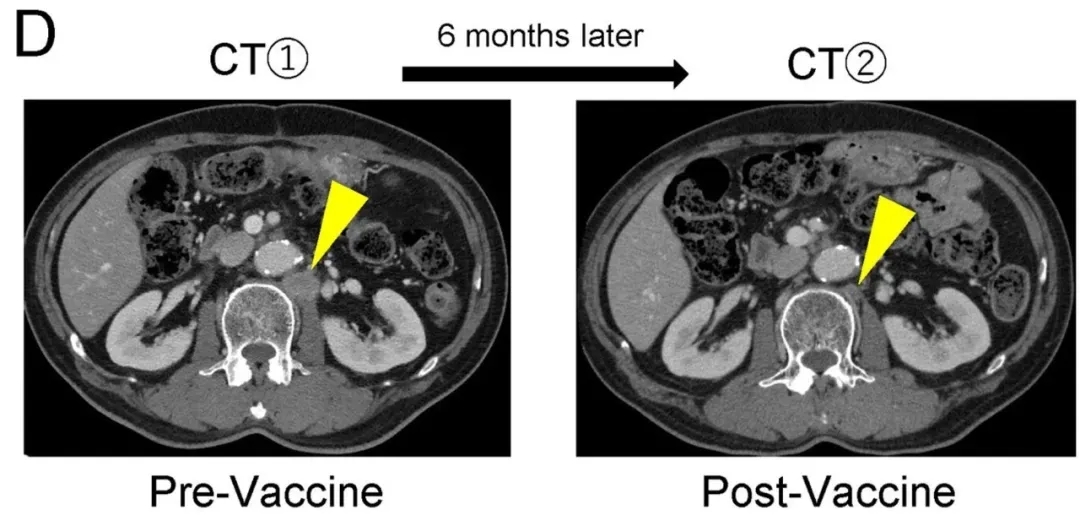
▲图源“frontiers”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
小编寄语
树突状细胞(DC)作为体内唯一能激活初始T细胞的抗原提呈细胞,在免疫反应中占据核心地位。目前,DC疫苗虽多数仍处于早期临床试验阶段,但已在部分国家正式应用于临床。对于早期肿瘤患者,术后采用DC疫苗联合放化疗的辅助治疗方案,可通过清除残留癌细胞、形成免疫记忆,降低复发转移风险。
树突状疫苗在日本、德国等,用于临床辅助治疗多种癌症,包括皮肤癌、肝癌、肺癌、肾癌、乳腺癌等,是癌症患者的新希望!值得欣慰的是,如今我国也有多款癌症疫苗正在开展临床研究,这也意味着中国患者也有机会寻求这款抗癌新技术的帮助!
对目前治疗方案不满意,或想寻求树突状细胞疫苗等抗癌新技术帮助的患者,可将近期病理报告、影像学检查资料、治疗经历等,提交至医学部,进行初步评估。
参考资料
[1]Gonzalez-Cao M,et al.350 Long term survivors from Phase Ib-II trial of tumor-loaded monocyte-derived dendritic cell vaccination plus atezolizumab in ES-SCLC[J]. 2025.
https://jitc.bmj.com/content/13/Suppl_2/A400?utm_source=researchgate.net&utm_medium=article
[2]Gonzalez-Cao M,et al.350 Long term survivors from Phase Ib-II trial of tumor-loaded monocyte-derived dendritic cell vaccination plus atezolizumab in ES-SCLC[J]. 2025.
https://aacrjournals.org/clincancerres/article/31/16/3412/763982/Addition-of-Dendritic-Cell-Vaccination-to
[3]Oyama K,et al.Neoantigen peptide-pulsed dendritic cell vaccine therapy after surgical treatment of pancreatic cancer: a retrospective study[J]. Frontiers in Immunology, 2025, 16: 1571182.
https://www.frontiersin.org/journals/immunology/articles/10.3389/fimmu.2025.1571182/full
[4]https://www.cancernetwork.com/view/atezolizumab-vaccine-combo-may-show-long-term-survival-in-es-sclc
扫描进患者病友群

肺癌|胃癌|肝癌|结直肠癌|胰腺癌
乳腺癌|脑瘤|淋巴瘤|儿童肿瘤等

相关推荐

癌症治疗本就不应千篇一律,揭秘mRNA癌
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
“不限癌种”新突破,NTRK基因融合的靶
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
肺癌疫苗重大突破,晚期患者多了一个新的选
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

“手术成功”不等于万事大吉,新型癌症疫苗
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

2026年靶向治疗抗癌风暴,突破困境,普
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

2026年这些肺癌疫苗正悄然改变患者的生
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05






![[field:title/]](/uploads/allimg/20200224/1-2002241I5262J.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241I3461D.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H94LK.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241HKW34.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H619327.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H34H52.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H22IH.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241G93O18.jpg)




