无癌生存4年!国研全球首创TIL三联疗法划时代攻克肝癌!还可惠及肺癌、乳腺癌、宫颈癌等
无癌生存4年!国研全球首创三联TIL细胞疗法划时代攻克肝癌!还可惠及肺癌、乳腺癌、宫颈癌等
近日,华中科技大学附属同济医院与华中科技大学软件学院合作,全球首次采用“自体肿瘤浸润淋巴细胞(TIL)+PD-1抑制剂+AI”联合疗法,助两位伴门静脉癌栓(PVTT)及肺转移的晚期肝细胞癌(aHCC)患者达到完全缓解,分别保持无瘤生存2年和4年,相关研究成果已刊发于国际权威期刊《肝癌》。
这一全球首创的突破,不仅为晚期肝癌伴转移患者点亮了生命新曙光,更彰显了中国在TIL细胞精准治疗领域的领跑实力,为全球癌症治疗难题的破解提供了极具价值的中国方案!
国研全球首创TIL三联疗法:肝癌治疗划时代突破,晚期转移患者最长无瘤生存4年
01、同济团队研发自体TIL+PD-1抑制剂+AI联合疗法:中国力量开启肝癌治疗新篇章
肝细胞癌(HCC)是全球第六大常见恶性肿瘤及第三大癌症相关死亡原因,中国病例占全球半数以上,约55%初诊时已属晚期。根据BCLC、NCCN、AASLD等指南,晚期患者(aHCC)不适合手术,需接受靶向药物或免疫疗法等全身治疗。尽管阿特珠单抗联合贝伐珠单抗客观缓解率达27.3%,但中位无进展生存期仅6.8个月,多数患者获益有限且易耐药;同时,肝癌早期隐匿、进展迅速,约70%患者初诊为中晚期而丧失手术机会,即便早期手术,术后5年复发率仍高达70%左右,治疗形势严峻。因此,迫切需要寻求新的治疗策略。
肿瘤浸润淋巴细胞(TILs)过继性细胞治疗为个体化免疫治疗方式,具有T细胞克隆多样性高、肿瘤抗原识别精准、归巢能力强、脱靶毒性低等优势,近年已在黑色素瘤、宫颈癌、非小细胞肺癌、乳腺癌等疾病中展现出持久临床疗效。
在此背景下,华中科技大学附属同济医院与软件学院合作,全球首次研发“自体TIL+PD-1抑制剂+AI”联合疗法,成功治愈两位伴门静脉癌栓(PVTT)及肺转移的晚期患者,相关成果刊发于《肝癌》期刊。该疗法核心逻辑为:从患者肿瘤组织分离TIL,经体外扩增后回输体内,其可迁移至肿瘤及转移灶;联合PD-1抑制剂可阻断肿瘤免疫逃逸,增强TIL对肿瘤细胞的杀伤能力,实现“1+1>2”的治疗效果。
在应用场景方面,该联合疗法提供了多元新思路:对伴有血管侵犯、术后高复发风险的患者,可术中同步提取TIL,扩增后回输以助力肿瘤根治、降低复发率;对无手术指征的患者,有望实现传统治疗难以达成的疗效突破。尽管仍需更多临床数据支撑,但该疗法为肝癌治疗创新提供了重要探索方向。
▲截图源自“Karger”
02、突破不可能!两例晚期肝癌伴转移患者,靠TIL细胞三联疗法实现2年/4年长期无瘤生存
《肝癌》杂志报道了两例应用全球首创“TIL+PD-1+AI”三联疗法治疗晚期肝癌的成功案例,目前两名患者分别生存超24个月和48个月,无需进一步抗肿瘤治疗,已恢复正常生活。具体情况如下:
患者1
患者1是一位49岁男性,因肝细胞癌破裂入院。上腹部CT显示左肝叶多发病灶(最大病灶71×48mm),左侧门静脉充满肿瘤血栓;肺部CT发现多个结节。甲胎蛋白水平超60,500ng/mL,确诊为乙型肝炎病毒(HBV)相关性肝细胞癌,BCLC分期为C期。
患者入组I期临床试验(NCT03658785)后,先接受左半肝切除术,并获取肿瘤组织用于TIL培养。之后相继接受淋巴细胞清除方案(环磷酰胺+氟达拉滨)、TIL细胞回输治疗、白细胞介素-2(IL-2)治疗、两次托利普利单抗注射治疗。
结果显示:肝切除术后2个月,所有肺转移灶完全消失,至今(48个月)仍保持无瘤状态(详见下图a、b)。
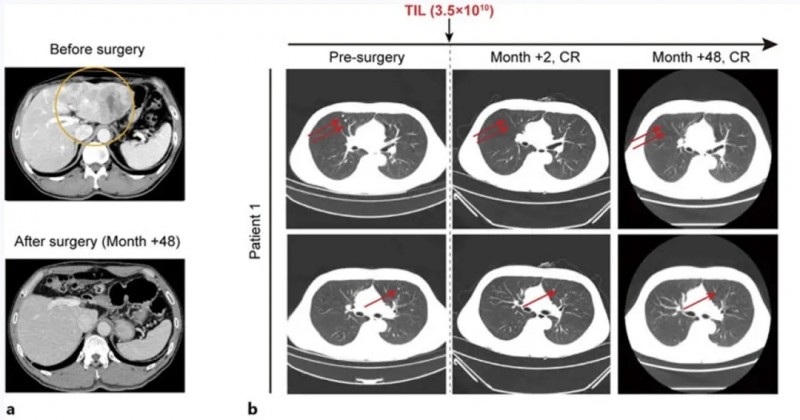
▲图源“Liver Cancer”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
患者2
患者2是一位67岁女性,因肿瘤破裂出血接受经肝动脉栓塞术后1周入院。CT显示肝左叶147×79mm混合信号肿块,双肺存在多个散在结节,右肺中叶最大结节直径18mm。甲胎蛋白水平14,529ng/mL,确诊为HBV相关性肝细胞癌,BCLC分期为C期。
该患者入组后,接受了姑息性左半肝切除术,在TIL培养29天后,先后接受淋巴细胞清除治疗+自体TIL细胞单次输注+IL-2治疗+特瑞普利单抗治疗(18个疗程)。
结果显示:肝切除术后1个月,肺转移灶进展,右肺结节增大至25mm;接受TIL输注及常规抗PD-1治疗后,术后10个月肺病灶完全消失,至今24个月仍保持无瘤状态(详见下图c、d)。
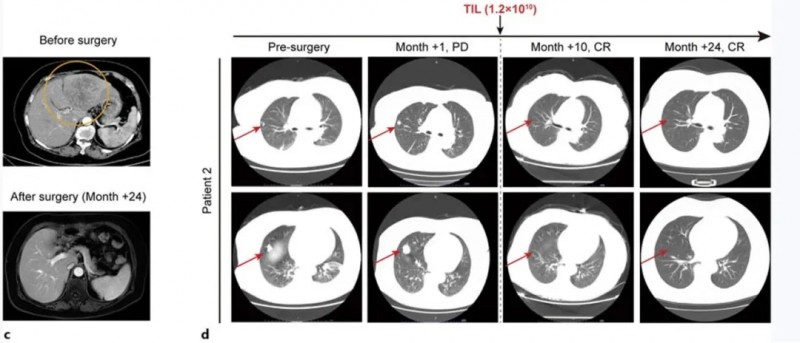
▲图源“Liver Cancer”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
好消息是,目前我国已研发出多款针对实体瘤的TIL疗法,并在国内多家知名癌症中心启动临床,主要针对肺癌、宫颈癌、乳腺癌、黑色素瘤、卵巢癌、消化系统肿瘤等恶性实体瘤。
想寻求TILs及其他国内外抗癌新技术帮助的患者,可先将病历、近期病理报告、基因检测报告等资料,提交至医学部,初步评估是否有机会参加相关临床试验。一旦审核通过,有机会获得”天价“疗法免费治疗的机会。
从"化疗无效"到"病灶全消"!HPV-TILs疗法助两例进展期转移性宫颈癌实现持久完全缓解
转移性宫颈癌属化疗难治性上皮恶性肿瘤,而过继性T细胞疗法(ACT)通过输注自体肿瘤反应性T细胞,已使部分B细胞恶性肿瘤及转移性黑色素瘤患者实现完全临床缓解。《临床肿瘤学杂志》报道了一项HPV靶向肿瘤浸润T细胞(HPV-TILs)治疗晚期宫颈癌的临床研究,其中2例患者实现了奇迹般的完全缓解。
该研究纳入9例转移性宫颈癌患者,均接受过铂类化疗或放化疗失败,中位年龄37岁(范围30-59岁),肿瘤类型包括鳞状细胞癌4例、腺癌3例、腺鳞癌2例。入组后患者先接受淋巴细胞清除化疗,随后单次输注优先筛选出的人乳头瘤病毒(HPV)E6和E7反应性HPV-TILs,最后给予白介素-2(IL-2)治疗。
结果显示:9例患者中3例出现肿瘤客观缓解(ORR),其中2例达完全缓解(CR),分别持续22个月、15个月。另1例达到部分缓解(PR),持续3个月。这两例治疗后达到完全缓解患者的疗效值得广泛关注。
患者3
患者3是一位患有转移性鳞状细胞癌的女性,此前接受过多线治疗,包括顺铂+长春新碱+博来霉素诱导化疗、吉西他滨+顺铂放化疗,后续出现气管旁、隆突下及双侧肺门淋巴结转移,经拓扑替康+紫杉醇治疗后病情仍进展,治疗时肿瘤已转移至腹主动脉旁、双侧肺门、隆突下及髂淋巴结。接受HPV-TIL治疗后,所有病灶完全消退(详见下图A、C),治疗后22个月无疾病复发。
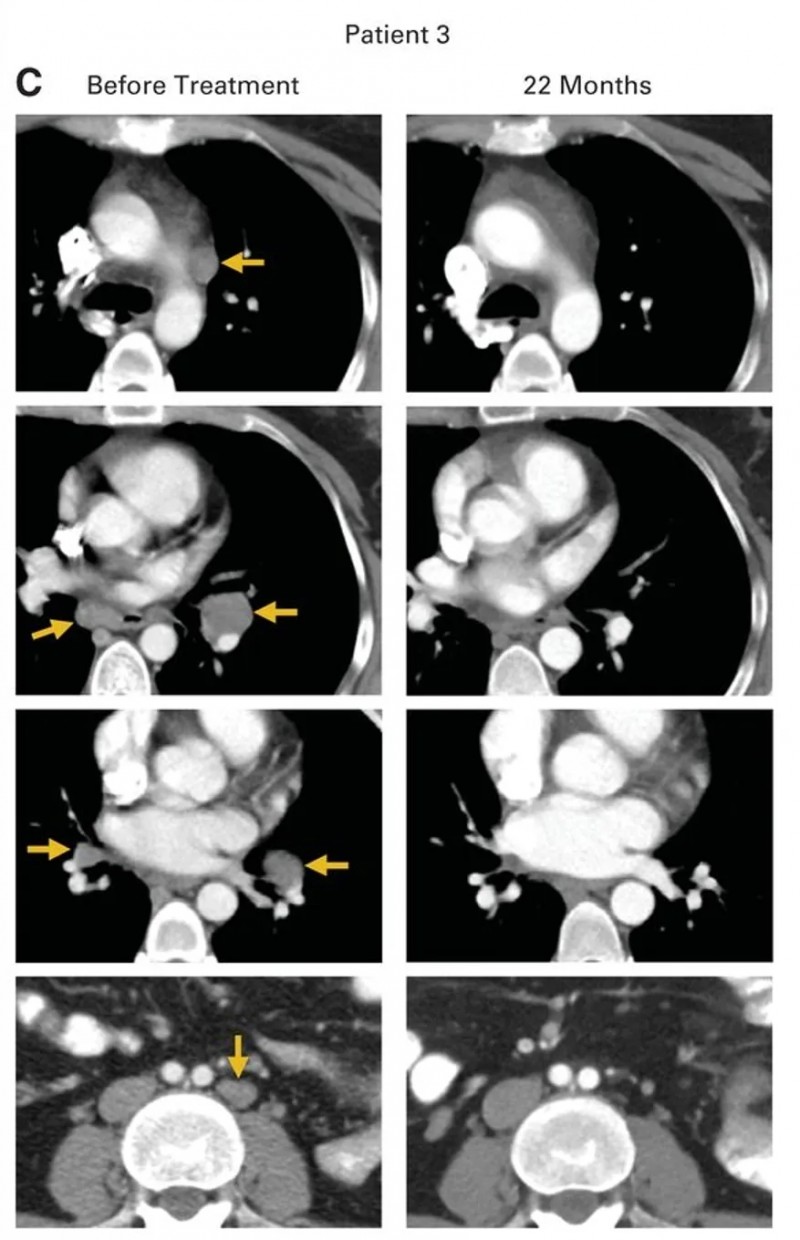
▲图源“JCO”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
患者6
患者6是一位转移性腺癌女性,原发肿瘤对放化疗耐药,挽救性手术发现腹主动脉旁、髂淋巴结及盆腔其他部位受累,后续癌症进展至腹膜后淋巴结、肝脏表面,伴右侧输尿管肾积水及双侧肺栓塞,需放置输尿管支架并抗凝治疗。治疗时腹膜后、腹壁、结肠旁、肝旁及盆腔均有进展性肿瘤,HPV-TIL治疗后获得完全临床缓解(CR,详见下图B、D),治疗后15个月无疾病复发迹象,右侧输尿管肿瘤消退后已取出输尿管支架。
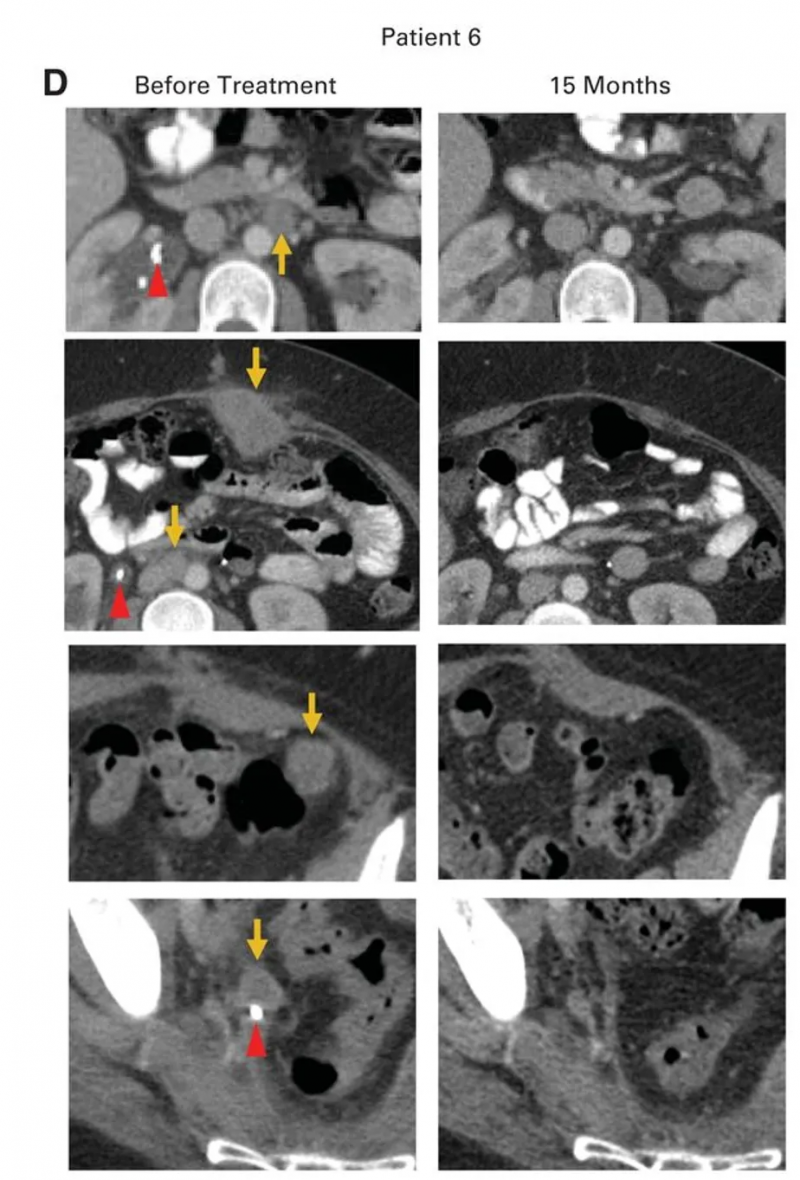
▲图源“JCO”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
综上,单次输注HPV-TILs可使转移性宫颈癌实现持久、完全的肿瘤消退,为这类化疗难治性患者提供了新的治疗方向。
重获新生!TIL联合疗法实现难治性转移性乳腺癌完全持久消退超22个月
《Nature Medicine》报道了一例振奋案例(NCT01174121):一名难治性激素受体(HR)阳性转移性乳腺癌患者,经特异性肿瘤浸润淋巴细胞(TIL)联合治疗后,肿瘤实现完全持久消退,截至报道已持续22个月以上。
本例患者是一位49岁女性,确诊为雌激素受体(ER)阳性、HER2阴性转移性乳腺癌,对多种化疗及内分泌疗法耐药。入组后接受TIL细胞+白细胞介素-2(IL-2)+检查点阻断联合治疗。
结果显示:细胞回输后6周,靶肿瘤负荷减少51%;细胞移植22个月时,所有靶病变及非靶病变均实现放射学完全消退(详见下图)。
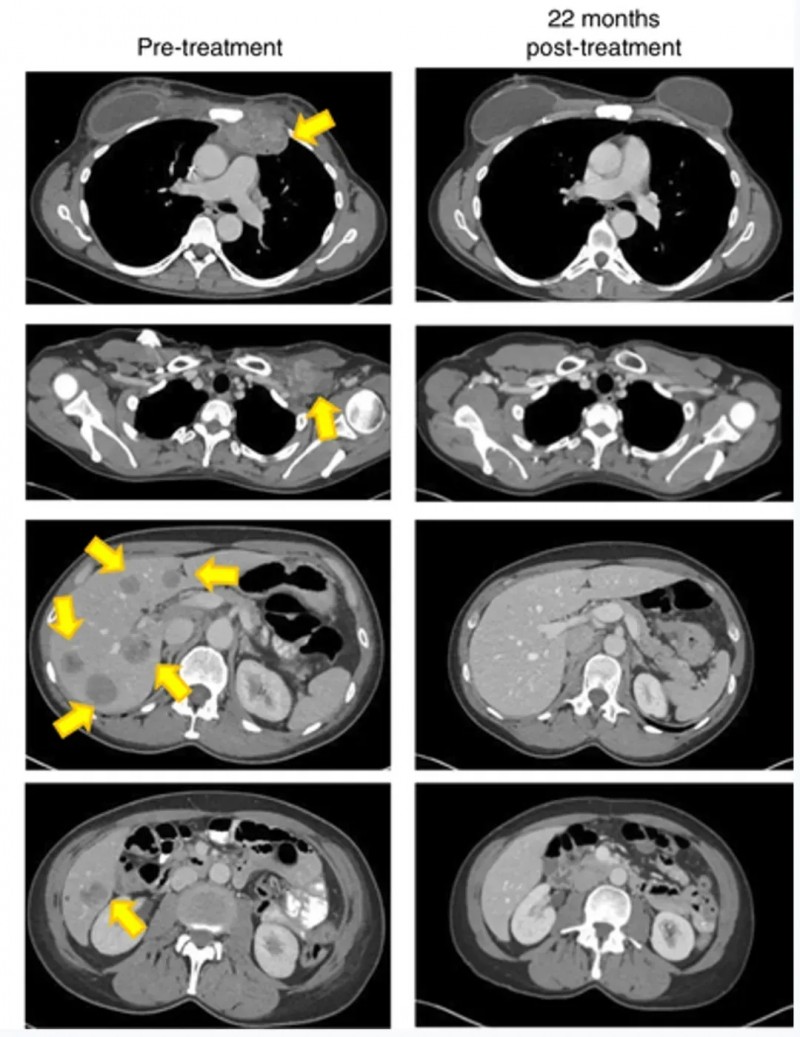
▲图源“Nat Med”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
治疗12周部分缓解率高达81%!全球首个FDA批准黑色素瘤TIL疗法,让肺癌患者疗效持续超2年
Lifileucel是一款个体化一次性肿瘤来源自体T细胞免疫疗法,也是全球首个获FDA批准的黑色素瘤TIL疗法(商品名Amtagvi®)。
《癌症探索》杂志曾报道一则其治疗肺癌的振奋案例:一名41岁IV期粘液性肺腺癌男性患者,携带KRAS G12D突变,肿瘤突变负荷(TMB)为3.3mut/Mb,PD-L1表达0%。接受Lifileucel治疗前,患者既往治疗的反应持续时间仅1.1+个月;治疗6周后,反应持续时间延长至26.2+个月,且疗效随时间加深,输注12周时部分缓解(PR)率达81%(详见下图)。
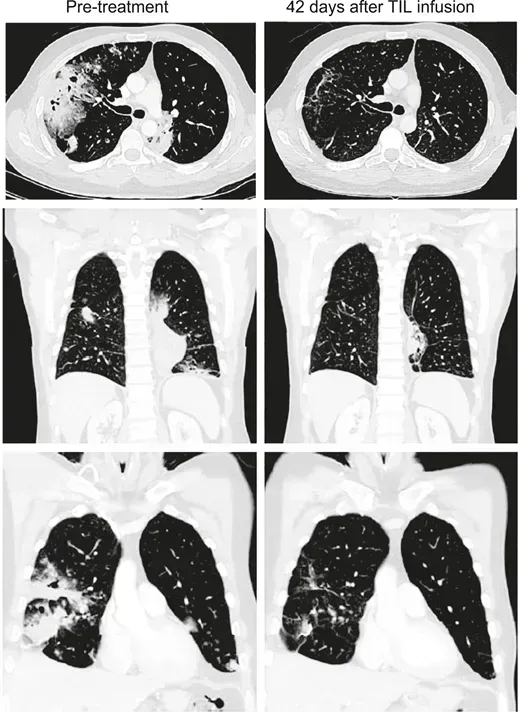
▲图源“Cancer Discov”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
小编寄语
肿瘤浸润淋巴细胞(TIL)疗法自1988年首次应用于临床以来,已走过30余载的发展历程。相较于其他免疫细胞疗法,TIL疗法独具将患者自身肿瘤组织“变废为宝”的神奇功效,堪称实体瘤治疗领域当之无愧的抗癌黑科技。它既适用于早期癌症患者,可有效预防肿瘤的复发与转移;又能作为晚期患者的挽救性治疗手段,为癌症患者带来一线生机。
值得关注的是,TILs细胞数量会随着肿瘤的进展而逐渐减少,并且在术后接受辅助性治疗(如放疗、化疗)时,不仅癌细胞会受到杀伤,体内的免疫细胞也可能受到影响。因此,建议患者务必珍惜这或许仅有一次的宝贵抗癌机会。在术前应积极与主治医师进行沟通,尽可能地保留新鲜的肿瘤标本组织,并联系专业机构对TIL细胞进行分离和冻存,做到未雨绸缪。
想寻求TILs疗法帮助或了解TILs细胞制备或冻存更多信息的患者,可将治疗经历、近期影像学检查及病理报告等资料,提交至医学部,进行初步评估获了解详细的入排标准。
参考资料
[1]Xia T,et al.Autologous Tumor-Infiltrating Lymphocyte Infusion plus Anti-Programmed Cell Death Protein 1 Therapy to Cure Advanced Hepatocellular Carcinoma following Palliative Hepatectomy. Liver Cancer. 2025 Feb 20;14(4):497-505.
https://pmc.ncbi.nlm.nih.gov/articles/PMC12360740/
[2]Stevanović S,et al.Complete regression of metastatic cervical cancer after treatment with human papillomavirus–targeted tumor-infiltrating T cells[J]. Journal of Clinical Oncology, 2015, 33(14): 1543-1550.
https://ascopubs.org/doi/10.1200/JCO.2014.58.9093?url_ver=Z39.88-2003&rfr_id=ori:rid:crossref.org&rfr_dat=cr_pub%20%200pubmed
[3]Zacharakis N,et al.Immune recognition of somatic mutations leading to complete durable regression in metastatic breast cancer. Nat Med. 2018 Jun;24(6):724-730.
https://pmc.ncbi.nlm.nih.gov/articles/PMC6348479/
扫描进患者病友群

肺癌|胃癌|肝癌|结直肠癌|胰腺癌
乳腺癌|脑瘤|淋巴瘤|儿童肿瘤等

相关推荐

癌症治疗本就不应千篇一律,揭秘mRNA癌
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
“不限癌种”新突破,NTRK基因融合的靶
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
肺癌疫苗重大突破,晚期患者多了一个新的选
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

“手术成功”不等于万事大吉,新型癌症疫苗
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

2026年靶向治疗抗癌风暴,突破困境,普
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

2026年这些肺癌疫苗正悄然改变患者的生
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05






![[field:title/]](/uploads/allimg/20200224/1-2002241I5262J.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241I3461D.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H94LK.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241HKW34.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H619327.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H34H52.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H22IH.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241G93O18.jpg)




