癌症疫苗重磅突破!从“通用型”到“私人订制”,这些新技术正在改写患者的结局
癌症疫苗重磅突破!从“通用型”到“私人订制”,这些新技术正在改写患者的结局
一、意外发现,新冠mRNA疫苗竟能增强抗癌疗效
科学探索中常常有意外之喜。2025年《自然》杂志发表的一项研究发现,接种mRNA新冠疫苗的癌症患者,生存时间显著延长。
美国MD安德森癌症中心的研究团队回顾性分析了大量癌症患者数据,发现在接受免疫检查点抑制剂治疗前后100天内接种mRNA疫苗的患者:
- 非小细胞肺癌患者中位生存期从20.6个月延长至37.3个月,三年生存率从30.8%提升至55.7%;
- 黑色素瘤患者三年生存率从44.1%提升到67.6%。
进一步机制研究发现,mRNA疫苗注射后会引发体内1型干扰素的大量产生,激活树突状细胞、巨噬细胞等抗原呈递细胞,它们迁移至淋巴器官,将肿瘤抗原“展示”给T细胞,从而启动针对癌细胞的免疫反应。
这一发现意味着,mRNA疫苗可能作为一种通用的免疫调节剂,为癌症患者提供低成本、易获取的辅助治疗选择。
二、癌症疫苗是如何改变癌症治疗格局的
在过去,癌症治疗往往依赖于“三大法宝”——手术、化疗和放疗。然而,这些传统疗法在杀死癌细胞的同时,也不可避免地损伤健康细胞,导致患者免疫力下降,生活质量大幅降低。更令人担忧的是,许多患者在治疗后仍面临复发和转移的风险。
近年来,癌症疫苗作为一种全新的免疫治疗策略,正悄然改变这一局面。与传统的预防性疫苗不同,治疗性癌症疫苗的目的是“教育”人体的免疫系统,使其能够精准识别并攻击癌细胞,而不伤害正常组织。
这种疗法的核心思路极具创新性——就像是给体内的免疫细胞发放“通缉令”,让它们能够从亿万细胞中准确找出伪装巧妙的癌细胞,进而发起精准打击。
三、癌症疫苗的工作原理
要理解癌症疫苗的独特之处,我们首先需要了解癌细胞是如何逃避免疫系统监视的。
癌细胞非常狡猾,它们虽然源于人体自身细胞,但因基因突变而变得异常;这些异常细胞表面会表达一些特殊的蛋白质(称为肿瘤抗原),本应被免疫系统识别并清除;然而,癌细胞通过各种机制(如表达PD-L1蛋白)给免疫系统“踩刹车”,从而在体内潜伏和生长。
癌症疫苗的作用就是解除这种“刹车”状态,并通过以下机制发挥作用:
1. 抗原呈递:将肿瘤特异性抗原递送给免疫系统,相当于让免疫细胞“记住”癌细胞的特征;
2. 免疫激活:刺激T细胞、B细胞等免疫细胞大量增殖,做好攻击准备;
3. 长效记忆:形成免疫记忆,即使日后出现新的癌细胞,也能快速识别并清除。
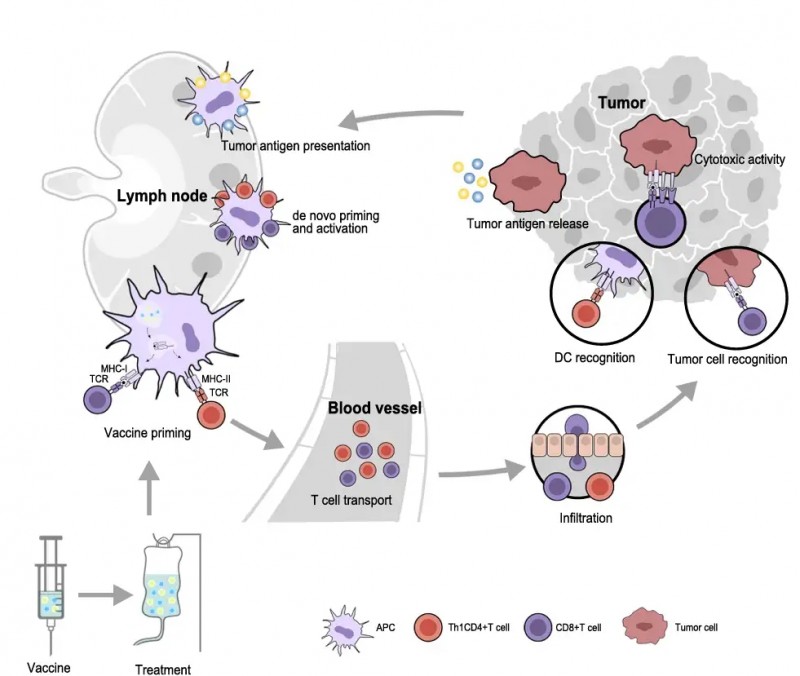
治疗性癌症疫苗的免疫反应机制
目前,科学家已开发出多种类型的癌症疫苗,包括肽疫苗、DNA疫苗、mRNA疫苗、树突状细胞(DC)疫苗等,每种都有其独特优势和应用场景。
四、癌症疫苗应用情况
1. 通用型mRNA疫苗
美国佛罗里达大学科研团队开发的实验性mRNA癌症疫苗,堪称癌症治疗领域的重大突破,这种疫苗采用脂质纳米颗粒作为“快递员”,将编码PD-L1蛋白的基因指令送入人体。
其精妙之处在于:它不仅让免疫系统识别PD-L1这一癌细胞的“身份徽章”,还能促使肿瘤自身表达更多PD-L1,相当于让癌细胞自我暴露。在动物实验中,这款疫苗对传统治疗完全耐药的黑色素瘤表现出彻底清除的效果,在脑癌、皮肤癌和骨癌模型中也单凭疫苗就消灭了肿瘤。
该研究的负责人埃利亚斯·萨尤尔博士激动地表示:“这一步能帮通用癌症疫苗早日上市,以后每个患者的肿瘤,都能被免疫系统精准盯上。”
2. 个体化mRNA疫苗
由默沙东与Moderna合作开发的mRNA-4157是个体化癌症疫苗的杰出代表,这款“私人订制”疫苗根据患者肿瘤的独特突变,编码多达34种专属抗原,激活针对性的免疫反应。
令人振奋的临床数据:在2024年公布的中期研究结果中,与PD-1药物Keytruda联合使用,对高风险黑色素瘤患者而言,三年复发或死亡风险降低了49%,远处转移或死亡风险更是大幅下降62%。这款疫苗已获得美国FDA“突破性治疗”认证和欧洲“优先药物”资格,预计最早2025年就能在一些国家投入使用。
3. 树突状细胞疫苗
日本东京大学研发的WT1树突细胞疫苗采用国际公认的“抗癌明星抗原”——WT1肽抗原,该抗原在75种癌症抗原评选中被评为最佳专利技术,能精准靶向多种实体瘤和血液肿瘤。
这款疫苗的个性化程度极高——先检测患者的HLA(人类白细胞抗原)类型,再将最匹配的WT1肽“装载”入患者自身血液培养的树突状细胞中,制备出完全个性化的疫苗。目前,日本多家机构已开始采用“基因检测+疫苗+PD-1/靶向药”的组合疗法,并积极推进医保临床试验。
4. 非mRNA路线
古巴研发的Cimavax肺癌疫苗为那些基因检测没有突变、无法使用靶向药的患者提供了新选择。它不直接杀死癌细胞,而是“唤醒”人体自身的免疫系统,让免疫系统去遏制肺癌生长。
生存数据说话:对EGF浓度高的晚期肺癌患者,接种疫苗后效果显著——肺鳞癌患者五年生存率达到23%,肺腺癌患者为18.2%,而未接种疫苗的对照组没有一人活过5年。目前该疫苗已用于一线治疗有效的非小细胞肺癌患者,帮助患者延长生存期并提高生活质量。
5. 纳米技术助推的疫苗
近日,斯克利普斯研究所Darrell J. Irvine团队在《自然·纳米技术》上发表综述,系统总结了纳米技术在癌症疫苗领域的最新进展。
纳米技术通过改善抗原递送、开发新型佐剂以及提高疫苗靶向性等方式,显著增强了癌症疫苗的免疫原性和临床疗效。例如:
- 脂质纳米圆盘能够携带肽段抗原和佐剂,通过淋巴引流到达淋巴结,激活T细胞反应;
- 自组装纳米颗粒通过将肽段与TLR7/8激动剂结合,形成微粒,延长了抗原在淋巴结的停留时间;
- 白蛋白偶联疫苗利用白蛋白在组织间液中的运输特性,将抗原递送至淋巴结。
这些技术创新正在解决传统疫苗面临的递送效率低、免疫原性不足等挑战,为癌症疫苗的进一步发展奠定基础。
6. 癌症疫苗联合疗法
2025年欧洲肿瘤内科学会(ESMO)年会上公布的多项研究结果显示,癌症疫苗与免疫检查点抑制剂的联合使用,展现出显著的协同效应。
Cylembio疫苗的III期临床试验显示,与单独使用帕博利珠单抗相比,联合治疗将晚期黑色素瘤患者的中位无进展生存期从11.0个月延长至19.4个月。特别是在PD-L1阴性肿瘤患者中,联合治疗的优势更加明显(16.6个月 vs 3.0个月)。
EVX-01个性化疫苗的II期试验数据显示,与帕博利珠单抗联合治疗晚期黑色素瘤,最佳总体缓解率达到69%,且82%的应答者在末次随访时仍维持缓解,中位缓解持续时间达21个月。
这些研究结果表明,癌症疫苗与现有免疫治疗的组合,有望为更多患者带来持久、有效的疾病控制。
五、中国力量崛起,LK101注射液
在全球癌症疫苗研发竞赛中,中国科学家也交出了亮眼答卷——LK101注射液,这是国内首个获得美国FDA临床试验批准的肿瘤mRNA疫苗,标志着中国肿瘤免疫治疗技术已获国际认可。
LK101是一款基于树突状细胞的“定制疫苗”,通过专利技术将患者肿瘤的专属抗原信息通过mRNA传递给树突状细胞,再由这些细胞“指挥”免疫细胞攻击癌细胞。
首次人体试验结果令人振奋:12名接受疫苗联合消融术的肝癌患者,随访近4年(48.4个月)时全部存活;而未接种疫苗的对照组,已有3名患者离世,随访时间也仅持续了38.8个月。这一数据充分展示了LK101在延长患者生存期方面的巨大潜力。
更令人欣喜的是,这款国产创新疫苗已有渠道让部分患者提前受益。据了解,LK101已在海南博鳌乐城国际医疗旅游先行区落地使用,为国内癌症患者提供了与国际同步的先进治疗选择。博鳌乐城作为中国医疗改革的“试验田”,享有特殊政策,允许使用国内尚未上市的国际创新药物和疗法,为众多晚期癌症患者打开了希望之门。

博鳌乐城国际医疗旅游先行区
值得一提的是,LK101已在海南博鳌乐城国际医疗旅游先行区落地,为符合条件的患者提供了国内接受先进治疗的机会。对于想了解更多癌症疫苗或其他海外新药信息的患者,可以整理好病历资料,提交到医学部,评估一下有没有合适的新药新技术可以使用。
六、癌症疫苗的主要应用场景
随着科研不断深入,癌症疫苗正从概念走向现实,未来可能在以下场景发挥重要作用:
1. 术后辅助治疗:清除残留癌细胞,预防复发;
2. 联合免疫治疗:提高“冷肿瘤”对免疫治疗的反应率;
3. 晚期患者治疗:控制肿瘤生长,延长生存期;
4. 高危人群预防:对具有癌症家族史或癌前病变的人群进行干预。
尽管癌症疫苗研发仍面临个体化制备成本高、大规模临床试验数据不足等挑战,但科学界普遍认为,这方向充满希望。就像20年前mRNA技术还无人看好,如今已成为疫苗研发的重要平台一样,癌症疫苗有望在未来5-10年内彻底改变癌症治疗格局。
七、总结:从“绝症”到“可控”,癌症治疗迎来转折点
回望抗癌之路,人类经历了从束手无策到手术切除,从放疗化疗到靶向治疗,再到如今的免疫治疗和癌症疫苗,每一次突破都让“癌症是绝症”的观念褪色一分。
癌症疫苗的崛起,特别是像LK101这样的国产创新产品的出现,标志着中国在尖端医疗领域已具备与国际并跑的实力。随着更多研究成果从实验室走向临床,我们有理由相信,“谈癌色变”的时代终将过去,癌症将成为一种可以预防、控制甚至治愈的疾病。
对于正在与癌症抗争的患者和家属,重要的是保持信心与希望,积极了解前沿医学进展,在专业医生指导下选择最适合的治疗方案。毕竟,在医学飞速发展的今天,明天永远可能有新希望。
扫描进患者病友群

肺癌|胃癌|肝癌|结直肠癌|胰腺癌
乳腺癌|脑瘤|淋巴瘤|儿童肿瘤等

相关推荐

“手术成功”不等于万事大吉,新型癌症疫苗
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

2026年靶向治疗抗癌风暴,突破困境,普
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

2026年这些肺癌疫苗正悄然改变患者的生
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
新一代NTRK基因融合突变靶向药TL11
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
实现33个月长生存!中国团队成功攻克&q
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

破解术后复发噩梦!NK细胞疗法让晚期胃癌
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05






![[field:title/]](/uploads/allimg/20200224/1-2002241I5262J.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241I3461D.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H94LK.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241HKW34.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H619327.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H34H52.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H22IH.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241G93O18.jpg)




