香港首创CAR-T 14天急速清除癌细胞!六大黄金靶点精准围剿胃癌、胰腺癌、肠癌、肝癌、肺癌等
香港首创CAR-T疗法14天急速清除癌细胞!六大黄金靶点精准围剿胃癌、胰腺癌、肠癌、肝癌、肺癌等
据明报新闻网报道,香港中文大学医学院在先进疗法研究领域取得重要突破。团队去年开展香港首个临床研究,评估本地制造的CAR-T细胞对血癌的治疗效果。目前5名接受治疗的患者中,4人已顺利出院,初步临床数据显示患者体内活跃癌细胞已被清除,让更多癌症患者看到了战胜癌症的曙光!

▲图源“mingpao”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
香港CAR-T突破年龄与时效双重壁垒:将治疗周期砍半,60岁患者也能"追"上治愈机会
研究证实,本土制造的CAR-T细胞对复发性及难治性血液肿瘤疗效明确。团队计划进一步拓展适应症,针对实体肿瘤及红斑狼疮等免疫疾病开发新型CAR-T产品。相比传统治疗模式,此次研发的CAR-T细胞疗法呈现两大技术优势:
1、制备周期大幅缩短:以往细胞需送海外处理,全程需4至6周;而中大实验室仅用12天完成细胞制造,从血液分离到回输患者体内仅需14天,显著提升治疗时效性。
2、适应症范围拓宽:突破传统疗法对25岁以下患者的年龄限制,将适用年龄上限放宽至60岁,且可用于急性白血病首次注射等临床场景。
作为血癌治疗的新兴技术,细胞疗法通过基因编辑增强免疫细胞识别与清除癌细胞的能力,使其在体内持续发挥抗癌作用,为实现疾病长期缓解甚至根治开辟了新路径。
01、CAR-T细胞疗法的四大突破性优势
1.机制革新:不依赖化学物质或放射线,而是利用患者自身免疫细胞的天然抗癌能力。
2.精准靶向:通过 CAR 受体特异性识别癌细胞表面抗原,专门针对癌细胞,避免伤害正常组织,从而显著降低传统疗法的毒副作用。
3.长效缓解:一次注射后,部分患者即可达到长期缓解,无需反复化疗或放疗,大幅提升生活质量。
4.持续免疫监视:改造后的T细胞可在体内存活数月至数年,形成 “抗癌记忆”,持续抵御肿瘤复发,这是传统放化疗无法实现的优势。
02、CAR-T相较于传统放化疗的优缺点比较(详见下表)
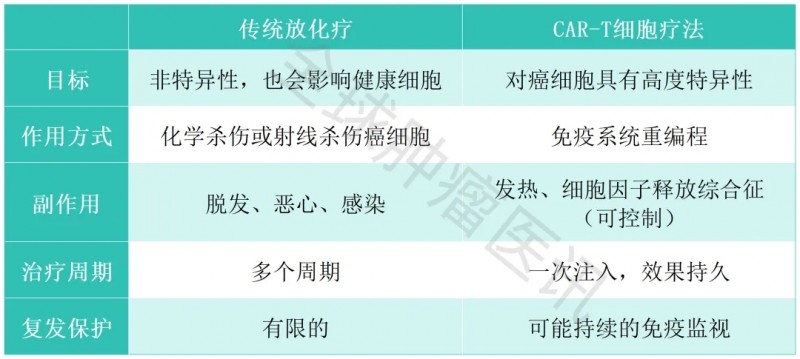
CAR-T细胞疗法的黄金靶点
01、CLDN18.2:胃癌/胰腺癌等
CLDN18.2(Claudin18.2)作为一种紧密连接蛋白,在胃癌、胃食管连接部癌中呈中至高度表达,已成为该领域极具潜力的治疗靶点。此外,它在胰腺癌、胃食管结合部腺癌(GEJ)、食管癌、结肠癌、乳腺癌、肝癌、卵巢癌、非小细胞肺癌等某些恶性肿瘤中也普遍表达。
1.中国自研CLDN18.2 CAR-T,让胃癌生存期提升30%
舒瑞基奥仑赛注射液(satri-cel,CT041)作为全球首个针对实体瘤的自体CLDN18.2 CAR-T细胞疗法,在2025年ASCO大会上公布的1期临床试验数据引发关注。该研究纳入156例胃癌患者,包括136例胃腺癌与20例胃食管连接部腺癌。
结果显示:satri-cel组客观缓解率(ORR)达22%(23/104,95%CI 15–31),较对照组4%(2/52,95%CI 0–13)提升5.5倍;疾病控制率为63%(95%CI 52–72),显著高于对照组的25%(95%CI14–39)。中位总生存期(OS)方面,satri-cel组为7.92个月(95%CI 5.78–10.02),较对照组5.49个月(95%CI3.94–6.93)提升超30%。
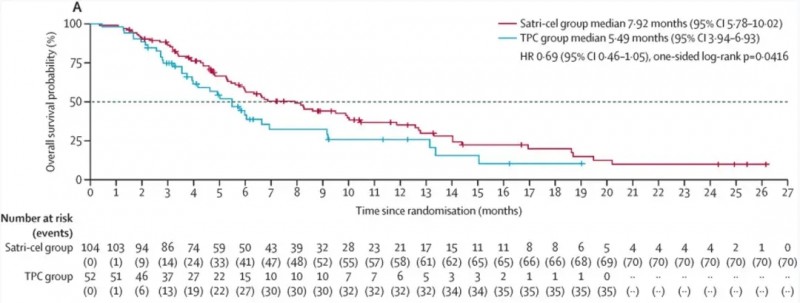
▲图源“The Lancet”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
值得关注的是,研究中一例患者在输注satri-cel后第2周出现肝脏病灶暂时性增大,但随访至第26周时病灶已缩小至基线水平以下,提示CAR-T疗法可能存在延迟起效的动态响应特征。这一数据为CLDN18.2靶点在实体瘤治疗中的应用提供了重要临床证据。
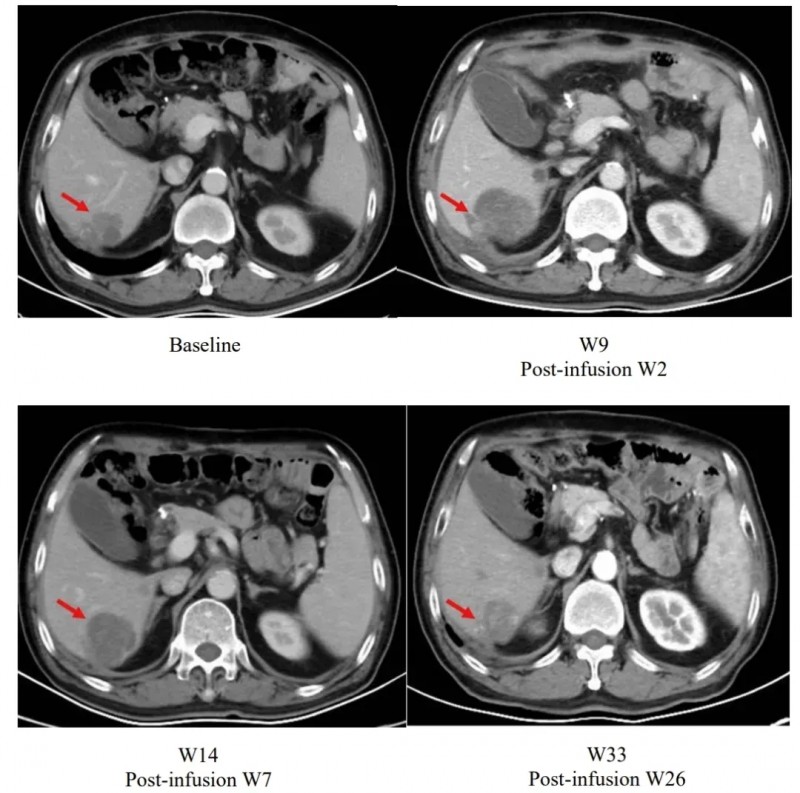
▲图源“The Lancet”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
2.CLDN18.2 CAR-T助多线治疗失败的胰腺癌患者,达完全缓解
Claudin18.2 CAR-T除了治疗胃癌外,还可用于胰腺癌的治疗。《免疫前沿》杂志报道了一名晚期多线治疗失败且肿瘤广泛转移的胰腺癌患者,在接受该疗法治疗后,奇迹般获得完全缓解的突破性案例。
该患者是一位72岁男性,确诊Ⅲ期胰腺导管腺癌(pT2N2M0,Ⅲ期),曾接受国胰十二指肠切除术、吉西他滨联合卡培他滨辅助化疗、FOLFIRINOX方案等等多线治疗,但病情仍持续进展,并出现肝/腹膜转移、颈部淋巴结转移等,后因严重不良反应被迫终止治疗。遂入组入组 Claudin18.2 CAR-T 疗法临床试验(NCT05620732),接受单次细胞输注。
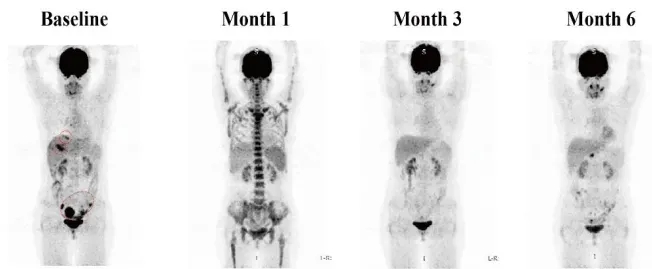
结果显示:患者在CAR-T细胞输注1个月后即达到完全缓解(CR),肿瘤标志物CA19-9从1100U/mL显著降至25.85U/mL,恢复到正常范围(详见下图),且CA19-9在治疗5个月后仍保持正常水平。此外,PET-CT扫描显示颈部淋巴结、肺部及其他转移病灶完全消失,且CAR-T细胞治疗后8个月,颈部及肺部病灶未复发(详见下图)。
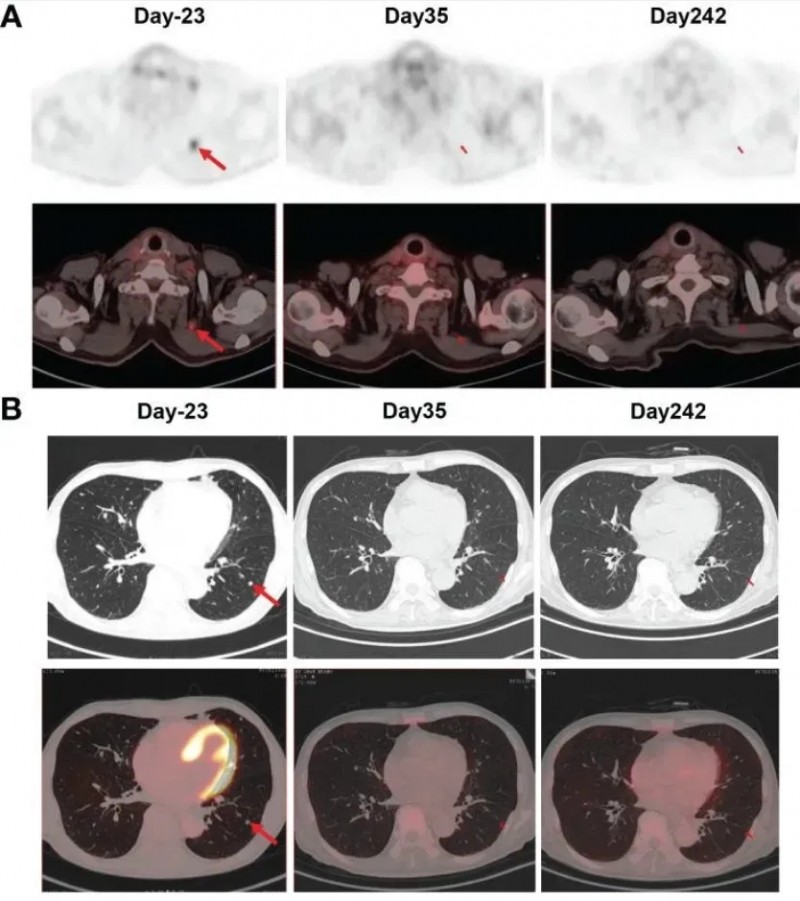
▲图源“Front Immunol”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
02、CEA:结直肠癌、胃癌、非小细胞肺癌、胆管癌
癌胚抗原(CEA)作为胃肠道癌症的高敏感性标志物,在结直肠癌(CRC)组织及患者血清中广泛表达,因其特异性成为CAR-T疗法的理想靶点。
1.中国自研CEA CAR-T让70%结直肠癌患者病情稳定,一例肿瘤30周"零进展"
我国一项针对CEA阳性结直肠癌(CRC)患者的I期临床试验(NCT02349724)显示,CEA CAR-T细胞疗法对伴肝肺转移的难治性患者具有疾病控制潜力。该研究纳入10例既往治疗中均出现疾病进展(PD)的患者,接受静脉输注CEACAR-T细胞治疗。
结果显示:10例患者经CAR-T治疗后,7例(70%)达到病情稳定(SD),肿瘤直径呈可控性变化。其中2例患者(Ps3、Ps5)病情持续稳定超30周。值得关注的是,患者P10接受DL4剂量治疗后,MRI影像学证实肝内单个转移病灶体积缩小,直接体现了CAR-T疗法对实体瘤的局部控制能力。
▼P10患者在CAR-T输注前(左图)和4周后(右图)的MRI评估
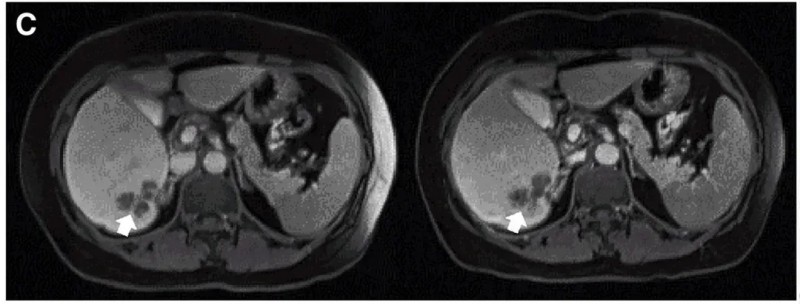
▲图源“Molecular Therapy”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
2.CEA CAR-T腹腔注射,让结直肠癌、胃癌、非小细胞肺癌、胆管癌等多癌种,DCR飙升至88%
2024年ASCO大会公布的CEA CAR-T疗法I期临床试验(NCT05396300)首次突破单一癌种限制,纳入35例结直肠癌及胃癌、非小细胞肺癌、胆管癌患者,通过腹腔注射(IP)的创新给药方式实现实体瘤治疗策略革新。该研究采用“CAR-T细胞直接靶向肿瘤微环境”的给药思路,突破传统静脉输注(IV)的局限性,既增强对实体瘤的局部杀伤能力,又可建立持久免疫监视,降低脱靶毒性风险。
结果显示,腹腔注射组客观缓解率(ORR)为25%,疾病控制率(DCR)达88%。其中高剂量腹腔注射亚组ORR提升至28.5%,且缓解患者的肿瘤持续控制时间均超5个月,其中1例患者在6个月随访时肿瘤病灶缩小76%。相比之下,静脉输注组ORR为8%,DCR为67%。
做了基因检测的病友可以拿出报告看看,一旦存在EGFR突变,可联系医学部,初步评估是否有机会接受国内新药治疗,看不懂的病友也可致电医学部解读报告。
03、GPC3:肝癌黄金靶点+跨界肺鳞癌
GPC3(磷脂酰肌醇蛋白聚糖-3)是一种硫酸肝素蛋白聚糖,参与调控细胞迁移、增殖与存活,它在72%的晚期肝细胞癌(HCC)组织中呈高表达,且与患者术后转移显著相关。但GPC3在正常肝脏、肝硬化肝脏或良性病变(如发育不良结节、肝腺瘤)组织中均无表达。这一特性使GPC3成为精准打击肝癌细胞的“黄金”靶标,既能精准识别癌细胞,又避免损伤健康肝组织。
1.GPC3 CAR-T精准爆破晚期肝癌,疾病控制率高达90.9%,病灶显著缩小44%
2024 ASCO大会上,公布了一款靶向GPC3的自体CAR-T疗法——C-CAR031首次人体临床研究(IIT)的强劲疗效数据。该研究共纳入24例晚期肝细胞癌(HCC)患者(83.3%伴肝外转移),入组接受4个剂量水平(DL)的C-CAR031输注。
结果显示:全部入组患者的疾病控制率(DCR)高达90.9%,客观缓解率(ORR)达50.0%(详见下图)。在22例可评估疗效的患者中,90.9%出现肿瘤缩小,肝内及肝外病灶中位缩小率达44.0%(范围为3.4%-94.4%)。中位无进展生存期(PFS)为4.27个月(95%CI,2.86-8.90)。
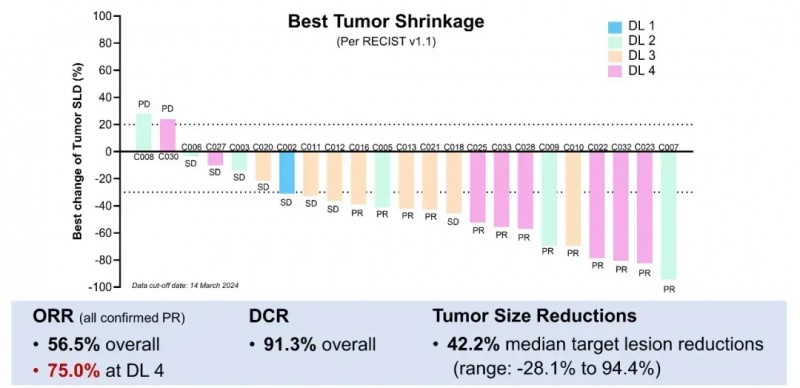
▲图源“ASCO”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
其中C023号患者(DL4剂量组)接受治疗后呈现持续肿瘤退缩:治疗1.5个月时,肺部转移病灶即出现深度应答,影像学检查显示肿瘤显著缩小,凸显了该疗法对肝外转移灶的控制能力与临床转化价值。
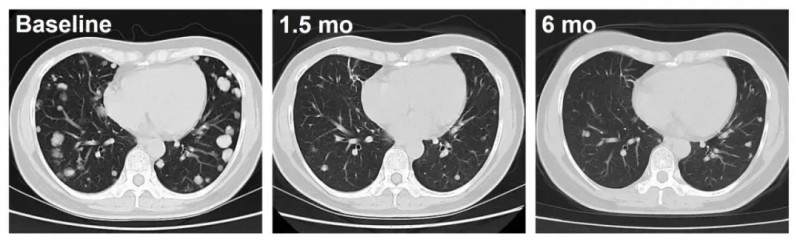
▲图源“ASCO”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
2.全球首个GPC3 CAR-T完成肺鳞癌首例回输,为肺癌免疫开辟"新赛道"
除肝癌治疗外,全球首个靶向GPC3的自体CAR-T疗法C-CAR031在肺癌领域取得突破性进展。2025年4月13日,由上海市肺部肿瘤临床医学中心发起的晚期肺鳞状细胞癌临床研究中,首例患者成功完成C-CAR031细胞回输。
这是全球首个针对GPC3靶点的肺鳞癌CAR-T疗法临床探索,标志着该疗法在实体瘤跨癌种应用中迈出关键一步,为肺癌免疫治疗,带来了全新希望!
04、GUCY2C/GCC:肠癌
鸟苷三磷酸化酶(GUCY2C,GCC)在胃肠道的液体和离子稳态中起关键作用,约80%的结直肠癌患者肿瘤中GCC表达阳性,被认为是能够精准打击肠癌细胞的“黄金”靶标!基于此,研究人员开发针对GCC的CAR-T细胞疗法GCC19CART。
《JAMA肿瘤学》发表的一项最新临床研究,为晚期肠癌患者点燃了新希望。结果显示客观缓解率(ORR)达40%,中位总生存期(OS)为22.8个月;高剂量组的中位无进展生存期(PFS)为6.0个月。
下图显示了一位代表性患者,在接受GCC19CART治疗后,达到部分缓解(PR),腹部及盆腔目标病灶显著缩小。
05、中美已获批的CAR-T疗法及其对应靶点:CD19/BCMA
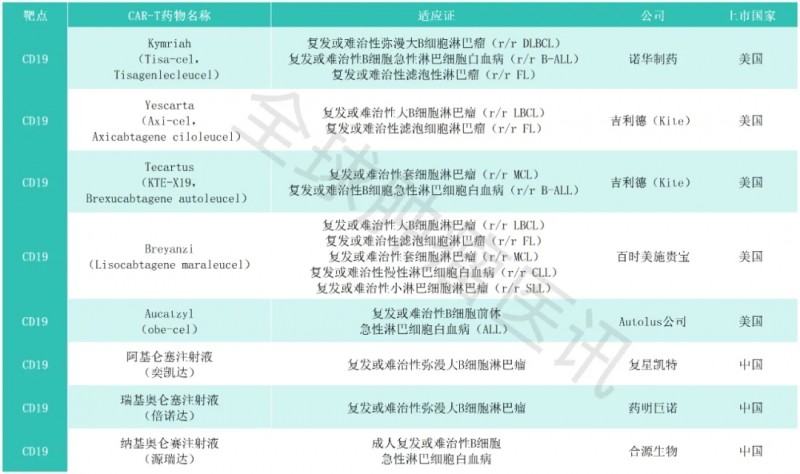
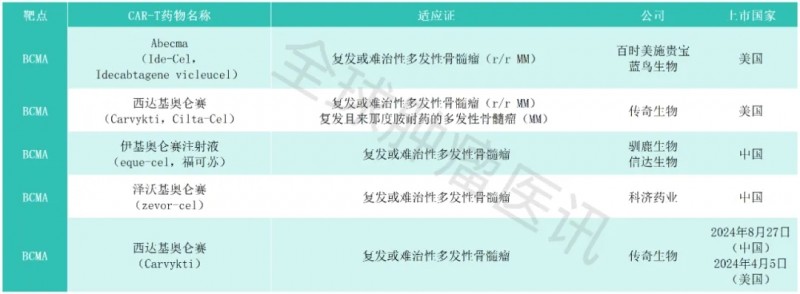
06、CAR-T疗法其他潜在治疗靶点
1.MUC-1:用于肝癌、肺癌、胰腺癌、结肠癌、胃癌等的治疗。
2.间皮素(mesothelin):用于间皮瘤、胰腺癌、卵巢癌、肺癌等的治疗。
3.PSMA:用于前列腺癌等。
4.EGFRvII:用于治疗神经胶质瘤、头颈部肿瘤。
5.B7-H3:用于治疗尤文肉瘤、横纹肌肉瘤、肾母细胞瘤、神经母细胞瘤和髓母细胞瘤以及特别难以治疗的脑干肿瘤(DIPG)。
小编寄语
时至今日,CAR-T 细胞疗法在血液系统恶性肿瘤的治疗领域已取得突破性进展,众多患者从中受益。令人欣慰的是,近年来全球的研究人员从未停止探索的脚步,持续钻研各种新型策略,致力于降低肿瘤抗原异质性,打破免疫抑制的困境,为癌症患者带来更多希望!
医学部小编也期望随着越来越多明星靶点的涌现、技术的不断革新,CAR-T疗法可以早日突破价格和癌症治疗的瓶颈,造福更多的癌症晚期患者,实现长期带瘤生存、提高生存质量、降低复发风险的美好愿景!想寻求CAR-T、TCR-T、TIL疗法等国内外抗癌新技术帮助的患者,可将病理检查报告、治疗经历、近期影像学检查等资料汇总后,提交至医学部,进行初步评估,或申请国内外抗癌专家会诊。
参考资料
[1]Zhong G,et al.Complete remission of advanced pancreatic cancer induced by claudin18.2-targeted CAR-T cell therapy: a case report. Front Immunol. 2024 Feb 29;15:1325860.
https://pmc.ncbi.nlm.nih.gov/articles/PMC10937427/
[2]Qi C,et al.Claudin-18 isoform 2-specific CAR T-cell therapy (satri-cel) versus treatment of physician's choice for previously treated advanced gastric or gastro-oesophageal junction cancer (CT041-ST-01): a randomised, open-label, phase 2 trial[J]. The Lancet, 2025.
https://www.thelancet.com/journals/lancet/article/PIIS0140-6736(25)00860-8/fulltext
[3]Zhang Q,et al.Phase I study of C-CAR031, a GPC3-specific TGFβRIIDN armored autologous CAR-T, in patients with advanced hepatocellular carcinoma (HCC)[J]. 2024.
https://meetings.asco.org/abstracts presentations/234377
[4]https://news.mingpao.com/pns/%E6%B8%AF%E8%81%9E/article/20250303/s00002/1740938094152
扫描进患者病友群

肺癌|胃癌|肝癌|结直肠癌|胰腺癌
乳腺癌|脑瘤|淋巴瘤|儿童肿瘤等

相关推荐

癌症治疗本就不应千篇一律,揭秘mRNA癌
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
“不限癌种”新突破,NTRK基因融合的靶
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
肺癌疫苗重大突破,晚期患者多了一个新的选
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

“手术成功”不等于万事大吉,新型癌症疫苗
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

2026年靶向治疗抗癌风暴,突破困境,普
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

2026年这些肺癌疫苗正悄然改变患者的生
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05






![[field:title/]](/uploads/allimg/20200224/1-2002241I5262J.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241I3461D.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H94LK.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241HKW34.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H619327.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H34H52.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H22IH.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241G93O18.jpg)




