“不限癌种”新突破,NTRK基因融合的靶向药TL118带来哪些新曙光
“不限癌种”新突破,NTRK基因融合的靶向药TL118带来哪些新曙光
长期以来,我们治疗癌症的传统思维是“按器官治病”——肺癌用肺癌的化疗药,肠癌用肠癌的方案。这种治疗模式虽然挽救了许多生命,但当疾病进展到晚期,或者遭遇传统治疗耐药时,患者往往面临无药可用的绝境。然而,随着精准医疗时代的到来,一种被称为“不限癌种(Tumor-Agnostic)”的全新治疗理念正在彻底颠覆我们的认知。今天,我就带大家深入了解这一领域的“明星靶点”——NTRK基因融合,以及在临床研究中大放异彩的国产新一代靶向药物:TL118。
一、 什么是NTRK基因融合?“不限癌种”的奇迹是如何发生的
要讲清楚TL118这款药,我们必须先弄明白它的“靶子”是什么。
在我们的身体里,有一组名为NTRK(神经营养因子受体激酶)的基因家族,包含了NTRK1、NTRK2和NTRK3。在正常情况下,它们就像是人体神经系统发育的“基建工程师”,非常守规矩。但是,在某些复杂的生物学因素影响下,癌细胞内的染色体发生了断裂和错误的重新拼接。这就好比两条原本平行的铁路发生了错位连接,NTRK基因与其他原本不相干的基因“融合”在了一起。
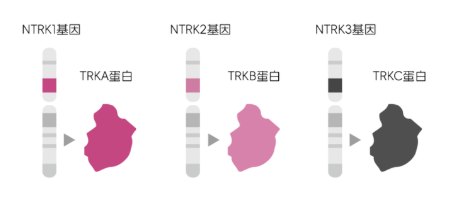
这种“基因融合”会导致异常的TRK蛋白被源源不断地制造出来。打个通俗的比方:如果把细胞的生长分裂比作一辆汽车,正常情况下是由油门和刹车共同控制的;而NTRK基因融合,就像是一块沉重的石头死死卡在了汽车的油门踏板上。细胞接收到了不受控制的“疯狂生长”信号,最终演变成了恶性肿瘤。
令人惊叹的是,这种“卡油门”的现象并不局限于某一种特定的器官。目前的研究发现,NTRK基因融合存在于数十种不同的成人和儿童实体瘤中,包括但不限于非小细胞肺癌、结直肠癌、甲状腺癌、乳腺癌、软组织肉瘤,甚至在一些罕见肿瘤(如婴儿纤维肉瘤、分泌型乳腺癌)中发生率极高。
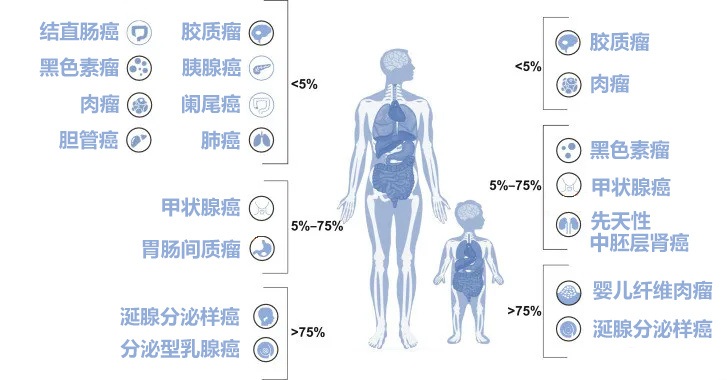
既然它们都是因为同一个“油门故障”引起的,那我们是不是只要找到能松开这个油门的“扳手”,就能跨越器官的界限,实现“异病同治”?答案是肯定的。这就是NTRK靶向药诞生的核心逻辑。
二、 初露锋芒:全面认识国产创新抗癌药TL118
目前,全球范围内已经有拉罗替尼(Larotrectinib)和恩曲替尼(Entrectinib)等第一代TRK抑制剂获批上市,并取得了令人瞩目的疗效。然而,狡猾的癌细胞绝不会轻易认输。在接受第一代靶向药治疗一段时间后(通常是一到两年),部分患者的肿瘤会发生新的基因突变(例如TRKA G595R或TRKC G623R突变)。这就好比原本的“锁”生锈变形了,第一代药物这把“钥匙”再也打不开它,导致病情再次恶化。这就是医学上令人头疼的“获得性耐药”。
面对这一临床痛点,由我国生物科技公司自主研发的新一代NTRK激酶抑制剂——TL118,应运而生。
与第一代药物相比,TL118的分子结构经过了更为精妙的特殊设计。它不仅能够强效抑制那些原本就存在NTRK融合的肿瘤细胞,更重要的是,它被赋予了“克服耐药突变”的强大使命。在临床前的细胞实验中,TL118展现出了极高的针对耐药性突变的抑制活性。它就像是一把能够自动适应锁孔变化的“万能钥匙”,致力于打破第一代靶向药耐药后的治疗僵局,为陷入绝境的患者重新撕开一道生命的裂缝。
三、 数据说话:TL118的临床研究与疗效印证
在医学界,任何天花乱坠的理论都必须经过严谨的临床数据检验。TL118目前的临床进展究竟如何?这是患者最关心的问题。
早在开展初期,TL118就启动了针对NTRK基因融合的晚期恶性实体瘤患者的剂量递增、开放的Ⅰ期临床试验。根据公布的临床研究数据显示:截至2022年6月30日,该研究共入组了30名患者接受TL118治疗,并且已顺利完成方案中设定的全部8个剂量组的爬坡试验。
最令人振奋的是,在这8个剂量组的逐渐增加过程中,并未观察到最高剂量限制性毒性(DLT)!这意味着什么?这意味着TL118具有非常良好的安全性和耐受性,药物在体内的安全窗口足够宽,患者在接受治疗时遭受严重毒副作用的风险较低,生活质量能够得到有效保障。
目前,TL118治疗NTRK融合基因阳性肿瘤患者的Ⅱ期临床研究(研究登记号:CTR20210067)也在如火如荼地进行中,旨在进一步大规模确证其抗肿瘤的临床有效性。
不仅如此,TL118的潜力不仅局限于成人肿瘤。众所周知,儿童恶性实体瘤的治疗药物极度匮乏,药物研发难度极大。但就在近期,国家药监局药审中心(CDE)公示了“儿童抗肿瘤药物研发鼓励试点计划(星光计划)”,TL118颗粒成功被纳入该星光计划的试点项目。这不仅是对TL118前期安全性和疗效潜力的国家级权威认可,更是为饱受罕见肿瘤折磨的患儿家庭点亮了新的希望。
四、 哪些患者能从TL118中获益?如何寻找这条“生命线索”
看到这里,很多患者可能会问:“这药这么好,我们能不能马上用?”
请大家先冷静下来。靶向治疗的精髓在于“精准”,没有靶点,千万不要盲目吃药。TL118的作用前提是患者体内必须确实存在“NTRK基因融合”。
那么,如何才能知道自己是否带有这个“幸运”的靶点呢?答案是通过二代测序技术(NGS)。
我经常强调:“如果不做全面的基因检测,就像是蒙着眼睛打仗。”传统的基因检测往往只查几个常见的突变(如肺癌的EGFR、ALK),而NTRK融合发生率在常见肿瘤中相对较低(不足1%),极容易被漏诊。只有通过包含几百个基因的NGS大Panel检测(最好包含RNA测序,因为RNA测序对“基因融合”的检出率更高),才能精准捕获这条隐藏的生命线索。
以下三类人群,我强烈建议进行NTRK基因融合的全面筛查:
1、标准治疗(手术、化疗、放疗等)均已失败,或者无法耐受传统治疗的晚期局部或转移性实体瘤患者;
2、患有某些罕见肿瘤(如分泌型乳腺癌、婴儿纤维肉瘤、先天性中胚层肾瘤等),这类肿瘤NTRK融合概率极高;
3、之前使用过第一代TRK抑制剂(如拉罗替尼、恩曲替尼)且出现耐药进展的患者,这部分患者正是TL118这款新一代药物重点攻克的对象。
五、 不放弃,就永远有希望
在对抗癌症这条充满荆棘的道路上,医学的每一次微小进步,都是无数患者重获新生的基石。从化疗时代的“狂轰滥炸”,到靶向时代的“精确制导”,再到如今如TL118这般“跨越癌种、克服耐药”的新一代利器,科学正在以超乎想象的速度改变着癌症的结局。
癌症不再是绝对的不治之症,它正逐渐变成一种可以通过药物长期控制的“慢性病”。我想对所有正在黑暗中摸索的病友和家属说:请不要轻易被一纸诊断书判处死刑。如果你身边有人正面临肿瘤治疗的瓶颈,可以整理好病例资料,提交到医学部,进行初步评估。
扫描进患者病友群

肺癌|胃癌|肝癌|结直肠癌|胰腺癌
乳腺癌|脑瘤|淋巴瘤|儿童肿瘤等

相关推荐

“不限癌种”新突破,NTRK基因融合的靶
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
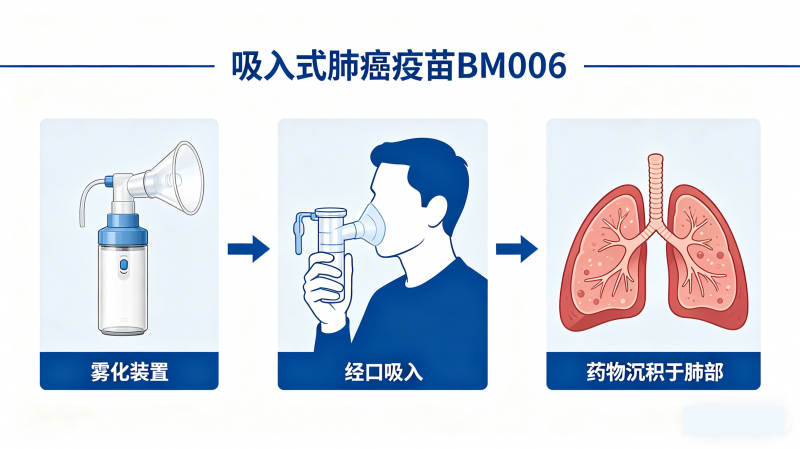
肺癌疫苗重大突破,晚期患者多了一个新的选
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

“手术成功”不等于万事大吉,新型癌症疫苗
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

2026年靶向治疗抗癌风暴,突破困境,普
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

2026年这些肺癌疫苗正悄然改变患者的生
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
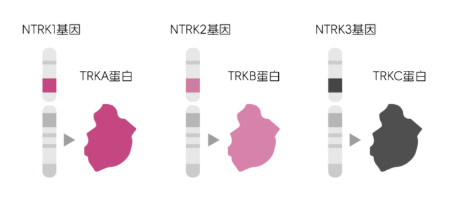
新一代NTRK基因融合突变靶向药TL11
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05






![[field:title/]](/uploads/allimg/20200224/1-2002241I5262J.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241I3461D.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H94LK.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241HKW34.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H619327.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H34H52.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H22IH.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241G93O18.jpg)




