生存期屡破3年大关!中美846项癌症疫苗获批临床,打一针阻断20多款癌种?
中美两国共846个癌症疫苗项目获批临床,生存期屡破3年大关!打一针阻断20多款癌种?
19世纪末,美国医生William B.Coley观察到一个奇特现象:部分癌症患者在感染丹毒后,体内肿瘤竟出现消退迹象。受此启发,他尝试将大肠杆菌毒素等细菌混合物配制成治疗剂,为癌症患者开启了"注射疗法"的新可能——这一突破性尝试,正式拉开了癌症疫苗研究的历史序幕。
时光流转至21世纪,癌症疫苗领域迎来爆发式发展。2014至2024年短短十年间,中美两国共开展了846项癌症疫苗临床试验(中国89项、美国757项),研究范围覆盖肺癌、宫颈癌、胰腺癌、乳腺癌、淋巴瘤、胶质母细胞瘤等20余种癌症类型。
从实验室里的细菌毒素探索,到如今mRNA疫苗、DC疫苗、古巴肺癌疫苗等创新成果的涌现。如今的癌症疫苗研究,已从零星探索迈向系统性攻坚,每一项临床试验的数据突破,每一针疫苗注入人体的瞬间,都在攻克癌症的进程中再进一步,为更多无药可用或想预防癌症复发/转移的患者,带来了新的希望与选择!
关于癌症疫苗你想知道的那些事儿
癌症疫苗是一类通过激活人体免疫系统来预防或治疗癌症的生物制品,其核心功效是针对已存在的肿瘤细胞,通过激活机体免疫系统识别并杀伤癌细胞,主要用于术后辅助治疗或晚期癌症的联合治疗,达到延缓肿瘤进展、降低肿瘤复发/转移风险、延长生存期等目的,根据其作用机制可分为预防性癌症疫苗和治疗性癌症疫苗。
癌症疫苗的关键里程碑
①2006年,美国食品和药物管理局(FDA)批准了首个用于预防宫颈癌的HPV疫苗。
②2010年,世界上第一个获批的治疗性癌症疫苗——Provenge,获得美国食品药品监督管理局(FDA)的批准。
③2021年,用于治疗黑色素瘤患者的Neovax新型抗原疫苗,可有效控制对肿瘤生长的免疫反应长达四年。
④2023年,德国和美国联合开展的小分子mRNA胰腺癌疫苗试验取得了积极成果,展示了个性化癌症疫苗的可行性和潜力。
⑤2023年,中国首个mRNA肿瘤抗原疫苗——XH101注射液的临床试验申请(IND),获得国家药品监督管理局(NMPA)药品审评中心受理。
⑥2024年,英国国家医疗服务体系(NHS)启动了一项开创性的大规模个性化癌症疫苗临床研究,这是全球首个此类大规模临床试验,有望提高癌症患者的存活率和生活质量。
⑦2024年,美国Geneos Therapeutics公司研究表明,癌症疫苗Gnos-PV02联合PD-1抑制剂,在晚期肝细胞癌患者中取得了令人鼓舞的疗效和良好的安全性。
这些里程碑事件不仅展现了癌症疫苗的巨大潜力,也为未来医学发展提供了新的方向。
治疗性癌症疫苗有哪些?各自的优缺点
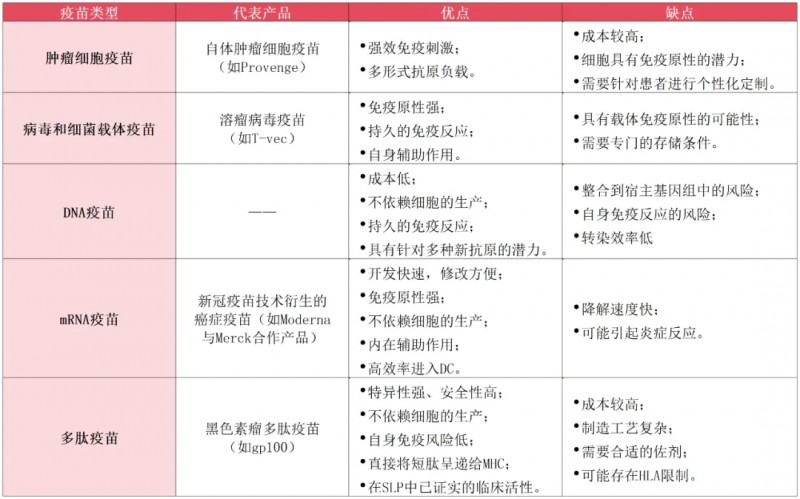
▲数据源自“Signal Transduct Target Ther”,医学部整理汇总
中美846项癌症疫苗试验,攻坚20多款癌种,为千万患者编织生命防护网
根据中国国家药品监督管理局(NMPA)药品审评中心、美国FDA及ClinicalTrials.gov公开数据,2014—2024年中美两国癌症疫苗临床试验呈现显著差异:中国注册89项(占本国药物临床试验总数的0.3%),美国注册757项(占本国药物临床试验总数的0.02%)。
从试验阶段看,中国I期(28.1%)和II期(15.7%)试验占比低于美国的52.1%和36.3%,而III期(40.5%)及IV期(15.7%)试验占比显著高于美国的7.9%和3.7%。
癌症类型覆盖方面,中国试验聚焦5大类型,其中HPV相关癌症占比高达93.3%(83例),其余为肺癌(3例,3.4%)、淋巴瘤(1例,1.1%)、实体瘤(1例,1.1%)、胶质母细胞瘤(1例,1.1%)。
美国则涉及20余种癌症,前五位为乳腺癌(73例,9.6%)、宫颈癌(62例,8.2%)、肺癌(62例,8.2%)、黑色素瘤(45例,5.9%)、胰腺癌(41例,5.4%),研究覆盖范围更为广泛。
▼2014-2024年间,中国和美国新疫苗试验的前20类癌种
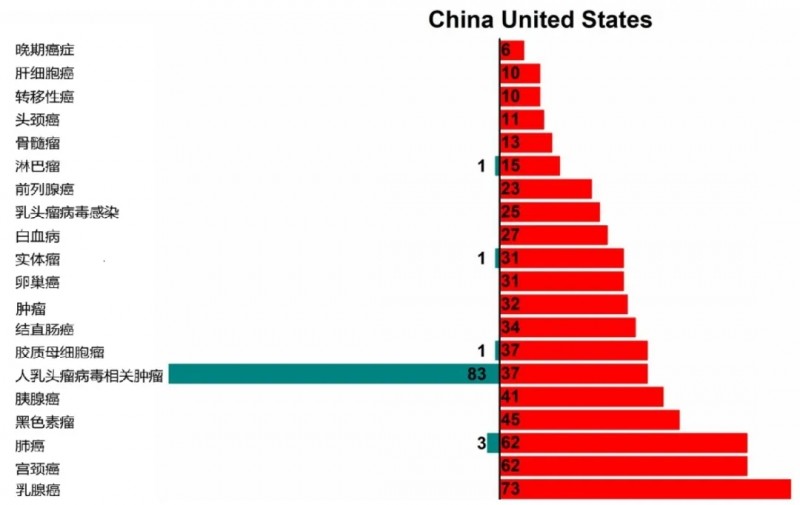
▲图源“frontiers”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
中国患者如何寻求癌症疫苗帮助
目前,癌症疫苗中疗效及预防复发效果较为突出的是树突状细胞疫苗、mRNA疫苗、古巴肺癌疫苗、个性化新抗原疫苗等,在德国、日本也有树突状细胞疫苗用于临床辅助治疗多种癌症,如肺癌、肾癌、肝癌、乳腺癌、皮肤癌等,是癌症患者治疗的新希望。
想参加上述临床试验的患者,可将近期病理报告、出院小结、治疗经历、影像学或血液检查等资料,提交至医学部,进行详细评估。
标准治疗失效不是终点!BNT122新抗原mRNA疫苗精准狙击多癌种,肠癌患者生存期突破超3年,肾癌缩小90%
BNT122(商品名Cevumeran,代号RO7198457)是一款创新型个体化新抗原mRNA疫苗,基于患者肿瘤组织的体细胞突变数据定制设计,可编码20余种肿瘤特异性新抗原,刺激机体产生这些新抗原的T细胞免疫反应,从而实现降低肿瘤复发风险、延长生存期的目的。临床研究显示,该疫苗对乳腺癌、黑色素瘤、肾细胞癌、尿路上皮癌、非小细胞肺癌、直肠癌等多种实体瘤均展现治疗潜力。
全球顶尖期刊《Nature Medicine》近期公布了BNT122治疗晚期实体瘤的1期GO39733临床试验(NCT03289962)的振奋数据。该研究纳入213例局部晚期、转移性或复发性恶性实体瘤患者,均为接受至少一种标准疗法后病情进展的难治性病例。
结果显示:对检查点抑制剂(CPI)初治患者疗效:黑色素瘤(n=9)患者的客观缓解率(ORR)33.3%;肾细胞癌(n=12)ORR为33.3%;尿路上皮癌(n=11)ORR为18.2%;非小细胞肺癌(n=10)ORR为10.0%。其中,1例胃癌(50μg 单药治疗组),及1例直肠癌(38μg 联合治疗组)患者奇迹般达到完全缓解(CR)。
尤为值得关注的是,两项突破性临床案例展现出令人振奋的治疗潜力:
案例1:直肠癌患者实现3年长期生存
一例为微卫星稳定(MSS)、PD-L1低表达的直肠癌患者(21号患者),二线治疗后肺部存在1.1cm病灶。接受9剂38μgBNT122联合阿替利珠单抗治疗后,肿瘤完全缓解(CR),且缓解持续8.2个月。更令人欣慰的是,截至数据统计时止,该患者已存活超3年(40.7个月)(详见下图)。
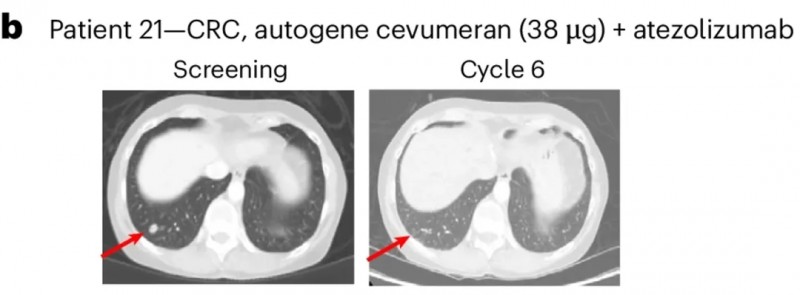
▲图源“nature”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
案例2:肾癌患者肿瘤缩小近10倍
另一例肾癌患者(患者38),入组前已接受4线治疗(含纳武单抗),初期病情进展后经BNT122治疗实现部分缓解(PR):胸膜靶病灶最长直径总和从基线108mm缩小至10mm,肿瘤显著缩小近10倍(肿瘤退缩幅度达90%)!
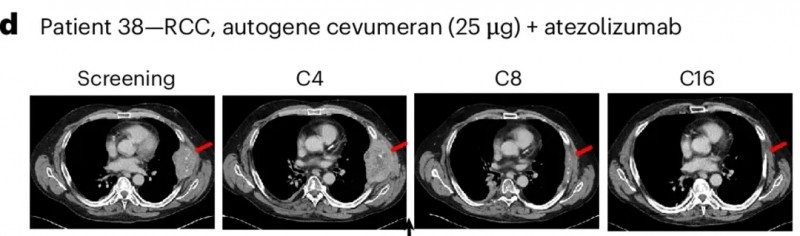
▲图源“nature”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
从"不可切除"到"长期存活":WT1-DC疫苗突破胰腺癌"死亡魔咒",中位总生存超3年
胰腺导管腺癌(PDAC)因恶性程度高、常规治疗耐药性强,一直是癌症攻克的难点。研究发现,转录因子WT1在PDAC肿瘤细胞中广泛表达,犹如癌基因的“助推器”,驱动肿瘤侵袭转移,是极具潜力的治疗靶点。而树突状细胞(DC)作为免疫系统的“侦察兵”,在启动肿瘤抗原特异性免疫反应中起关键作用。基于此,科研团队研发出新型WT1肽脉冲树突状细胞(WT1-DC)疫苗,相关成果发表于《癌症免疫治疗杂志》。
该研究共纳入10例不可切除的胰腺导管腺癌(PDAC)患者,包括6例局部晚期(III期)、3例转移性、1例术后复发患者。所有患者先接受白蛋白结合型紫杉醇+吉西他滨联合治疗,随后回输WT1-DC疫苗。结果显示如下:
1、肿瘤缓解与稳定:通过CE-CT评估显示,所有患者肿瘤负荷均下降(降幅0.0%~57.4%),其中7例(6例局部晚期+1例转移性)获部分缓解(PR),3例病情长期稳定。
2、生存期突破:9例患者中位无进展生存期(PFS)达2.23年(详见下图A),中位总生存期(OS)3.52年(详见下图B)。其中5例局部晚期患者中位PFS为2.48年,OS尚未达到,显著优于3例转移性患者的1.37年PFS和2.41年OS。
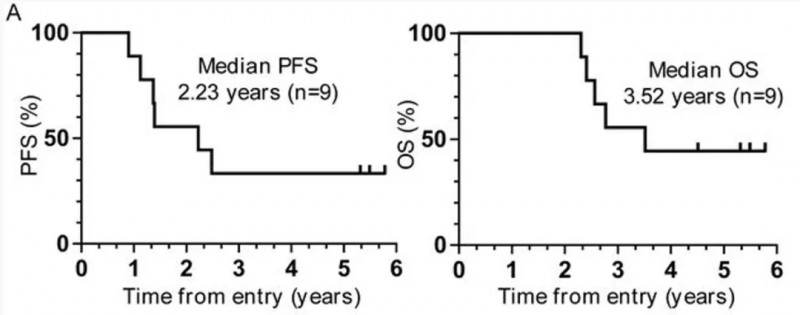
▲图源“J Immunother Cancer”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
值得一提的是,4例接受R0切除的局部晚期患者中,3例持续呈现WT1-DTH阳性,且自治疗起均存活超4.5年。下图展示了一例代表性胰腺癌患者经WT1-DC疫苗治疗前后的影像图对比。
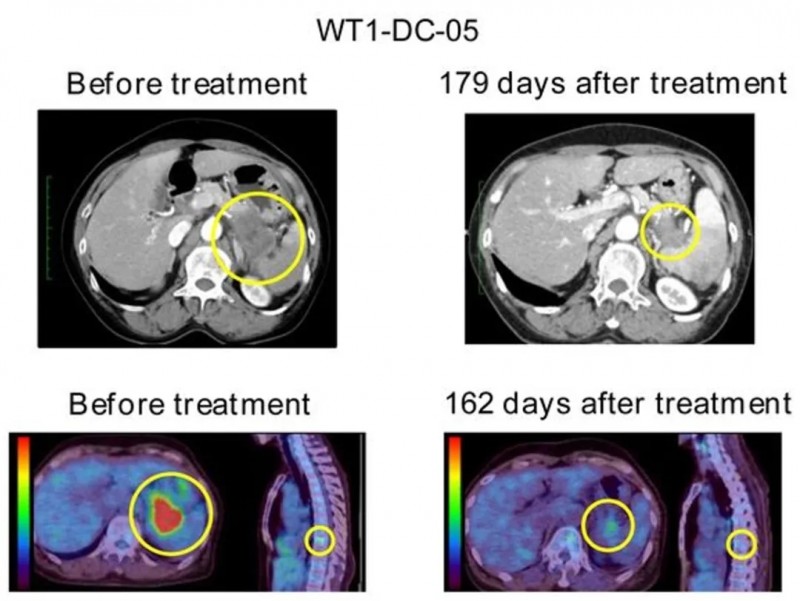
▲图源“J Immunother Cancer”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
无法耐受手术及放疗者也有春天!WT1-DC疫苗联合化疗击退IV期肺癌全身转移,无进展生存577天
WT1树突状细胞疫苗(WT1-DC)除了治疗胰腺癌、肠癌外,还可用于治疗肺癌。《Cureus》曾报道过WT1-DC疫苗联合化疗,助肺癌全身转移患者无进展生存577天的突破性案例。该69岁男性患者确诊右肺中叶IV期鳞状细胞癌,伴多发性骨转移、肝转移及双侧肾上腺转移,因无法耐受手术及放疗,遂入组接受WT1-DC联合化疗(卡铂AUC6+紫杉醇)治疗。结果显示如下:
1、无进展生存期(PFS)显著延长:治疗后,患者无进展生存期(PFS)超577天。治疗期间癌胚抗原(CEA)曾持续升高,但经联合雷莫芦单抗+多西他赛后降至5.9(正常范围)。体能状态评分1分,可正常生活。
2、肺部原发灶及复发病灶动态退缩:该患者治疗前,胸部CT显示右下肺原发肿瘤,伴双侧胸腔积液;在WT1-DC治疗第114天:肺部原发病灶几乎消失;治疗第213天:虽原发灶轻度复发;但在治疗第338天:原发及复发病灶再次缩小(详见下图)。
▼该患者WT1-DC治疗前后胸部CT图像对比
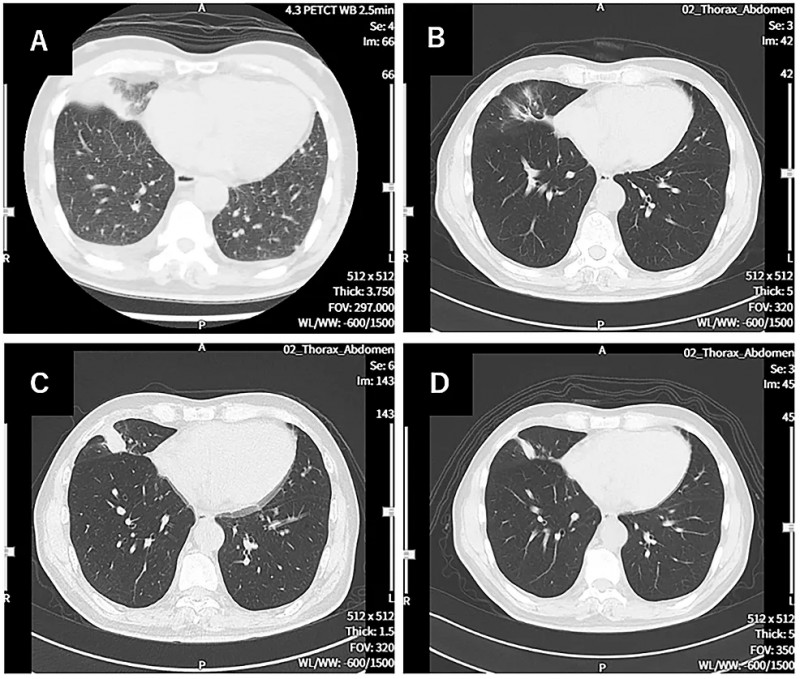
▲图源“Cureus”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
3、全身转移灶显著改善:该患者治疗前,PET-CT显示右下肺原发肿瘤,伴双肺、肝脏、肾上腺及骨骼多发性转移;治疗第479天,全身转移灶明显消退,仅残留右肺(1.0cm)及肝脏(1.7cm)转移灶,其余病灶均消失(详见下图)。
▼该患者WT1-DC治疗前后全身PET-CT对比
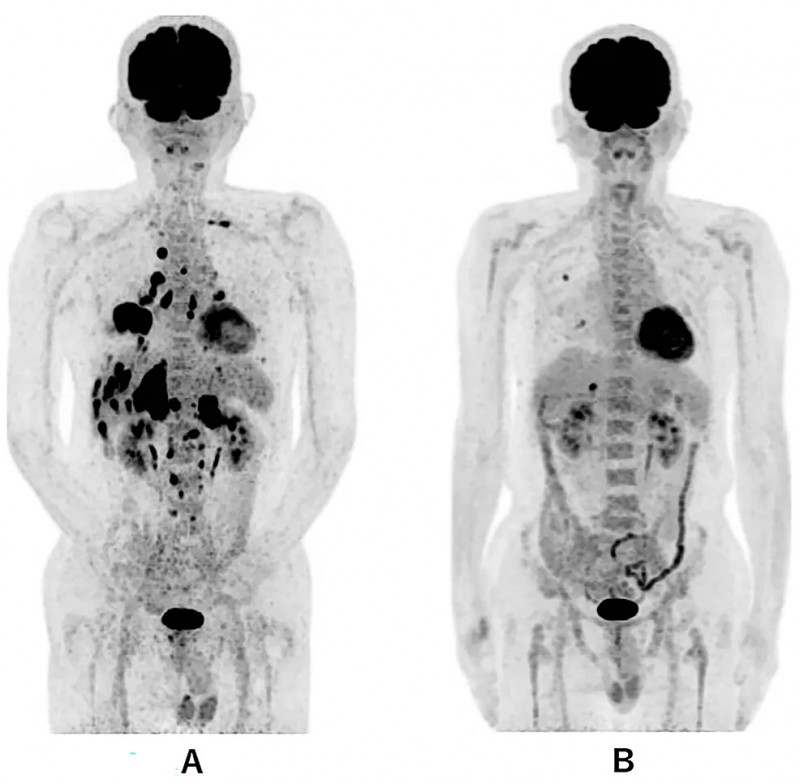
▲图源“Cureus”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
小编寄语
癌症作为一种高度复杂且突变频繁的疾病,仅依靠单一治疗手段,很难达到理想的治疗效果。目前,较为理想的治疗策略是在权威医院进行手术、放化疗等传统治疗的基础上,综合考虑患者的病情严重程度、个体体质差异、突变靶点特征以及经济状况等多方面因素,合理辅助靶向药物、免疫细胞治疗(如CAR-T、TCR-T、TIL细胞疗法、DC疫苗等)、质子治疗、电场疗法等新型治疗手段。通过这种多管齐下的治疗方式,能够巩固传统治疗的效果,降低肿瘤复发风险,提高患者的生存质量,并有效延长生存期。
其中,癌症疫苗历经数十年的发展,逐渐从基础研究转向了临床研究阶段,近年来更是取得了突破性进展。NHS国家癌症临床主任Peter Johnson教授曾说过:“我们知道,即使手术成功,癌症有时也会复发。这可能与体内仍残留少量癌细胞有关,但使用针对这些残留癌细胞的癌症疫苗,或许可以阻止这种情况的发生”。小编也希望终有一天能实现“打一针治疗癌症”的美好愿景!好消息是,我国现阶段正在进行多款癌症疫苗的临床研究,对此感兴趣的病友,可将治疗经历、近期病理及影像学检查结果,提交至医学部,进行初步评估。
参考资料
[1]Shi W,et al.Advances on cancer vaccine trials registered in China and the USA in 2014-2024[J]. Frontiers in Oncology, 2025, 15: 1557253.
https://www.frontiersin.org/journals/oncology/articles/10.3389/fonc.2025.1557253/full
[2]Lopez J,et al.Autogene cevumeran with or without atezolizumab in advanced solid tumors: a phase 1 trial[J]. Nature Medicine, 2025: 1-13.
https://www.nature.com/articles/s41591-024-03334-7
[3]Koido S,et al.Dendritic cells pulsed with multifunctional Wilms' tumor 1 (WT1) peptides combined with multiagent chemotherapy modulate the tumor microenvironment and enable conversion surgery in pancreatic cancer. J Immunother Cancer. 2024 Oct 8;12(10):e009765.
https://jitc.bmj.com/content/12/10/e009765.long
[4]Nagai H,et al.WT1 Dendritic Cell Vaccine Therapy Improves Immune Profile and Prolongs Progression-Free Survival in End-Stage Lung Cancer[J].Cureus,2023,15(10).
https://www.cureus.com/articles/193305-wt1-dendritic-cell-vaccine-therapy-improves-immune-profile-and-prolongs-progression-free-survival-in-end-stage-lung-cancer#!/
扫描进患者病友群

肺癌|胃癌|肝癌|结直肠癌|胰腺癌
乳腺癌|脑瘤|淋巴瘤|儿童肿瘤等

相关推荐

2026年这些肺癌疫苗正悄然改变患者的生
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
新一代NTRK基因融合突变靶向药TL11
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
实现33个月长生存!中国团队成功攻克&q
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

破解术后复发噩梦!NK细胞疗法让晚期胃癌
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

【胃癌CAR-T细胞疗法】IMC002注
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
晚期肺癌实现完全缓解!2026非小细胞肺
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05







![[field:title/]](/uploads/allimg/20200224/1-2002241I5262J.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241I3461D.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H94LK.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241HKW34.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H619327.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H34H52.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H22IH.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241G93O18.jpg)




