伊基奥仑赛长生存数据出炉:3年生存率超66%!多款国研首创CAR-T猛攻肺癌、肝癌、卵巢癌等
伊基奥仑赛长生存数据出炉:3年生存率超66%!多款国研首创CAR-T细胞疗法猛攻肺癌、肝癌、卵巢癌等
2025年9月19日,驯鹿生物宣布,其自主研发的全人源靶向BCMA CAR-T细胞治疗产品——伊基奥仑赛注射液(Eque-cel,福可苏®)针对复发/难治性多发性骨髓瘤(R/RMM)的FUMANBA-1研究36个月长期随访数据,已在国际骨髓瘤学会(IMS)年会发布,最终结果以口头报告呈现(摘要号:2142568)。
结果进一步证实,伊基奥仑赛注射液能为R/R MM患者(包括具有高危特征者)带来深度且持久的疗效,且长期安全性可控,可显著提升患者长期生存质量。这一成果不仅为全球深陷治疗困境的患者点亮了长期生存的希望,更标志着中国自主创新CAR-T疗法在国际舞台上站稳脚跟,为全球血液肿瘤治疗的突破注入了强劲的“中国力量”!

▲图源“PR Newswire”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
伊基奥仑赛注射液:筑牢深度持久缓解"防护墙",破解多发性骨髓瘤耐药复发困局
多发性骨髓瘤(MM)是全球第二大常见血液系统恶性肿瘤,作为一种恶性浆细胞肿瘤,以骨质破坏、髓外受累为典型特征。根据GLOBOCAN数据,2022年全球MM发病率为1.8例/10万人,五年患病率为6.8例/10万人,且对多种药物耐药、易多次复发,因此,迫切需要寻求可实现深度持久缓解的新型治疗方案。
而如今这一情况终于有了转机,伊基奥仑赛注射液(Equecabtagene Autoleucel,福可苏®)是一款创新型全人源抗BCMA CAR-T细胞疗法,通过慢病毒作为基因载体转染自体T细胞制备而成。其CAR结构包含全人源scFv、CD8a铰链区与跨膜结构域、4-1BB共刺激分子及CD3ζ激活结构域。基于严格的分子结构筛选与全面的体内外功能评估,该疗法展现出快速强效的治疗效果,且具备优异的体内长期持久性,能帮助患者获得深度持久缓解,为MM患者带来持续的治疗获益与保障。
伊基奥仑赛注射液的卓越疗效源于其独特设计:凭借适度的抗原亲和力,可实现CAR-T细胞与肿瘤细胞的快速结合与解离,既能快速起效清除肿瘤,又能避免过度激活;同时作为全人源CAR-T产品,其免疫原性低,能维持CAR-T细胞的低衰竭表型,从而实现持久疗效与持续抗肿瘤活性,最终延长患者生存期。
伊基奥仑赛3年随访数据重磅发布:总缓解率96.3%、3年存活率66.3%,CAR-T初治者PFS达35.9个月,点亮高缓解+长生存希望
国际骨髓瘤学会(IMS)发布的这项1b/2期FUMANBA-1临床试验的长期随访数据。该研究共纳入109例复发/难治性多发性骨髓瘤(R/RMM)患者,均为既往接受至少三线治疗且最后一线治疗后病情进展的人群,其中12.8%合并髓外病变(EMD),11%曾接受过BCMA CAR-T治疗。所有患者入组后先接受淋巴细胞清除治疗(环磷酰胺+氟达拉滨),再单次输注伊基奥仑赛注射液(Eque-cel),结果显示如下:

▲截图源自“PR Newswire”
1、缓解率表现优异:在107例可评估患者中,总缓解率(ORR)达96.3%,其中83.2%实现完全缓解/严格完全缓解(CR/sCR);而在CAR-T初治患者中,疗效更优——ORR提升至98.9%,CR/sCR率达88.4%。
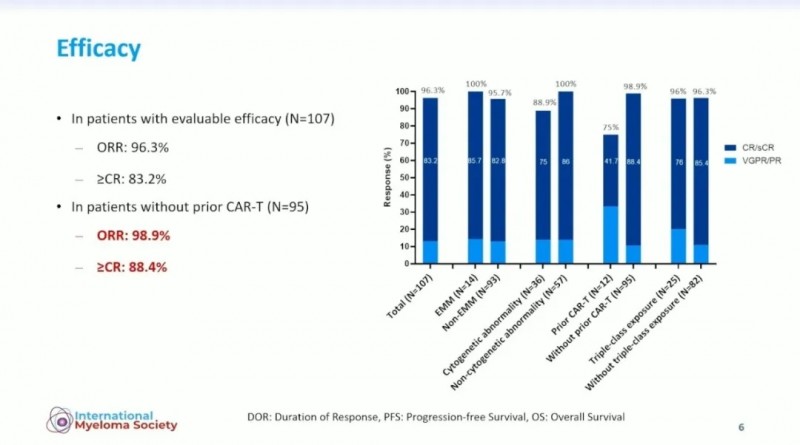
▲图源“PR Newswire”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
2、MRD阴性率高且持久:所有患者微小残留病灶(MRD)阴性率为95.3%,其中达到CR的89例患者MRD阴性率达100%,CAR-T初治患者MRD阴性率为98.9%。此外,患者MRD阴性持续时间中位数为36.5个月(95%CI:25.56-未达到[NE]),12个月、24个月、36个月MRD阴性率分别为81.0%(95%CI:71.2%-87.7%)、62.2%(95%CI:50.6%-71.9%)、50.2%(95%CI:37.9%-61.3%)。
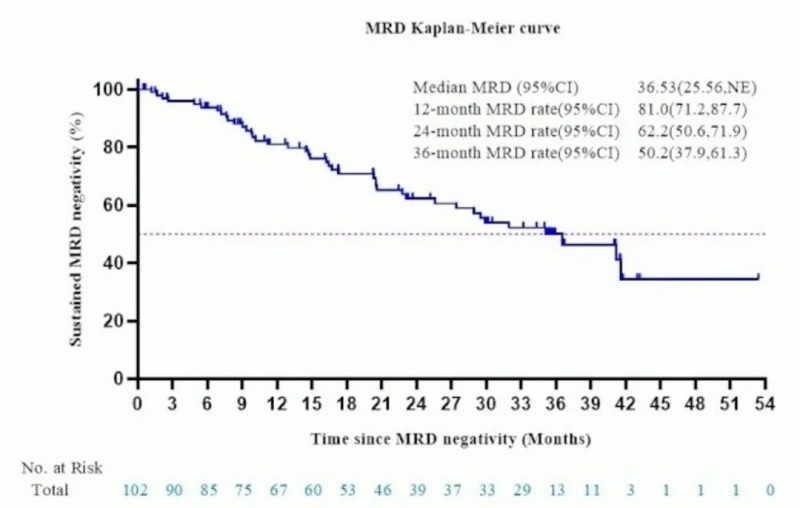
▲图源“PR Newswire”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
3、生存数据亮眼:109例接受Eque-cel治疗的患者中,中位无进展生存期(PFS)为30.5个月(95%CI:24.11-42.15);CAR-T初治患者中位PFS延长至35.9个月(95%CI:25.95-47.67),达到CR的患者中位PFS更达39.8个月(95%CI:30.26-NE)。目前患者中位总生存期(OS)尚未达到,3年随访时仍有66.3%的患者存活;中位缓解持续时间(DOR)为31.3个月,中位随访时间36个月,充分体现长期疗效优势。
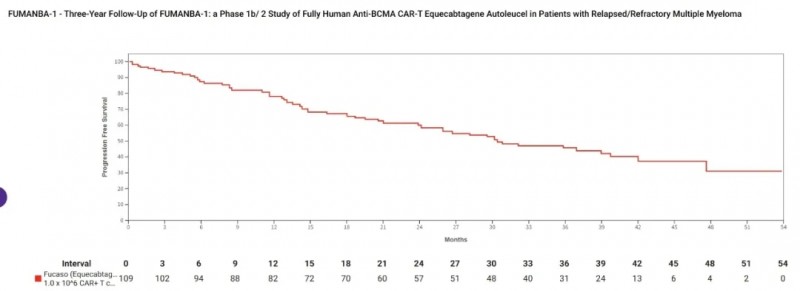
▲图源“PR Newswire”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
4、长期安全性表现良好:93.6%的患者发生细胞因子释放综合征(CRS),仅1例为≥3级;仅2例患者报告免疫效应细胞相关神经毒性综合征(ICANS),且均为1-2级;全程未观察到迟发性神经毒性或继发性恶性肿瘤,未发现新的安全信号。综上,FUMANBA-1研究的3年随访数据再次证实,Eque-cel在经多线治疗(含高危特征)的R/RMM患者中,能实现深度且持久的缓解,维持高MRD阴性率,且长期安全性可控;尤其CAR-T初治患者35.9个月的中位PFS,可显著延长患者无治疗间隔、改善生活质量。我们期待这一高质量CAR-T疗法能惠及全球更多R/RMM患者,为更多家庭带去治疗希望。
CAR-T疗法实体瘤突破不断,多癌种临床火热招募中
CAR-T细胞疗法在血液肿瘤治疗中的卓越疗效有目共睹,近年来在实体瘤领域亦斩获多项突破性进展——针对GPC3、CEA、Claudin18.2、间皮素(mesothelin)等关键实体瘤靶点,已涌现出多项瞩目的研究成果。
▼临床前和临床试验中,CAR-T细胞疗法的潜在靶向抗原
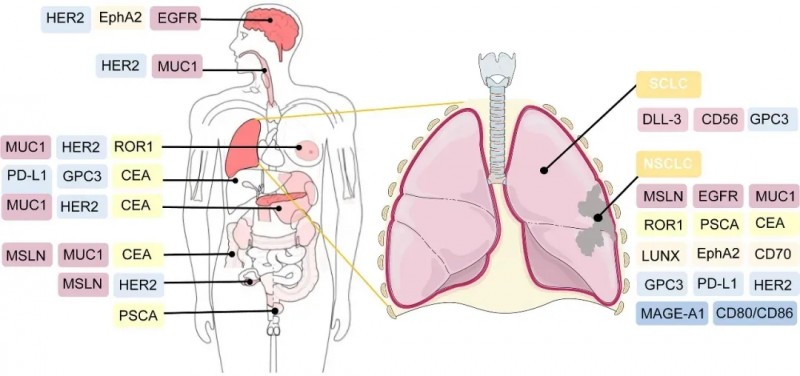
▲图源“frontiers”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
· 中国患者如何寻求CAR-T疗法帮助 ·
好消息是,目前有多款CAR-T临床实验正在火热招募中,主要针对Claudin18.2、GPC3、GUCY2C、PSMA、CEA、间皮素(mesothelin)、MUC-1、BCMA、CD1、CD20等靶点。以及胰腺癌、胃癌、肝癌、结直肠癌、神经胶质瘤、肺癌、多发性骨髓瘤、多发性骨髓瘤、弥漫大B细胞淋巴瘤等癌种。
做过基因检测的患者,可自行查看基因检测报告,一旦发现存在上述突变,可将近期病理报告、基因检测报告等资料汇总后,提交至医学部,初步评估是否有机会参加相关临床试验。一旦审核通过,有机会获得”天价“疗法免费治疗的机会。看不懂检测报告或想要明确相关靶点的患者,也可联系医学部,详细解读报告或了解检测详情。
全球首个GPC3 CAR-T肝癌临床传捷报:中位总生存达278天
其中,GPC3(磷脂酰肌醇蛋白聚糖-3)是一种参与调控细胞迁移、增殖与存活的硫酸肝素蛋白聚糖:其在72%的晚期肝细胞癌(HCC)组织中呈高表达,且与患者术后转移风险显著相关;反观正常肝脏、肝硬化肝脏及肝良性病变(如发育不良结节、肝腺瘤)组织,均未检测到GPC3表达。这种“癌有正常无”的特性,让GPC3成为肝癌靶向治疗的理想靶点——既能精准识别癌细胞,又可避免损伤健康肝组织。
基于此,研究人员开展了全球首个靶向GPC3的CAR-T细胞治疗肝细胞癌的临床试验,相关数据同步发表于国际重磅肿瘤学期刊《Clinical Cancer Research》。该研究共纳入13例晚期肝细胞癌患者,中位年龄51岁(34-70岁),均为经手术、局部治疗或全身系统治疗后病情进展的难治性患者,临床已无标准治疗方案可选;经检测确认肿瘤细胞表面GPC3抗原阳性后,患者入组接受CAR-GPC3 T细胞回输治疗。
结果显示:13例患者中2例达到部分缓解(PR),肿瘤病灶显著缩小;3年、1年、6个月生存率分别为10.5%、42.0%、50.3%,中位总生存期(OS)达278天(95%CI:48~615天)(详见下图)。好消息是,目前我国正在开展关于GPC3 CAR-T的临床研究。
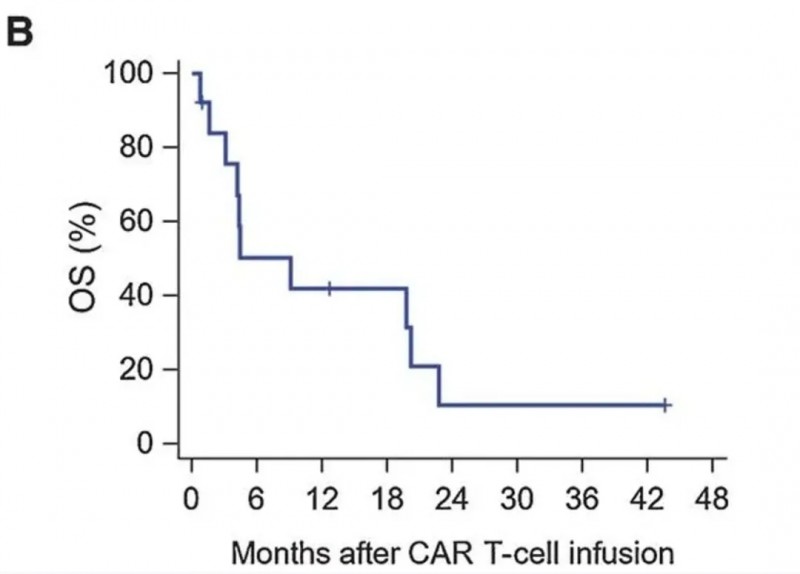
▲图源“AACR”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
其中,患者P3与P13的治疗情况尤为值得关注,尤其是P3的疗效堪称亮眼——该患者为50岁男性,有2.2年多灶性肝癌病史,入组前GPC3 IHC染色强度评分为3+(强阳性);接受CAR-GPC3 T细胞治疗后,CT显示病灶从31.0×27.8mm缩小至12.2×9.5mm,经评估达到部分缓解(PR),无进展生存期(PFS)达111天,为晚期肝癌治疗提供了突破性范例。
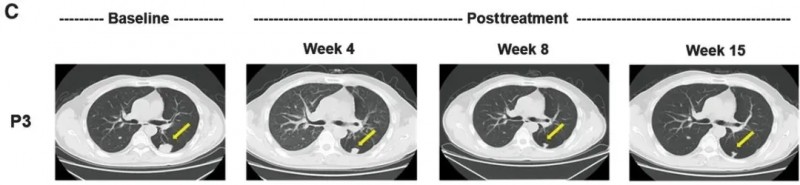
▲图源“AACR”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
全球首创国研KT032 CAR-T:卵巢癌/间皮瘤疾病控制率100%,生存期远超预期
近期,国研新型CAR-T细胞疗法KT032引发广泛关注,其首次人体临床试验表现亮眼——在卵巢癌与间皮瘤患者中疾病控制率达100%!
KT032是全球首创的靶向间皮素(MSLN)多链DAP-CAR-T细胞疗法。在体外细胞杀伤试验与异种移植模型中,该疗法(尤其由自然杀伤细胞免疫球蛋白样受体截短体与DAP12结合形成的多链DAP-CAR-T),相比其他与DAP12、DAP10或CD3ζ相关的自然杀伤细胞激活受体介导的CAR-T,展现出更优的细胞毒性与肿瘤杀伤能力。
该研究共纳入8例晚期难治性卵巢癌或间皮瘤患者(7例卵巢癌、1例间皮瘤),所有患者均至少接受过2种标准治疗(如化疗、靶向药)后复发或进展,且经病理检查确认肿瘤细胞间皮素表达≥15%(间皮素为该CAR-T疗法的精准靶点)。
结果显示:8例患者中,6例肿瘤被有效压制,无1例出现快速进展,疾病控制率(DCR)达100%,意味着CAR-T细胞成功“拖住”肿瘤进展;患者中位无进展生存期(PFS)达5.5个月,中位总生存期(OS)达10.5个月,远超同类患者预期生存时间。部分患者治疗后癌抗原125(CA125)水平显著下降,4例达到“疾病稳定”(肿瘤未增大或略有缩小),治疗有效率远超传统方案。
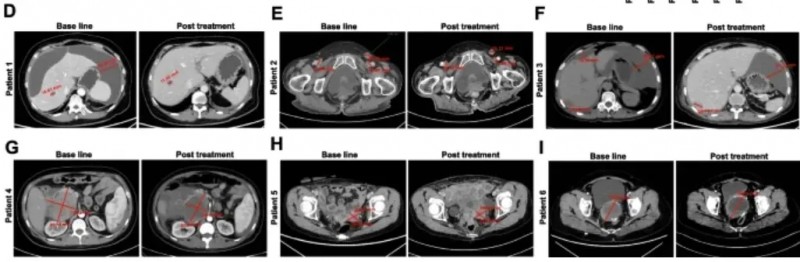
更值得关注的是,该疗法部分缓解率达33.3%:2例患者实现“部分缓解”(肿瘤缩小≥30%),其中患者1肝转移灶缩小31%且腹腔积液消失,患者2可测量病灶总最大直径缩小42%。
国产首个!靶向CEA CAR-T(C-13-X)闪耀ASCO大会,肺癌DCR高达93%,总生存率达71%
近期,我国自主研发的国内首个获得临床试验许可的靶向CEA CAR-T产品——C-13-X,在2025年美国ASCO大会上,公布了其在晚期复发或难治性非小细胞肺癌(NSCLC)研究者发起临床试验(IIT)中的突破性进展。
C-13-X依托专为实体瘤肿瘤微环境开发的PhiCAR®与RESCAR®技术平台,旨在攻克实体瘤微环境抑制难题,适用范围覆盖≥18周岁的CEA阳性晚期恶性肿瘤患者,包括结直肠癌、食管癌、胃癌、胰腺癌、非小细胞肺癌、乳腺癌、胆管癌等。
在C-13-X治疗晚期转移性NSCLC的Ⅰ期临床试验(NCT060006390)中,共纳入15例经多线治疗失败的难治性晚期患者,所有患者均接受C-13-X输注并纳入最终分析。
结果显示:入组患者的1年总生存率(OS)高达71.1%,整体疾病控制率(DCR)达87%(13/15),其中肺部靶病灶DCR更是高达93%,客观缓解率(ORR)达47%(7/15)。值得关注的是,进一步分析表明,CEA表达水平≥30%的患者缓解趋势更显著,提示这类患者能从C-13-X治疗中获得更多获益。
此外,C-13-X的生存数据同样亮眼,1年总生存率(OS)高达71.1%,堪称肺癌治疗领域的重大突破。这一成果为CAR-T治疗实体瘤(尤其是晚期肺癌)提供了强有力的初步证据,更为肺癌患者点亮了新的治疗希望!
国研CEA CAR-T精准狙击"癌细胞特供"靶标!70%结直肠癌患者获病情稳定,最长持续超7.5个月
CEA(癌胚抗原)是一种特殊糖蛋白,胚胎期短暂表达,成年后仅在胃肠道上皮细胞中低水平存在。但在多种实体瘤中,CEA呈“异常活跃”状态——结直肠癌、70%的非小细胞肺癌、50%的乳腺癌,以及胃癌、胰腺癌等癌细胞表面,均高表达CEA。这种“癌细胞特供”的表达模式,让CEA成为精准抗癌的“黄金靶标”:CAR-T细胞可通过识别CEA,像导弹般锁定癌细胞,不伤及正常细胞。
基于此特性,中国团队研发了CEA CAR-T疗法,主要针对规范治疗后进展的患者,包括化疗/靶向耐药的结直肠癌、既往治疗失败或CEA升高的非小细胞肺癌,以及乳腺癌、胃癌、胰腺癌患者。
我国此前开展过一项“CEA CAR-T细胞疗法治疗CEA阳性结直肠癌(CRC)”的I期临床试验(NCT02349724),结果令人振奋,多数患者治疗后观察到明确疗效。
该研究共纳入10例转移性结直肠癌(CRC)患者,中位年龄58岁(范围48.8-67岁),其中80%(8/10)伴肝转移、50%(5/10)伴肺转移,所有患者入组后均接受CEA CAR-T细胞静脉输注。
结果显示:10例既往治疗进展(PD)的患者中,7例经CAR-T治疗后达病情稳定(SD),肿瘤直径仅轻微变化,其中P3、P5患者稳定期超30周(7.5个月)。
值得一提的是,其中两例典型病例的疗效尤为突出:
一例P9-2患者:在接受CEA CAR-T回输后,PET/CT显示肿瘤活动减弱、代谢活性显著降低。下图展示了CAR-T输注前(左图)、治疗4周后(右图)的PET/CT对比。
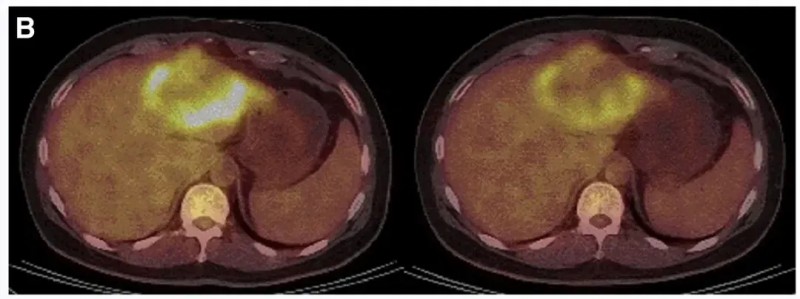
▲图源“Molecular Therapy”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
另一例P10患者:在接受DL4剂量CEA CAR-T治疗后,MRI证实肝内一处病灶缩小。下图展示了CAR-T治疗前(左图)、治疗4周后(右图)的MRI对比。
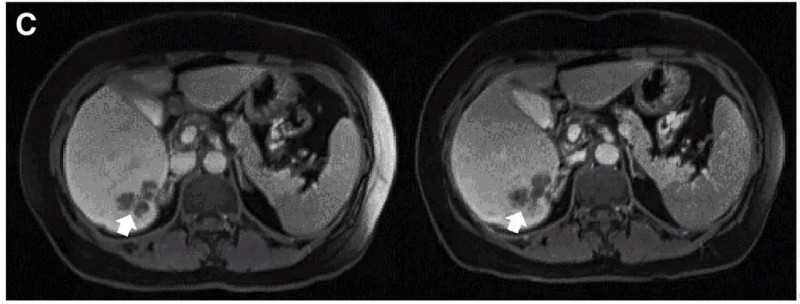
▲图源“Molecular Therapy”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
小编寄语
CAR-T疗法在血液肿瘤治疗领域战绩斐然,国内外已有多款产品获批上市,为复发或难治性白血病、淋巴瘤、骨髓瘤等血液肿瘤患者带来了“生”的希望!更令人振奋的是,近年来全球研究人员从未停止探索脚步,通过钻研新型策略,攻克肿瘤抗原异质性、打破免疫抑制等难题,已在胃癌、脑瘤、胰腺癌、肝癌、结直肠癌等实体瘤领域取得突破性进展!
目前,国内多家癌症中心正开展CAR-T的临床试验,晚期耐药、术后高危等患者均可提交病历评估入组资格。想寻求CAR-T、TCR-T、TIL等细胞疗法及其他国内外治疗新技术帮助的患者,可将治疗经历、影像学检查结果等,提交至医学部,进行初步评估。
参考资料
[1]Shi, Donghua,et al."Chimeric antigen receptor-glypican-3 T-cell therapy for advanced hepatocellular carcinoma: results of phase I trials." Clinical Cancer Research 26.15 (2020): 3979-3989.
https://aacrjournals.org/clincancerres/article/26/15/3979/82521/Chimeric-Antigen-Receptor-Glypican-3-T-Cell
[2]Zhang C,et al.Phase I escalating-dose trial of CAR-T therapy targeting CEA+ metastatic colorectal cancers[J]. Molecular Therapy, 2017, 25(5): 1248-1258.
https://www.cell.com/molecular-therapy-family/molecular-therapy/fulltext/S1525-0016(17)30108-9?returnURL=https%3A%2F%2Flinkinghub.elsevier.com%2Fretrieve%2Fpii%2FS1525001617301089%3Fshowall%3Dtrue
[3]https://www.prnewswire.com/news-releases/2025-ims--iaso-bio-highlights-three-year-follow-up-data-of-car-t-cell-therapy-fucaso-for-multiple-myeloma-treatment-302561198.html
[4]https://www.cancernetwork.com/view/eque-cel-displays-favorable-long-term-survival-in-r-r-multiple-myeloma
扫描进患者病友群

肺癌|胃癌|肝癌|结直肠癌|胰腺癌
乳腺癌|脑瘤|淋巴瘤|儿童肿瘤等

相关推荐

癌症治疗本就不应千篇一律,揭秘mRNA癌
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
“不限癌种”新突破,NTRK基因融合的靶
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
肺癌疫苗重大突破,晚期患者多了一个新的选
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

“手术成功”不等于万事大吉,新型癌症疫苗
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

2026年靶向治疗抗癌风暴,突破困境,普
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

2026年这些肺癌疫苗正悄然改变患者的生
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05






![[field:title/]](/uploads/allimg/20200224/1-2002241I5262J.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241I3461D.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H94LK.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241HKW34.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H619327.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H34H52.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H22IH.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241G93O18.jpg)




