我国初代治白血病的CAR-T产品上市,总缓解率达82.1%,价格创历史新低!
我国初代白血病CAR-T产品上市,获批上市的CAR-T药品有哪些
据“搜狐网”近期报道,我国第四款CAR-T细胞产品——纳基奥仑赛注射液(Inaticabtagene Autoleucel Injection,CNCT19细胞注射液,商品名:源瑞达)的处方,在中国医学科学院血液病医院开出,国内定价为99.9万元/支,目前已获已获中国国家药监局(NMPA)批准,用于成人复发或难治性B细胞急性淋巴细胞白血病(r/r B-ALL)的治疗。
该药的出现不仅打破了CAR-T疗法“百万定价”的门槛,而且还是首款在中国获批上市的治疗白血病的CAR-T产品,并被国家药监局药品审评中心(CDE)纳入“突破性治疗药物”!
一、纳基奥仑赛——急性淋巴细胞白血病的"克星"
成人B细胞急性淋巴细胞白血病(B-ALL)初治后复发率高,虽然诱导化疗的反应率很高,但仅有30%~40%的成年ALL患者可实现长期缓解,约60%的患者会进展到预后较差的复发或难治阶段(r/r B-ALL),纳基奥仑赛的出现为此类患者带来了新的希望!
此次获批上市是基于一项关键性的临床研究(NCT04684147)结果。合源生物在2022年12月举行的第64届美国血液学年会(ASH)上,以口头报告的形式发布了相关研究数据。
该研究选取39例成人r/r B-ALL患者入组,其中,29例(74.3%)患者既往接受过≥2线抗B-ALL的标准治疗,7例(17.9%)患者既往接受过造血干细胞移植。这些患者在接受清淋(环磷酰胺+氟达拉滨)预处理后,输注赫基仑赛注射液,结果显示:
●总体缓解率(ORR)高:这39例接受治疗的患者中,治疗3个月内的ORR为82.1%,有32例患者达到缓解;治疗3个月时的ORR为64.1%,经IRC评估有25例患者达到缓解。
●完全缓解(CR)率高:在治疗3个月内获得ORR的32例患者中,有26例完全缓解(CR),CR率为66.7%(26/39);在治疗3个月时获得ORR的25例患者中,有20例完全缓解(CR),CR率为51.3%(20/39)。
●微小残留病灶(MRD)阴性率高:在治疗3个月时和3个月内,达“完全缓解”或“完全缓解但计数不完全恢复”(CR/CRi)的患者中,其MRD阴性率分别为92.0%、100%。
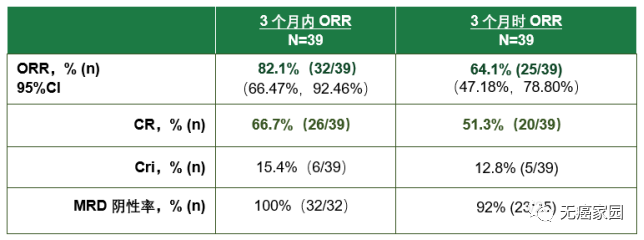
▲纳基奥仑赛有效性数据总结
目前急招B细胞淋巴瘤、T细胞淋巴瘤、T细胞白血病(T-ALL)、急性淋巴细胞白血病、非霍奇金淋巴瘤、胃癌、肝癌、胰腺癌、结直肠癌、间皮瘤、卵巢癌等癌种!
想要评估病情是否能够接受CAR-T疗法可将病理报告、治疗经历及出院小结等提交至医学部进行初步评估!
二、打破传统抗癌模式的"CAR-T疗法"
传统的抗癌疗法,如手术、化疗和放疗等,虽然在降低癌症相关死亡率和改善治愈前景方面,取得了不可否认的成功。但同时也会因健康组织的附带损害,而伴随严重的副作用,比如因化疗引起的恶心、脱发、头痛、肌肉损伤等,会降低患者的生活质量。因此,近几十年癌症治疗逐渐进入免疫疗法和精准治疗的时代,以进一步提高总体生存率,并降低全身毒性。其中,免疫治疗是使用抗体、细胞因子和免疫细胞,来调节宿主对癌症的免疫反应。而CAR-T细胞疗法是唯一获得FDA(美国食品和药物管理局)或EMA(欧洲药品管理局)商业化批准的过继性免疫疗法。
嵌合抗原受体T细胞疗法(CAR-T细胞疗法),是通过插入一段编码嵌合抗原受体(CAR)的DNA片段,对患者自体T细胞进行基因重新编程,仿佛在T细胞上安装了“导航头”,使其可以更好地靶向并杀死癌细胞,并产生持续的免疫反应。
目前获批上市的CAR-T细胞产品集中在血液肿瘤治疗方面,靶点锁定在CD19和BCMA。因为在血液恶性肿瘤中,CAR-T细胞无需穿透致密的细胞外基质(ECM)层,即可到达肿瘤细胞,与实体瘤相比更易到达靶细胞,为急性淋巴细胞性白血病、多发性骨髓瘤、弥漫大B细胞淋巴瘤等血液肿瘤的治疗,带来一场颠覆性的变革!不过近年来研究人员也在不断尝试将CAR-T疗法用于实体瘤方面的研究。
三、已获批上市的CAR-T细胞产品
据无癌家园编获悉,目前已获批上市的CAR-T细胞产品共计10款,其中,国内已获批上市4款,国外已上市6款,详情见表2。
| CAR-T药物名称 | 适应症 | 上市国家 | 靶点 | 价格 | 获批时间 | |
| 1 | Kymriah(Tisagenlecleucel,Tisa-cel) | 复发或难治性弥漫大B细胞淋巴瘤 | 美国 | CD19 | 475,000美元 | 2017年8月30日 |
| 2 | Yescarta(Axicabtagene ciloleucel,Axi-cel) | 1、复发或难治性弥漫大B细胞淋巴瘤 2、复发或难治性滤泡细胞淋巴瘤 | 美国 | CD19 | 373,000美元 | 2017年10月18日 |
| 3 | Tecartus(Brexucabtagene autoleucel,KTE-X19) | 复发或难治性套细胞淋巴瘤 | 美国 | CD19 | 373,000美元 | 2020年7月24日 |
| 4 | Breyanzi(Lisocabtagene maraleucel) | 复发或难治性弥漫大B细胞淋巴瘤 | 美国 | CD19 | 410,300美元 | 2021年2月5日 |
| 5 | Abecma(Idecabtagene vicleucel,Ide-Cel) | 复发或难治性多发性骨髓瘤 | 美国 | BCMA | 419,500美元 | 2021年3月26日 |
| 6 | 西达基奥仓赛(Carvykti,Cilta-Cel) | 复发或难治性多发性骨髓瘤 | 美国 | BCMA | 465,000美元 | 2022年2月28日 |
| 7 | 阿基伦塞注射液(奕凯达) | 复发或难治性弥漫大B细胞淋巴瘤 | 中国 | CD19 | 120万人民币 | 2021年6月 |
| 8 | 瑞吉奥伦塞注射液(倍诺达) | 复发或难治性弥漫大B细胞淋巴瘤 | 中国 | CD19 | 129万人民币 | 2021年9月 |
| 9 | 伊基奥仑赛注射液(福可苏) | 复发或难治性多发性骨髓瘤 | 中国 | BCMA | 116.6万人民币 | 2023年6月 |
| 10 | 纳基奥仑赛注射液(源瑞达,CNCT19细胞注射液) | 成人复发或难治性B细胞急性淋巴细胞 白血病 | 中国 | CD19 | 99.9万人民币 | 2023年11月1日 |
▲全球已获批上市的CAR-T细胞产品
CAR-T细胞疗法精准打击各类血液肿瘤
1、慢性淋巴细胞白血病——部分长期随访未复发
据《J Transl Med》报道,18例CD19阳性的慢性淋巴细胞白血病患者,在接受自体CD19 CAR-T细胞治疗后,在有反应的8例患者(57%)中,4例获得持久的完全缓解(CR)率,且在49个月的随访期内均未复发;剩余患者达到部分缓解(PR)。
2、急性淋巴细胞白血病——90%获得完全缓解
在2014年进行的一项临床试验中,30例(包括儿童和成人)患有B细胞急性淋巴细胞白血病(B-ALL)的患者,在接受一款CTL019(后被命名为Kymriah,为首款获批上市的CAR-T产品)治疗后,结果显示:
27例患者(90%)获得完全缓解,22例在输注后1个月,显示出MRD。在输注后6个月,总生存率为78%,无事件生存率达到67%。经过为期2年的随访,其中19例患者仍处于缓解状态。
3、多发性骨髓瘤——OR达98%
西达基奥仑赛是FDA批准的用于治疗多发性骨髓瘤(MM)的一款CAR-T细胞产品。
CARTITUDE-1研究结果显示,其严格完全缓解率(CR)达80%,客观缓解率(OR)达98%。在治疗12个月后,总生存期(OS)为89%,无进展生存期(PFS)为77%。
4、套细胞淋巴瘤——中位OS超18个月
Tecartus是唯一获得FDA批准,用于治疗成人复发或难治性套细胞淋巴瘤(MCL)的CAR-T细胞产品。
ZUMA-3 2期研究结果显示,该产品在97%的应答患者中具有显著的长期CR率(71%),其中位总生存期(OS)超过18个月,且未检测到微小残留病灶。
5、B细胞淋巴瘤——OR达83%
FDA批准的一款CAR-T细胞产品——Yescarta,治疗非霍奇金淋巴瘤的1/2期临床试验(ZUMA-1)结果显示,Yescarta组患者的客观缓解率(OR)为83%,完全缓解率(CR)为50%;而标准治疗组的OR仅为50%,CR仅为32%。显而易见,Yescarta组的OR和CR明显高于标准治疗组。
小编有话说
纳基奥仑赛注射液自2019年11月底,获得新药临床试验许可;到今年成功获批上市,在免疫细胞新药研发领域跑出了“中国速度”!据悉,我国还有多款CAR-T产品处于蓄势待发的状态,其中,包括正处于申请上市阶段的华东医药的泽沃基奥仑赛(BCMA),以及两款处于Ⅲ期临床研究阶段的产品,即诺华的CTL-019(CD19)、武汉思安医疗的B-cell malignancy(CD19)。
随着越来越多的CAR-T产品获批,“天价抗癌药”似乎也有开启价格战的苗头,未来或将看到它们共同携手奋战医保的场景。小编也期待这些产品可以尽早上市,惠及更多的患者!
参考资料
[1]Gu R,et al.Efficacy and safety of CD19 CAR T constructed with a new anti-CD19 chimeric antigen receptor in relapsed or refractory acute lymphoblastic leukemia[J]. Journal of Hematology & Oncology,2020,13:1-13.
https://jhoonline.biomedcentral.com/articles/10.1186/s13045-020-00953-8
[2]De Marco RC,et al.CAR T Cell Therapy: A Versatile Living Drug. Int J Mol Sci. 2023 Mar 27;24(7):6300. doi: 10.3390/ijms24076300.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC10094630/
[3]https://www.wolterskluwer.com/en/expert-insights/car-t-cell-therapy-a-remarkable-breakthrough-in-cancer-treatment
[4]https://finance.sina.cn/2023-11-28/detail-imzwecms4798997.d.html?vt=4&cid=76524&node_id=76524
[5]https://www.nmpa.gov.cn/zhuanti/cxylqx/cxypxx/20231108092415187.html
[6]http://www.juventas.cn/news.php?id=624
扫描进患者病友群

肺癌|胃癌|肝癌|结直肠癌|胰腺癌
乳腺癌|脑瘤|淋巴瘤|儿童肿瘤等

相关推荐

癌症治疗本就不应千篇一律,揭秘mRNA癌
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
“不限癌种”新突破,NTRK基因融合的靶
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
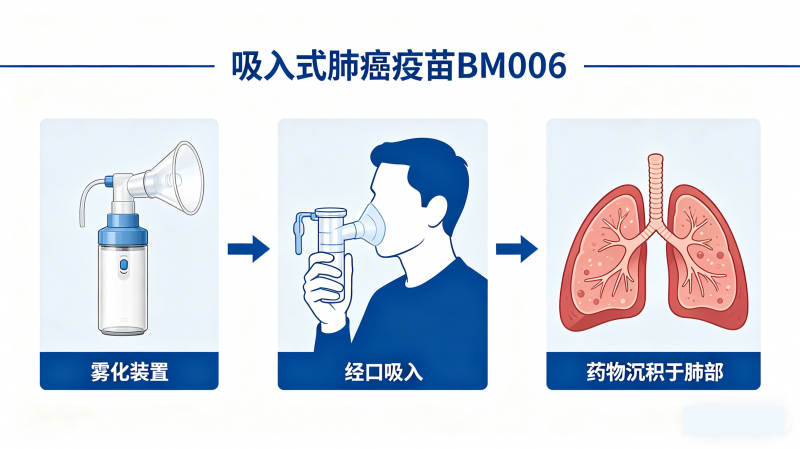
肺癌疫苗重大突破,晚期患者多了一个新的选
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

“手术成功”不等于万事大吉,新型癌症疫苗
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

2026年靶向治疗抗癌风暴,突破困境,普
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

2026年这些肺癌疫苗正悄然改变患者的生
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05






![[field:title/]](/uploads/allimg/20200224/1-2002241I5262J.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241I3461D.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H94LK.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241HKW34.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H619327.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H34H52.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H22IH.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241G93O18.jpg)




