3年无病生存率92.4%!FDA重磅授予T-DXd突破性疗法,精准狙击乳腺癌
2025年12月22日FDA授予德曲妥珠单抗(Enhertu、DS8201、优赫得、T-DXd、Trastuzumab deruxtecan、fam-trastuzumab deruxtecan-nxki)治疗乳腺癌突破性疗法
2025年12月22日,美国食品药品监督管理局(FDA)授予德曲妥珠单抗(T-DXd)突破性疗法认定,用于治疗新辅助治疗后乳腺和/或腋窝淋巴结仍有残留浸润性病灶、且疾病复发风险高的HER2阳性早期乳腺癌成人患者。
这是T-DXd斩获的第十项突破性疗法认定,不仅进一步巩固了其在乳腺癌治疗领域持续取得变革性成果的地位,随着突破性疗法认定的加持,T-DXd有望加速推进临床应用进程,更为那些面临高复发风险的HER2阳性早期乳腺癌患者带来更优的治疗选择。

▲截图源自“OncLive”
抗癌"导弹"曲妥珠单抗,智能杀伤HER2阳性肿瘤
人类表皮生长因子受体 2(HER2)阳性早期乳腺癌患者,若接受新辅助治疗后仍存在残留浸润性病灶,复发风险会显著升高。
而德曲妥珠单抗(Trastuzumab deruxtecan、fam-trastuzumab deruxtecan-nxki、T-DXd、Enhertu®、优赫得®、DS-8201)是阿斯利康研发的一款抗体偶联药物(ADC),巧妙地将靶向HER2的抗体与高效的细胞毒性药物连接在一起,可同时杀伤目标肿瘤细胞和邻近的肿瘤细胞。其作用机制就像一枚精准制导的“智能武器”,能够特异性地识别并结合HER2阳性的肿瘤细胞,然后将细胞毒性药物精准输送到肿瘤细胞内部,发挥强大的杀伤作用。这种靶向治疗的方式不仅能够更有效地杀死肿瘤细胞,还能减少对正常细胞的损伤,从而降低治疗的副作用。
T-DXd在高危HER2阳性乳腺癌中展现压倒性疗效优势,3年无侵袭性疾病生存率超92%
德曲妥珠单抗(T-DXd)突破性疗法认定,是基于2025年欧洲肿瘤内科学会(ESMO)大会公布的一项3期DESTINY-Breast05试验(NCT04622319)的关键数据,并同步发表于《新英格兰医学杂志》。
该研究共纳入1635例患者,将其分为两组:T-DXd组(818例)、T-DM1组(817例),截至数据截止日期,两组中位随访时间约为30个月。
核心疗效结果显示:T-DXd组3年无侵袭性疾病生存(IDFS)率高达92.4%(95%CI,89.7%-94.4%),显著优于T-DM1组的83.7%(95%CI,80.2%-86.7%),风险比(HR)为0.47(95%CI,0.34-0.66;P<0.0001,详见下图A);T-DXd组仅6.2%的患者发生侵袭性疾病事件或死亡,远低于T-DM1组的12.5%。
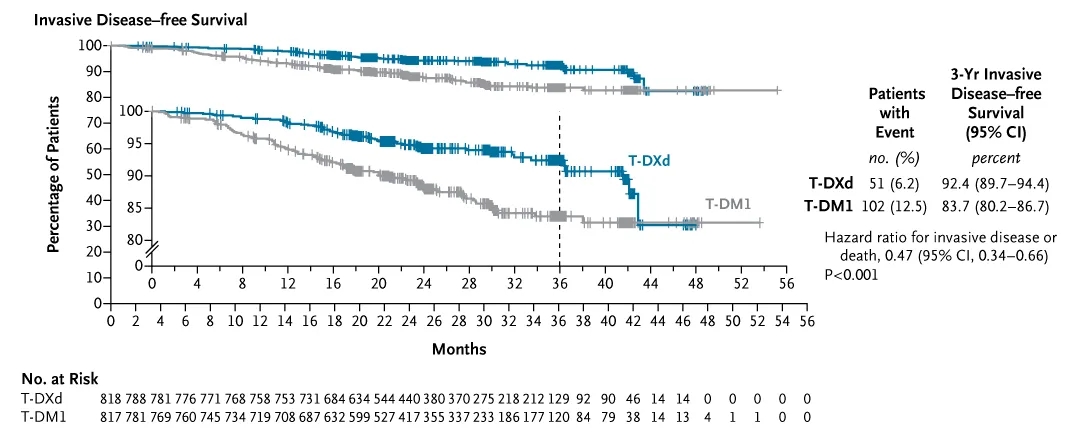
▲图源“N Engl J Med”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
关键次要终点方面,T-DXd组3年无病生存率为92.3%(89.5-94.3),优于T-DM1组的83.5%(79.9-86.4,详见下图B),风险比为0.47(95%CI,0.34-0.66;P<0.001),且仅6.4%的患者报告侵袭性疾病事件、非侵袭性疾病事件或死亡,低于T-DM1组的12.6%。
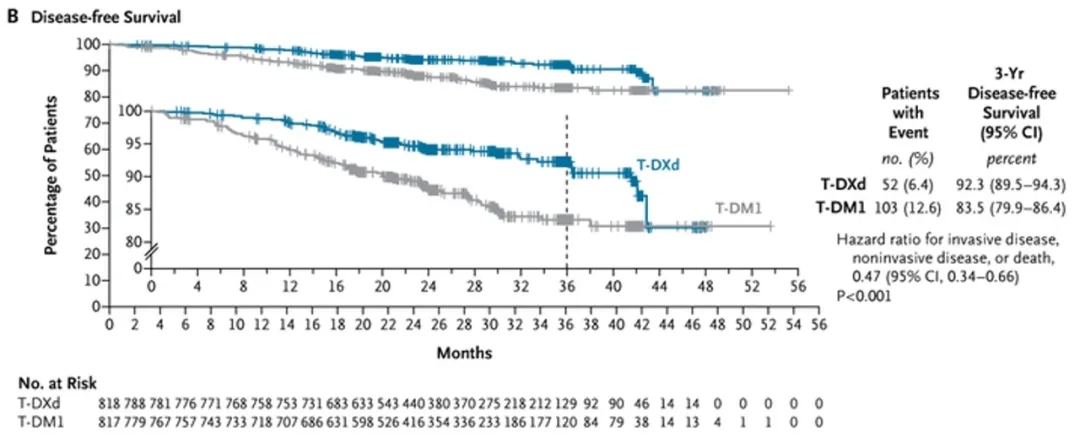
▲图源“N Engl J Med”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
综上,对于新辅助治疗后仍有残留浸润性病灶的高危HER2阳性乳腺癌患者,T-DXd方案较标准治疗T-DM1能显著提高无侵袭性疾病生存率,疗效优势明确。其毒性反应主要表现为胃肠道和血液系统毒性,虽存在间质性肺病这一重要风险,但通过适当的监测与管理可有效把控。
三大前沿疗法开启乳腺癌治疗新纪元
国内首个!异体NK细胞治疗复发性乳腺癌疗效显著优于自体,疾病控制率超83%
除了上文提到的抗癌新药外,还有多款针对乳腺癌的治疗新技术。近期,暨南大学研究团队开展了国内首个对比自体与同种异体NK细胞治疗复发性乳腺癌的临床研究(NCT02853903),该研究共入组36例经组织病理学确诊的复发性乳腺癌患者。
结果显示:按RECIST疗效评价标准分析,接受异体NK细胞治疗的Ⅱ组,临床疗效显著优于接受自体NK细胞治疗的Ⅰ组。Ⅱ组3例(16.67%)达部分缓解(PR)、12例(66.67%)达疾病稳定(SD),疾病控制率(DCR)高达83.34%;Ⅰ组仅1例(5.56%)达PR(P<0.05)、10例(55.56%)达SD(P>0.05)。初步结果显示,部分患者不仅肿瘤显著缩小,生活质量也得到明显提升。
值得一提的是,一位46岁复发性乳腺癌患者的治疗效果尤为亮眼。治疗前,其右乳可见8.0×3.8×5.7cm边界不清的软组织肿块(增强CT呈中度不均匀强化),腋窝伴多处肿大淋巴结,较大者约2.9×1.7×3.8cm;接受NK细胞治疗2个月后,右乳肿块缩小至6.8×3.5×5.8cm(呈轻度不均匀强化),腋窝较大肿大淋巴结也明显缩小(详见下图)。
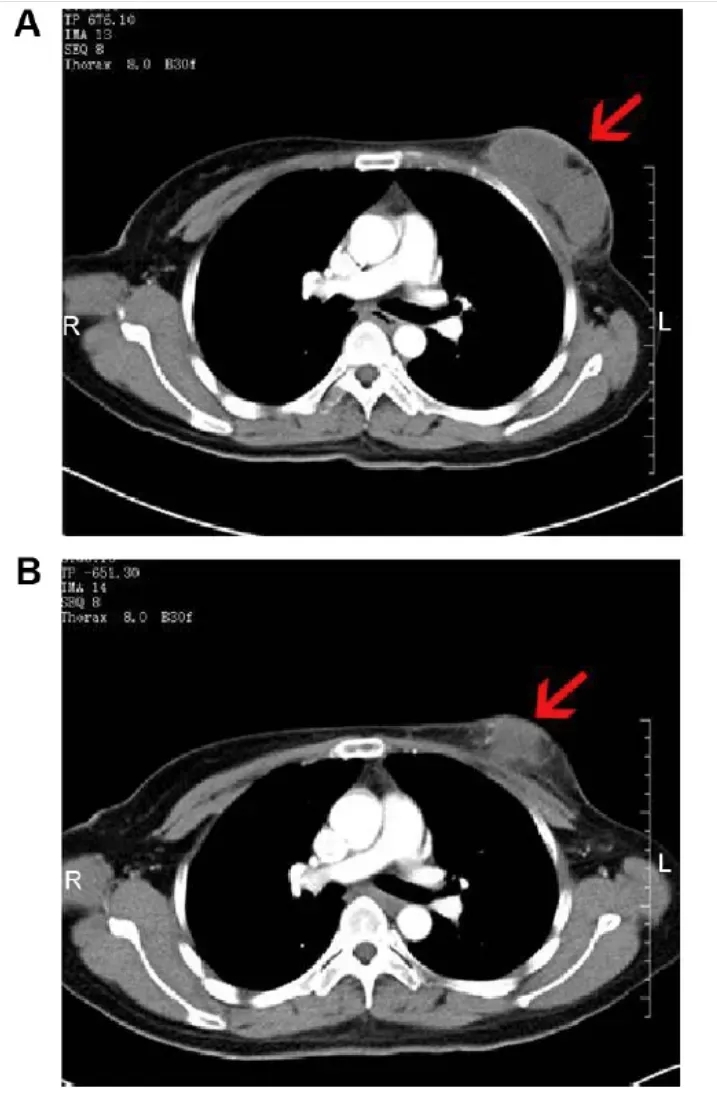
▲图源“Dovepress”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
全球首个!BNCT成难治复发性癌症治疗高精度新利器,精准杀癌不伤正常组织
硼中子俘获疗法(BNCT)是一种将中子束与硼药物结合的肿瘤选择性粒子放射疗法,能精准作用于细胞水平,已成为治疗难治性肿瘤的高精度、高效率方法,尤其在难治性和复发性癌症治疗领域展现出巨大潜力。其抗癌原理与传统放疗存在显著差异:传统放疗通过X射线或碳离子等强电离辐射束直接杀灭肿瘤细胞;而BNCT利用超热中子源,精准摧毁吸收了硼药物的肿瘤细胞,因所用辐射强度低于传统放疗,能最大程度减少对健康组织的损伤。
《Cureus》曾报道全球首个采用基于加速器的BNCT系统,治疗放疗后复发性乳腺癌的临床研究。其中一例52岁女性患者的治疗经历颇具参考价值:该患者10年前因右侧乳腺癌,先后接受化疗、保乳手术及25次共50Gy的保乳放疗;3年半前疾病局部复发,接受手术(rpT3N2M0)及化疗;后续虽又经历两次局部复发手术及激素治疗,癌症仍再次复发,最终接受BNCT治疗。
结果显示:在BNCT治疗后1天、7天、30天、60天、90天的CT扫描中,均未发现放射性肺炎迹象。下图3为该患者的肺部剂量分布及治疗后90天的CT扫描影像。
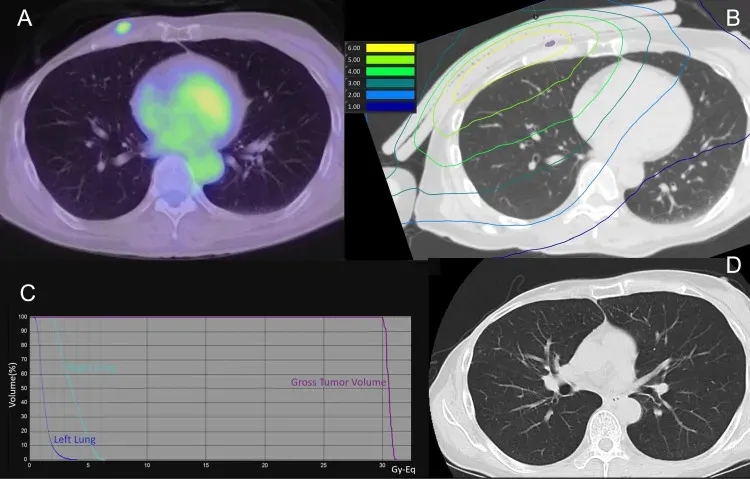
好消息是,日本近期已启动硼中子俘获疗法的临床研究,入组人群仅限不可切除的局部晚期或局部复发的头颈癌、乳腺癌成年患者等。感兴趣的癌友可将治疗经历、近期影像及病理学检查结果,提交至医学部,进行初步评估或了解详细入排标准。
益生菌成化疗"好帮手"!助乳腺癌患者症状缓解+体能提升
化疗是乳腺癌的主要治疗手段之一,但存在“无差别攻击”的局限——它不仅针对癌细胞,还可能损伤骨髓(造血功能)、毛囊、口腔、胃肠道及生殖系统等正常细胞,进而引发疲劳、感染、出血、脱发、胃肠道紊乱等副作用。严重时,这些副作用可能导致患者被迫中断治疗,最终影响生存率。因此,临床上迫切需要寻求补充替代疗法,以降低化疗相关风险。近年来,益生菌作为潜在替代疗法备受关注,这类由活微生物组成的制剂,在适当剂量下对癌症患者有益,尤其对乳腺癌细胞(MDA-MB-231)可产生抗增殖作用,有望减轻病情、改善患者预后。
2025年开展的一项研究进一步验证了益生菌的应用潜力。该研究旨在探究7种益生菌配方对化疗相关副作用的影响,同时评估患者的全血细胞计数、血液生物化学指标及卡氏体能评分,最终为多菌株益生菌补充剂缓解化疗副作用的潜在作用提供了初步证据,也为优化乳腺癌患者治疗方案提供了重要参考。研究共纳入28例接受化疗联合益生菌补充的乳腺癌患者。
结果显示:多菌株益生菌可有效缓解患者的疲劳与恶心症状。补充益生菌后,患者的卡氏体能评分显著提高,基线与干预后的中位数分别为90、100(p<0.001)。由此推测,疲劳、恶心等症状的改善,将进一步推动患者身体功能的持续恢复。血液生化检查结果亦显示,患者的血尿素氮(BUN)水平明显改善,基线与干预后的数值分别为11.6mg/dL、10.05mg/dL(p=0.008);若以高BUN水平患者为基线,益生菌补充对BUN水平的改善作用更为显著。

▲截图源自“PHARMACIA”
小编寄语
近年来,乳腺癌的治疗已经取得了长足的进展,逆转了晚期患者的生存期,除了上面整理的内容,还有更多的新药正在研发中。如果您对现有治疗方案不满意,或想了解乳腺癌更多抗癌新药/新技术的更多讯息,可将治疗经历、近期病理检查报告、出院小结等,提交至医学部,进行初步评估。
参考资料
[1]Loibl S,et al.DESTINY-Breast05 Trial Investigators. Trastuzumab Deruxtecan in Residual HER2-Positive Early Breast Cancer. N Engl J Med. 2025 Dec 10.
https://www.nejm.org/doi/full/10.1056/NEJMoa2514661
[2]Liang S,et al.Comparison of autogeneic and allogeneic natural killer cells immunotherapy on the clinical outcome of recurrent breast cancer. Onco Targets Ther. 2017 Aug 28;10:4273-4281.
https://www.dovepress.com/comparison-of-autogeneic-and-allogeneic-natural-killer-cells-immunothe-peer-reviewed-fulltext-article-OTT
[3]Kurosaki H,et al.The Effects of Boron Neutron Capture Therapy on the Lungs in Recurrent Breast Cancer Treatment. Cureus. 2024 Apr 1;16(4):e57417.
https://pmc.ncbi.nlm.nih.gov/articles/PMC11061820/
[4]Kirtishanti A,et al.Effect of multi-strain probiotics supplementation on chemotherapy-related side effects among patients with breast cancer: A pilot trial[J]. Pharmacia, 2025, 72: 1-9.
https://pharmacia.pensoft.net/article/144998/
[5]https://www.onclive.com/view/fda-gives-breakthrough-therapy-designation-to-post-neoadjuvant-t-dxd-for-her2-early-breast-cancer
扫描进患者病友群

肺癌|胃癌|肝癌|结直肠癌|胰腺癌
乳腺癌|脑瘤|淋巴瘤|儿童肿瘤等

相关推荐
实现33个月长生存!中国团队成功攻克&q
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

破解术后复发噩梦!NK细胞疗法让晚期胃癌
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

【胃癌CAR-T细胞疗法】IMC002注
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
晚期肺癌实现完全缓解!2026非小细胞肺
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

【淋巴瘤疫苗招募】WGc-043疫苗剑指
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

4个月婴儿确诊致命脑瘤被判死刑,革命性抗
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05







![[field:title/]](/uploads/allimg/20200224/1-2002241I5262J.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241I3461D.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H94LK.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241HKW34.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H619327.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H34H52.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H22IH.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241G93O18.jpg)




