重磅!2025首版商保创新药目录震撼发布,5款百万级CAR-T和9大抗癌药集体"入保"
重磅!2025年首版商保创新药目录震撼发布,5款百万级CAR-T和9大抗癌药集体“入保”
2025年12月7日,国家医保局正式发布《国家基本医疗保险、生育保险和工伤保险药品目录(2025年)》及首版《商业健康保险创新药品目录》,标志着中国医药支付迈入“双目录”互补新阶段,创新药准入效率显著提升。
值得一提的是,曾被称作“天价药物”的CAR-T疗法,此前因价格高昂多次无缘基本医保,此次5款申报的CAR-T疗法却悉数纳入商保目录,成为本次目录发布的一大重磅亮点!尽管具体协商价格暂未披露,但可以预见,2026年1月1日目录正式执行后,将显著降低患者自付比例,让这款百万级别的高价创新药不再遥不可及,为肿瘤患者带来全新治疗希望!
小编已第一时间汇总更新首版商保创新药目录中的CAR-T疗法信息,建议有需要的病友先收藏,方便及时查询适配药物(注:下列信息仅供参考,具体用药方案需遵循医嘱,也可联系医学部,进行初步评估)。
▲截图源自“NHSA”
五款CAR-T疗法全部纳入2025首版商保创新药品目录
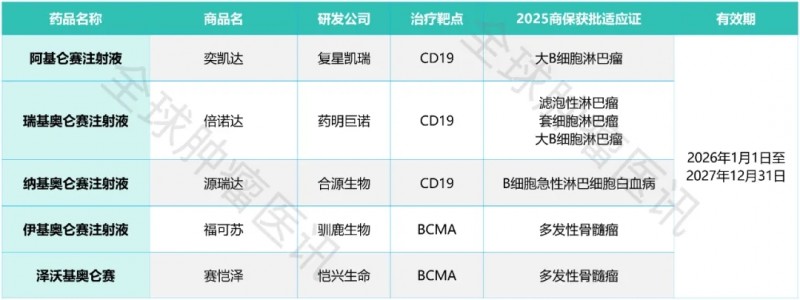
阿基仑赛注射液
1、药品简介
①药物名称:阿基仑赛注射液(axi-cel,FKC876,奕凯达®,Axicabtagene Ciloleucel Injection)。
②研发公司:复星凯瑞。
③治疗靶点:CD19。
2、2025商保获批适应证
1.一线免疫化疗无效或在一线免疫化疗后12个月内复发的成人大B细胞淋巴瘤(r/r LBCL)。本适应症为附条件批准上市,上市后将提供更多的有效性和安全性数据。
2.既往接受二线或以上系统性治疗后复发或难治性大B细胞淋巴瘤成人患者,包括弥漫性大B细胞淋巴瘤(DLBCL)非特指型(NOS),原发纵隔大B细胞淋巴瘤(PMBCL)、高级别B细胞淋巴瘤和滤泡性淋巴瘤转化的DLBCL。
3、药物详情
阿基仑赛注射液(axi-cel)是一款CD19 CAR-T产品,同时也是中国首个以药品途径批准上市的CAR-T细胞治疗产品。2021年6月22日在中国获批上市,用于治疗成人复发或难治性大B细胞淋巴瘤(r/r LBCL)。
根据ZUMA-12的2期临床研究(NCT03761056)数据显示:ORR率达82%,12个月时预计OS率达91%(95% CI,73–97,详见下图e),12个月时的PFS率为75%(95% CI,55–87,详见下图d)。
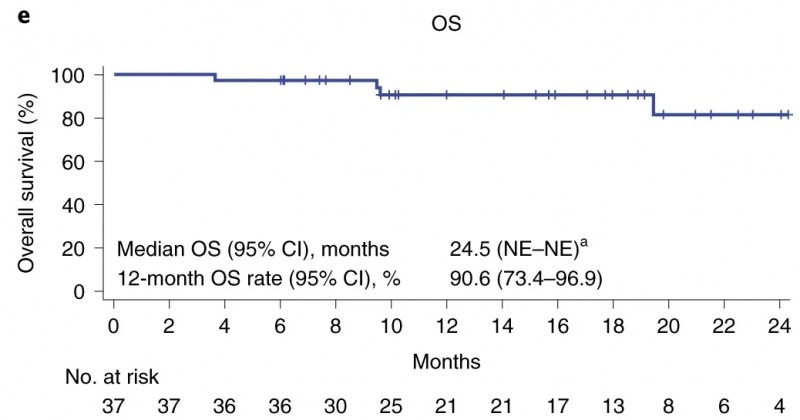

▲图源“nature”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
瑞基奥仑赛注射液
1、药品简介
①药物名称:瑞基奥仑赛注射液(relma-cel,倍诺达®,Carteyva®,relmacabtagene autoleucel)
②研发公司:药明巨诺。
③治疗靶点:CD19。
2、2025商保获批适应证
1.经过二线或以上系统性治疗后成人患者的复发或难治性大B细胞淋巴瘤,包括弥漫性大B细胞淋巴瘤非特指型、滤泡性淋巴瘤转化的弥漫性大B细胞淋巴瘤、3b级滤泡性淋巴瘤、原发纵隔大B细胞淋巴瘤、高级别B细胞淋巴瘤伴MYC和BCL-2和/或BCL-6重排(双打击/三打击淋巴瘤)。本品适应症为附条件批准上市,更多的有效性和安全性数据待上市后研究提供。
2.经过二线或以上系统性治疗的成人难治性或24个月内复发的滤泡性淋巴瘤,包括组织学分级为1、2、3a级的滤泡性淋巴瘤。本品适应症为附条件批准上市,更长时间的有效性数据待上市后研究提供;3.经过包括布鲁顿酪氨酸激酶抑制剂治疗在内的二线及以上系统性治疗的成人复发或难治性套细胞淋巴瘤。
3、药物详情
瑞基奥仑赛注射液(relma-cel)是我国首个靶向CD19的CAR-T细胞治疗产品,也是国内首款获批三项适应症的CAR-T疗法,其首个适应症为复发或难治性套细胞淋巴瘤(r/rMCL)。
该产品于2021年9月1日首次在中国获批上市,用于治疗既往经二线及以上系统性治疗后复发或难治性大B细胞淋巴瘤(r/r LBCL)。支持其上市的RELIANCE试验(NCT04089215),是中国首个实现符合上市许可标准的CAR-T细胞生产项目,同时获取了r/rLBCL患者的关键临床试验数据。结果显示:截至数据截止日,总体缓解率(BOR)达75.9%(95%CI,62.8–86.1),完全缓解(CR)率为51.7%(95%CI,38.2–65.1;详见下图)。
2025年6月4日,瑞基奥仑赛注射液的新药上市许可申请(NDA)获中国澳门药物监督管理局批准,新增三项适应症,分别为:经二线及以上系统性治疗的成人r/r LBCL;经二线及以上系统性治疗的成人难治性或24个月内复发的滤泡性淋巴瘤(r/r FL);经包括布鲁顿酪氨酸激酶抑制剂(BTKi)在内的二线及以上系统性治疗的成人复发或难治性套细胞淋巴瘤(r/r MCL)。
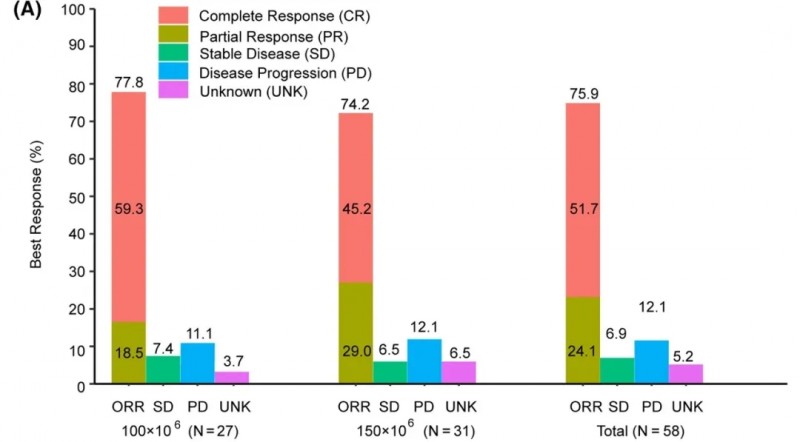
▲图源“Cancer Med”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
纳基奥仑赛注射液
1、药品简介
①药物名称:纳基奥仑赛注射液(源瑞达®,CNCT19细胞注射液,Inaticabtagene Autoleucel Injection)。
②研发公司:合源生物。
③治疗靶点:CD19。
2、2025商保获批适应证
适用于成人复发或难治性B细胞急性淋巴细胞白血病。
3、药物详情
纳基奥仑赛注射液(商品名:源瑞达®)是一款靶向CD19的CAR-T细胞治疗产品,更是我国首款用于治疗白血病的CAR-T产品。
该产品于2023年11月8日首次在中国获批上市,适应症为成人复发或难治性B细胞急性淋巴细胞白血病(r/r B-ALL)。其关键性临床试验(NCT04684147)数据亮眼:治疗3个月内总体缓解率(ORR)达82.1%。真实世界有效率更是高达92.8%,已被纳入国内权威诊疗指南。
2025年11月28日,该药第二项适应证的上市申请获国家药品监督管理局批准,用于经二线及以上系统性治疗后复发或难治性大B细胞淋巴瘤(r/r LBCL)的治疗,至此纳基奥仑赛成为了国内唯一覆盖白血病与淋巴瘤两大血液肿瘤领域的CAR-T疗法。该药联合高剂量化疗/自体干细胞移植治疗r/rLBCL的I/II期临床试验结果显示:最佳客观缓解率(ORR)达92.0%(95%CI:74.0%-99.0%),最佳完全缓解率(CR)为72.0%(95%CI:50.6%-87.9%,详见下图)。

▲图源“BMJ”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
伊基奥仑赛注射液
1、药品简介
①药物名称:伊基奥仑赛注射液(福可苏®,Equecabtagene Autoleucel Injection)。
②研发公司:驯鹿生物。
③治疗靶点:BCMA。
2、2025商保获批适应证
用于治疗复发或难治性多发性骨髓瘤成人患者,既往经过至少3线治疗后进展(至少使用过一种蛋白酶体抑制剂及免疫调节剂)。
3、药物详情
伊基奥仑赛注射液是一款全人源B细胞成熟抗原特异性CAR-T细胞,同时也是全球首款全人源BCMA靶向的CAR-T疗法,以及中国首款获批的BCMA CAR-T疗法!
2023年6月30日,获国家药品监督管理局(NMPA)批准上市,用于治疗复发/难治性多发性骨髓瘤(R/R MM)。1/2期临床研究数据显示,总体缓解率(ORR)高达96.0%!
泽沃基奥仑赛注射液
1、药品简介
①药物名称:泽沃基奥仑赛(zevor-cel,赛恺泽®,产品编号CT053,Zevorcabtagene Autoleucel)。
②研发公司:恺兴生命。
③治疗靶点:BCMA。
2、2025商保获批适应证
用于治疗复发或难治性多发性骨髓瘤成人患者,既往经过至少3线治疗后进展(至少使用过一种蛋白酶体抑制剂及免疫调节剂)。
3、药物详情
泽沃基奥仑赛是我国第五款获批的CAR-T产品,同时也是一款靶向BCMA的自体CAR-T细胞疗法。2024年3月1日,其新药上市申请获国家药品监督管理局(NMPA)批准,用于治疗既往接受过包括1种免疫调节剂、蛋白酶体抑制剂在内的至少3线治疗的成年复发或难治性多发性骨髓瘤患者。
此次获批主要依托中国LUMMICARSTUDY1Ⅰ/Ⅱ期临床试验(NCT03975907)的振奋数据:全部14例入组患者的总缓解率(ORR)高达100%,其中78.6%(11例)达到完全缓解(CR)或严格完全缓解(sCR),21.4%(3例)达到部分缓解(PR)。患者中位缓解持续时间(DOR)达24.1个月,中位无进展生存期(PFS)长达25.0个月(超2年),而达到sCR/CR的患者中位PFS更是延长至26.9个月(详见下图)。
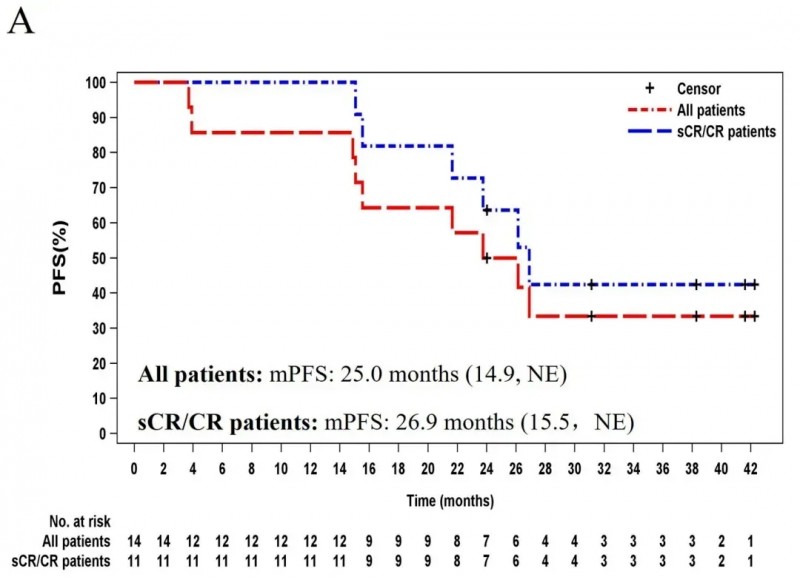
▲图源“ScienceDirect”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
其他九款纳入2025首版商保创新药品目录的抗癌药
告别"遥不可及"!普通家庭患者如何获取CAR-T疗法?国内多中心招募启动
面对疾病,最让人绝望的莫过于“有药难及”——要么无药可治,要么因天价费用望而却步。曾经,CAR-T这一前沿抗癌技术长期被医疗发达国家主导,不少国内病友在苦苦等待中错失治疗机会。
但如今,希望已照进现实!除经济条件优越的患者可选择已上市的CAR-T疗法外,国内外目前还有数百项CAR-T临床试验正在推进,并在国内多家知名癌症中心启动招募。目前已有众多经济条件有限的晚期患者,通过医学部成功申请入组,获得了更好的治疗机会!
在招项目(部分)
01、【C-CAR031】
1.药品名称:C-CAR031(靶向GPC3的装甲型CAR-T疗法)。
2.临床分期:Ⅰ期。
3、治疗线数:标准治疗失败。
4.突变基因:GPC3。
5.适合人群:GPC3阳性的晚期肺鳞癌患者。
02、【ECT204】
1.药品名称:ECT204(GPC3 自体T细胞疗法)。
2.临床分期:Ⅰ期;
3、治疗线数:二线治疗失败。
4.突变基因:GPC3。
5.适合人群:经免疫组化 (IHC)检测确定的肝细胞癌(HCC),肿瘤细胞存在 GPC3阳性表达。
03、【U16注射液】
1.药品名称:U16注射液(CAR-T细胞治疗产品)。
2.临床分期:Ⅰ期、Ⅱ期。
3.治疗线数:标准治疗失败。
4.突变基因:CD20。
5.适合人群:B细胞非霍奇金淋巴瘤。
04、【CT0596】
1.药品名称:CT0596(异基因BCMA/NKG2A双靶点通用型CAR-T)。
2.临床分期:Ⅳ期。
3.治疗线数:标准治疗失败。
4.突变基因:无靶点要求。
5.适合人群:复发/难治多发性骨髓瘤和浆细胞白血病。
申请流程
想申请CAR-T疗法的病友可将近期病理报告、基因检测报告等资料汇总后,提交至医学部,我们的专家将为您全面分析解读检测报告,预计一个工作日内电话联系推荐用药方案,并匹配适合患者入组的临床试验项目。注:作为国内权威的肿瘤患者服务平台,我们承诺对所有受试者的个人信息保密,并保证在整个过程中,遵循国家临床研究相关的法律法规。
小编寄语
CAR-T疗法作为免疫细胞疗法的标杆,其疗效有目共睹,近年来更是在实体瘤治疗领域更实现突破性进展。更大的好消息是,我国CAR-T疗法研发已进入蓬勃发展阶段,驯鹿医疗、科济生物、复星凯特、传奇生物等24家生物公司纷纷入局角逐。
但此前高昂的价格让不少患者望而却步,所幸我国近年持续推进抗癌药市场化改革,如今5款CAR-T疗法已全部纳入商保目录,将大幅减轻患者经济负担。我们更期待未来CAR-T疗法能进一步纳入医保,让更多癌症患者享受到这一前沿治疗的福音!
对于希望寻求CAR-T疗法帮助,或想通过临床试验获得免费治疗机会的患者,可将治疗经历、近期影像学及病理检查结果等资料,提交至医学部,获取2025年医保及商保创新药目录完整药物清单,或了解更多抗癌新药/新技术的入组标准,初步评估是否能通过方舟计划获得免费用药资格。
参考资料
[1]Neelapu S S,et al.Axicabtagene ciloleucel as first-line therapy in high-risk large B-cell lymphoma: the phase 2 ZUMA-12 trial[J]. Nature medicine, 2022, 28(4): 735-742.
https://www.nature.com/articles/s41591-022-01731-4
[2]Ying Z,et al.Relmacabtagene autoleucel (relma-cel) CD19 CAR-T therapy for adults with heavily pretreated relapsed/refractory large B-cell lymphoma in China. Cancer Med. 2021 Feb;10(3):999-1011.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7897944/
[3]Liu W,et al.Combinational therapy of CAR T-cell and HDT/ASCT demonstrates impressive clinical efficacy and improved CAR T-cell behavior in relapsed/refractory large B-cell lymphoma[J]. Journal for ImmunoTherapy of Cancer, 2024, 12(4): e008857.
https://jitc.bmj.com/content/12/4/e008857
[4]Fu C,et al.Three-Year Follow-up on Efficacy and Safety Results from Phase 1 Lummicar Study 1 of Zevorcabtagene Autoleucel in Chinese Patients with Relapsed or Refractory Multiple Myeloma[J]. Blood,2023, 142(Supplement 1): 4845-4845.
https://www.sciencedirect.com/science/article/abs/pii/S0006497123114467
扫描进患者病友群

肺癌|胃癌|肝癌|结直肠癌|胰腺癌
乳腺癌|脑瘤|淋巴瘤|儿童肿瘤等

相关推荐

“手术成功”不等于万事大吉,新型癌症疫苗
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

2026年靶向治疗抗癌风暴,突破困境,普
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

2026年这些肺癌疫苗正悄然改变患者的生
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
新一代NTRK基因融合突变靶向药TL11
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
实现33个月长生存!中国团队成功攻克&q
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

破解术后复发噩梦!NK细胞疗法让晚期胃癌
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05






![[field:title/]](/uploads/allimg/20200224/1-2002241I5262J.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241I3461D.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H94LK.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241HKW34.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H619327.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H34H52.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H22IH.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241G93O18.jpg)




