告别盲目抗癌!2026 NCCN指南重磅更新,13大癌种治疗大升级,难治性肺癌、肠癌等也有突破
2026年版NCCN指南重磅更新,13大癌种治疗大升级,难治性肺癌、肠癌等也有突破
美国国家综合癌症网络(NCCN)作为全球最具影响力的癌症指南平台之一,联合33家综合癌症中心共建肿瘤临床实践指南,对治疗方案的选择与排序、支持治疗规范及手术注意事项等核心环节提供系统性指导。
截至2025年12月,我们结合其他疾病领域最新指南版本,梳理了2026版NCCN指南的核心变革,重点汇总其对肺癌、结直肠癌、乳腺癌、肝癌、卵巢癌、膀胱癌、胃癌等癌种临床实践的影响(注:以上信息基于同期发布的2026 NCCN指南,后续可能有补充更新,部分未成熟临床试验数据及未来潜在更新暂未纳入)。
▲截图源自“OncLive”
2025~2026版NCCN指南十三大癌种的核心变革
2026版NCCN指南最深刻的变革,核心在于完成了从“基于经验”到“基于分子”的诊疗模式跨越。检测技术的全面升级、治疗方案的精准分层与多学科协作(MDT)的制度化,共同确立了肿瘤精准医疗的全新标准,助力更多患者获得个性化治疗,提升生存率、改善生活质量,标志着肿瘤治疗正式迈入更精准、高效的全新阶段。不同癌种的2025-2026年NCCN多癌种指南核心变革如下:
非小细胞肺癌(2026版NCCN指南1.2026)
1、德达博妥单抗(Dato-DXd,Datopotamab deruxtecan-dlnk,Datroway)治疗地位明确:作为首个针对EGFR突变患者的TROP-2ADC药物,其客观缓解率达45%,被新增为EGFR突变型NSCLC患者的优选治疗方案——在奥希替尼联合化疗一线治疗进展后的二线首选,同时列为其他一线方案进展后的三线首选;此外,也适用于携带EGFR19号外显子缺失、L858R突变、EGFRS768/L861Q/G79X突变及20号外显子插入突变患者的后续治疗。
2、一线治疗方案升级:奥希替尼联合卡铂或顺铂/培美曲塞,以及阿米万他单抗-vmjw(Rybrevant)+拉泽替尼(Lazcluze),从“其他推荐”升至1类首选,适用于一线全身治疗前已明确EGFR突变的NSCLC患者;拉泽替尼在特定场景下对该方案仍有效。
3、后续治疗补充:对于EGFR19号外显子缺失或21号外显子L858R突变、奥希替尼治疗后出现多发病灶且未接受过相关治疗的NSCLC患者,阿米万他单抗联合拉泽替尼被纳入“在某些情况下有用”的后续治疗类别。
4、围手术期治疗规范:所有可切除IB–IIIB期患者,术前需强制检测PD-L1、EGFR、ALK;若PD-L1≥1%且无驱动突变,优先采用“纳武利尤单抗+含铂双药”新辅助方案;术后病理未达病理完全缓解(pCR)者,可继续接受一年辅助免疫维持治疗。
5、晚期患者治疗禁忌明确:对EGFR/ALK/RET/ROS1阳性的晚期NSCLC患者,指南首次以脚注明确“PD-1/PD-L1抑制剂单药疗效有限,不推荐使用”,将该类靶向阳性人群列为免疫单药治疗禁忌。
小细胞肺癌(2026年第2版)
1、对于广泛期SCLC患者,在卡铂+依托泊苷+阿特珠单抗(Tecentriq)诱导治疗后,鲁比替定(Zepzelca)联合阿特珠单抗为推荐维持治疗方案。
2、若患者经4周期诱导化疗联合免疫治疗后,病情至少稳定、ECOG体能状态评分为0或1,且无脑病转移史,可在维持治疗的阿特珠单抗中加用鲁比替定。
胃癌(2025年第3版)
1、所有新确诊患者:建议常规开展PD-L1检测。
2、对于PD-L1联合阳性评分(CPS)或肿瘤面积比例(TAP)评分≥1的患者,FLOT方案联合度伐利尤单抗(Imfinzi)被列为围手术期全身治疗1类首选方案。
3、对于HER2过表达阴性患者,氟尿嘧啶+奥沙利铂+替雷利珠单抗-jsgr(Tevimbra)被列为的一线治疗中1类推荐方案。
4、对于NTRK基因融合阳性患者,恩曲替尼、拉罗替尼或瑞波替尼被列为一线系统治疗2B类选择。
肝癌(2025年第2版)
1、一线全身治疗新增:纳武利尤单抗(Opdivo)联合伊匹木单抗(Yervoy),被列为2A类推荐方案。
2、治疗方案调整:乐伐替尼(Lenvima)、索拉非尼(Nexavar)已从后续系统治疗中移除;疾病进展后,纳武利尤单抗联合伊匹木单抗+帕博利珠单抗(Keytruda),从其他推荐后续治疗方案中移除。
3、NTRK基因融合阳性患者治疗更新:瑞波替尼(Augtyro)从原2B类推荐中移除后,与恩曲替尼(Rozlytrek)、拉罗替尼(Vitrakvi)共同列为2A类推荐药物,用于NTRK基因融合阳性肿瘤的治疗。
直肠癌(2025年第4版)
2025年第4版NCCN直肠癌指南核心修订要点:对于错配修复功能正常(pMMR)/微卫星稳定(MSS)、仅发生肝脏和/或肺部转移且疾病可切除的直肠癌患者,可将FOLFIRINOX(亚叶酸+5-氟尿嘧啶+伊立替康+奥沙利铂)化疗,作为新辅助治疗方案。
结肠癌(2025年第5版)
1、错配修复缺陷(dMMR)/微卫星不稳定性高(MSI-H)患者治疗调整:
①低风险III期疾病可考虑辅助全身治疗。
②基于ATOMIC3期试验(NCT02912559)数据,阿特珠单抗联合FOLFOX[亚叶酸钙+5-氟尿嘧啶(5-FU)+奥沙利铂]或CAPOX(卡培他滨+奥沙利铂),已被列为低危/高危III期dMMR/MSI-H患者辅助治疗的2A类首选方案,标志着免疫检查点抑制剂疗法在患者治疗早期阶段即可应用。
③原2A类推荐的卡培他滨、5-FU,调整为该人群的2B类推荐。
2、晚期/转移性疾病治疗新增:基于BREAKWATER3期试验(NCT04607421)数据,FOLFOX联合恩考非尼(Braftovi)+西妥昔单抗(Erbitux)或帕尼单抗(Vectibix),成为BRAFV600E突变转移性结直肠癌的一线治疗方案,为预后通常较差的该患者群体带来更优疗效。
乳腺癌(2025年第5版)
1、对于激素受体(HR)阳性、HER2阴性且携带ESR1突变的复发性不可切除或IV期患者,Imlunestrant(Inluriyo)被列为2A类其他推荐方案,适用于一线或后续治疗。
2、对于HR阳性、HER2阳性的复发性不可切除或IV期患者,Abemaciclib(Verzenio)+氟维司群(Faslodex)+曲妥珠单抗(Herceptin)被列为2B类推荐方案。
3、对于携带HER2激活突变的IV期(M1)患者,奈拉替尼(Nerlynx)联合或不联合曲妥珠单抗(Herceptin)/氟维司群(Faslodex),被列为2A类推荐方案(部分场景适用)。
4、对于携带FGFR1/2/3融合或突变的IV期(M1)患者,Erdafitinib(Balversa)被列为2A类推荐方案(部分场景适用)。
卵巢癌(含输卵管癌、原发性腹膜癌,2025年第3版)
1、对于初始治疗未接受贝伐珠单抗(Avastin)的BRCA1/2野生型、同源重组缺陷型患者,奥拉帕尼(Lynparza)维持治疗被列为2B类推荐。
2、对于KRAS突变的低级别浆液性癌患者,部分场景下可选用Avutometinib+defactinib(Avmapki Fakzynja)治疗。
3、2025年版指南基于长期随访数据及FDA新适应症,更新了PARP抑制剂用于晚期卵巢癌一线维持治疗的适应症;同时新增铂敏感/耐药复发性卵巢癌治疗方案,包括mirvetuximab soravtansine-gynx(Elahere)、T-DXd、avutometinib/defactinib及FOLFIRI±贝伐珠单抗。这些更新体现了对不同类型卵巢癌分子特征的深入认知,助力精准靶向治疗的个体化实施。
膀胱癌(2025年第2版)
1、部分对BCG无反应或不耐受的患者,吉西他滨膀胱内灌注系统被列为治疗选择。
2、转移性疾病治疗调整:
①恩福妥单抗-维多汀-ejfv(Padcev)+帕博利珠单抗列为一线首选方案(疗效优于传统铂类化疗),铂类化疗转为二线。
②建议所有患者进行基因组检测,以匹配靶向治疗,如HER2阳性患者可选T-DXd;FGFR3突变患者可选厄达替尼(Balversa)。
关于肿瘤基因检测
癌症本质是基因病,每个肿瘤细胞都携带独特的突变“指纹”。而肿瘤基因检测(又称基因组检测、肿瘤DNA测序、生物标志物检测),是一种通过分析个体基因序列、检测肿瘤相关基因突变,识别可能增加癌症患病风险的特定遗传变化的生物医学技术。它能助力更早发现肿瘤,为针对性预防或治疗提供支撑,核心作用包括明确肿瘤诊断、指导靶向药物与免疫治疗、监测治疗效果、评估肿瘤预后,同时还关系到部分抗癌药物的报销资格。
作为医学领域的重要技术,肿瘤基因检测为肿瘤的预防、诊断与治疗带来了新的希望,更是精准诊治不可或缺的基石,也是实现个体化精准治疗的必经之路。其价值早已超越“找药”的单一功能,不仅能为后续治疗方案制定提供关键指导,更能为患者保留与未来新疗法接轨的可能——每一份突变记录,都有望在医学技术突破时成为战胜癌症的关键突破口!
▼需要/无需进行基因检测的癌种及靶向药一览表


好消息是,目前我国部分省市(如北京、福建、山东、吉林等)已将基因检测项目纳入医保范畴,大大减轻了肿瘤患者的负担。此外,我们目前发起的方舟援助计划,针对符合条件的患者可给予1000-3000援助金,想申请的患者可致电医学部,了解检测详情或进行申请。
急性髓系白血病(AML,2026年第3版)
1、对于NPM1突变的复发性/难治性AML患者,Ziftomenib(Komzifti)被列为2A类推荐方案。
2、符合强化诱导条件的患者,新增2B类方案:CLIA(克拉屈滨+伊达比星+阿糖胞苷)+维奈托克,以及FLAG-IDA(氟达拉滨+阿糖胞苷+粒细胞集落刺激因子+伊达比星)+维奈托克。
3、不符合首选方案及ivosidenib(Tibsovo)治疗条件的患者,将Olutasidenib(Rezlidhia)列为2B类推荐方案。
4、对于复发/难治性患者,新增靶向治疗药物Revumenib(Revuforj)。
5、阿糖胞苷为基础的诱导治疗后,随访及再诱导治疗新增阿扎胞苷/地西他滨+维奈托克,作为第6种治疗方案。
多发性骨髓瘤(2026年第4版)
1、接受过2种先前疗法(含蛋白酶体抑制剂PI+免疫调节药物IMiD)的患者,玛贝妥单抗(Belantamab Mafodotin,Blenrep®)+硼替佐米(Velcade)+地塞米松,被列为1类其他推荐方案。
2、接受过4线治疗(含抗CD38单克隆抗体+PI+IMiD)的预处理患者,新增Linvoseltamab-gcpt(Lynozyfic)作为治疗选择。
3、适合造血干细胞移植(HCT)的初诊患者:
①艾沙妥昔单抗(Isatuximab,Sarclisa)+硼替佐米+来那度胺(Revlimid)+地塞米松列为1类首选方案。
②达雷妥尤单抗(Daratumumab,Darzalex)isatuximab,均与carfilzomib(Kyprolis)、lenalidomide+dexamethasone联合使用已从推荐中移除;部分场景可考虑达雷妥尤单抗维持治疗。
4、年龄<80岁且HCT推迟/不适用的患者,达雷妥尤单抗+硼替佐米+来那度胺+地塞米松,列为1类首选方案。
5、伊沙妥昔单抗+来那度胺+地塞米松,以及硼替佐米+来那度胺+地塞米松均被列为1类其他推荐方案。
6、部分场景下,伊沙佐米+来那度胺+地塞米松方案适用。
7、复发/难治性患者:BCMA靶向CAR-T(如Cilta-cel、Ide-cel)有望成为关键治疗选项。
慢性淋巴细胞白血病(CLL)/小淋巴细胞淋巴瘤(SLL,2026年第1版)
Richter转化患者治疗新增多项2A类推荐方案:
1、维奈克拉(Venetoclax,Venclexta)+阿替利珠单抗+奥滨尤妥珠单抗(Gazyva)。
2、Epcoritamab-bysp(Epkinly)、格菲妥单抗(Glofitamab,Columvi®、高罗华®)。
3、两款CAR-T细胞疗法:Axicabtagene ciloleucel(axi-cel;Yescarta)、tisagenlecleucel(tisa-cel;Kymriah)。
B细胞淋巴瘤(2025年第3版)
1、对于至少接受过1次含抗CD20单克隆抗体全身治疗的患者,Tafasitamab-crix(Monjuvi)+来那度胺+利妥昔单抗(Rituxan)列为二线2A类首选方案。
2、三线及后续治疗:Loncastuximab tesirine-lpyl(Zynlonta)+利妥昔单抗列为2B类方案;Glofitamab列为2B类二线及后续治疗药物。
3、对于需温和诱导治疗的患者,Acalabrutinib(Calquence)+苯达莫司汀+利妥昔单抗列为一线2A类首选方案。
4、对于不适合CAR-T治疗的复发/难治性患者,Epcoritamab+吉西他滨+奥沙利铂列为首选方案。
5、在复发/难治性大B细胞淋巴瘤、高级别B细胞淋巴瘤、滤泡性淋巴瘤等癌种中,CAR-T治疗(如Axi-cel、Tisa-cel、Liso-cel)的二线或后线治疗地位进一步巩固。
▼中美已获批上市的CAR-T疗法汇总(截至2025年11月)


2026版NCCN指南免疫细胞治疗与癌症疫苗突破性更新
截至2025年底发布的2026.V1版NCCN指南,在免疫细胞治疗、癌症疫苗领域实现“颠覆性”升级,核心逻辑可概括为:免疫治疗地位前移且管理精细化、癌症疫苗预留临床转化通道,二者协同搭建肿瘤全周期精准管理框架。以下为两大板块的核心更新:
免疫细胞治疗:独立化管理+场景拓展,疗效与安全性双提升
2026版NCCN指南对免疫细胞治疗的调整聚焦“专业化细分”与“全流程规范”,核心突破体现在三方面:
01、CAR-T治疗:独立指南落地,治疗线级前移
指南首次将CAR-T与淋巴细胞衔接器相关毒性管理从原免疫治疗指南中剥离,发布独立的《CAR-T细胞与淋巴细胞衔接器相关毒性管理指南(V1.2026)》,明确患者筛选、输注前评估、长期随访的全流程路径,凸显该疗法的独特性与临床重视度。
基于ZUMA-7、TRANSFORM等III期试验结果,CAR-T极有可能成为部分高危大B细胞淋巴瘤患者的标准二线治疗(突破原三线及以上限制);若GPRC5D靶向CAR-T获批,将同步纳入多发性骨髓瘤指南。
02、NK/CAR-NK细胞:血液肿瘤疗效显著,实体瘤探索中
在血液肿瘤领域取得关键进展,新型产品FT596、NKX019预计2026-2027年上市。
其中,FT596作为一款iPSC衍生CD19定向CAR-NK细胞,其I期首次人体试验(NCT04245722)结果显示:68例复发/难治性B细胞淋巴瘤患者联合治疗后,客观缓解率(ORR)达54%,完全缓解(CR)率37%;滤泡性淋巴瘤亚组(n=13)ORR更是达到100%,中位缓解持续时间为16.9个月。大B细胞淋巴瘤(LBCL,n=32)亚组客观缓解率(ORR)达38%(12/32),完全缓解率(CR)为25%。
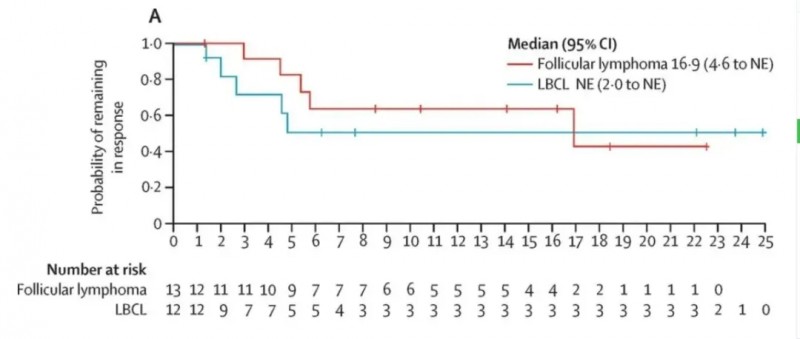
▲图源“Lancet”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
03、肿瘤浸润淋巴细胞(TIL):实体瘤探索加速,NSCLC适应症可期
黑色素瘤治疗地位进一步巩固,非小细胞肺癌(NSCLC)等实体瘤研究快速推进。
2025年11月,Iovance官网披露II期IOV-LUN-202试验(NCT04614103)中期数据显示:39例既往接受过治疗的晚期非鳞状NSCLC患者,接受Lifileucel(TIL疗法)单药治疗后,按RECISTv1.1标准,客观缓解率(ORR)达25.6%(含2例CR、7例PR),疾病控制率(DCR)更是高达71.8%。其中完全缓解(CR)2例、部分缓解(PR)7例(详见下图)。经25.4个月随访,中位缓解持续时间未达,较标准治疗多西他赛展现出更优的疗效持久性。该试验预计2026年出最终结果,Lifileucel有望2027年获批用于非鳞NSCLC。
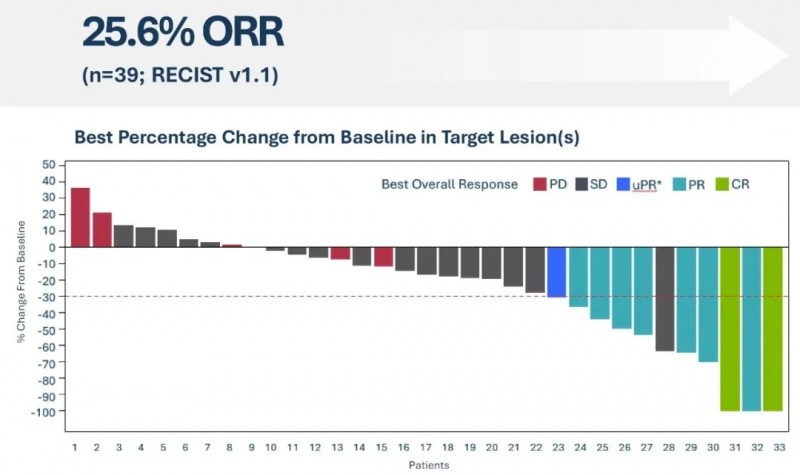
▲图源“Iovance”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
癌症疫苗:未入常规推荐,临床试验通道提前开放
2026.V1版全瘤种指南暂未将任何治疗性癌症疫苗列为标准治疗,但通过新增临床试验推荐、细化研究方向,为未来临床转化预留空间:
01、全瘤种统一引导:鼓励疫苗联合免疫治疗试验
指南在“系统性治疗”章节新增共同脚注,明确“鼓励符合条件的患者参与新抗原疫苗、HPV治疗性疫苗±免疫检查点抑制剂的临床试验”,为二者联合应用提供方向指引。
02、mRNA肿瘤疫苗:个性化与广谱并行,疗效数据亮眼
1.广谱疫苗:BNT113(针对HPV16阳性头颈鳞癌)进入II/III期试验;肺癌预防性疫苗LungVax将于2026年启动I期临床。
2.个性化新抗原疫苗mRNA-4157(V940):在黑色素瘤III期试验中持续招募,与PD-1抑制剂联合可显著降低高危患者复发风险,预计2026-2029年提交监管审批。2023ASCO大会公布的IIb期临床试验(KEYNOTE-942)结果显示:联合派姆单抗治疗高危III/IV期黑色素瘤,可将患者远处转移或死亡风险降低62%,18个月无复发生存(RFS)率达78.6%(单药组为62.2%),18个月无远处转移生存期(DMFS)率为91.8%,单药治疗组仅为76.8%。
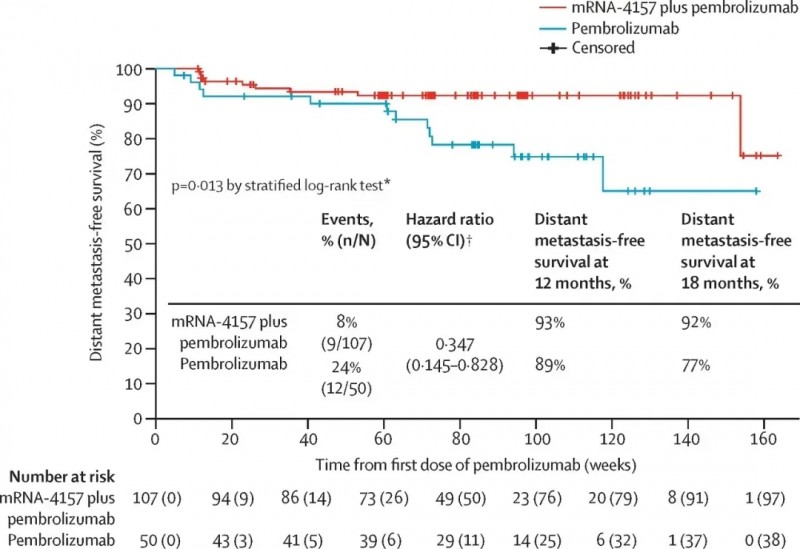
▲图源“Lancet”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
03、树突状细胞(DC)疫苗:联合治疗显效,案例证实长期获益
凭借强大抗原呈递能力激活肿瘤特异性T细胞,与免疫检查点抑制剂联合显示协同效应,部分临床试验证实可延长晚期实体瘤患者生存期。
《Cureus》报道的案例显示,WT1/MUC1肽脉冲树突状细胞(DC)联合CD3激活T淋巴细胞(CAT)的过继细胞疗法(ACT),成功实现晚期十二指肠癌患者长期疾病控制——截至首次给药后54个月,肿瘤无复发进展。
治疗前后变化显著:治疗前,腹部CT可见十二指肠周围大网膜明显扩张(详见下图A箭头所示),且存在大量恶性腹水(详见下图B、C)。
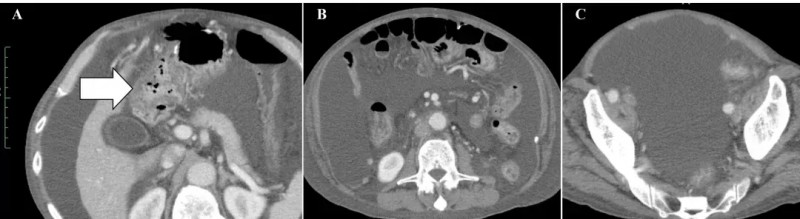
▲图源“Cureus”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
完成8次治疗后1个月,患者症状与影像学表现均大幅改善:恶性腹水完全消退,腹胀、腿部水肿消失,食欲恢复,原发病灶及转移性淋巴结持续缩小,腹膜播散的影像学特征已不明显,腹腔内大网膜(脂肪性粘稠组织)消失(详见下图A),仅右侧腹股沟疝因既往大量腹水导致的腹压影响仍持续存在(详见下图C)。此外,治疗无严重不良反应,患者恢复正常活动,截至首次给药后54个月仍无复发。

▲图源“Cureus”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
04、其他:靶向突变疫苗持续探索
KRAS突变肽疫苗ELI-002 7P(覆盖七种常见突变)、WT1-mRNA/DC疫苗等在多种晚期实体瘤中开展评估,可诱导持久抗肿瘤免疫。其中,ELI-002的I期AMPLIFY-201临床试验(NCT05726864)显示,23例可评估患者中77%肿瘤标志物减少,6例达到完全缓解,25例患者中位总生存期16.33个月(详见下图)。
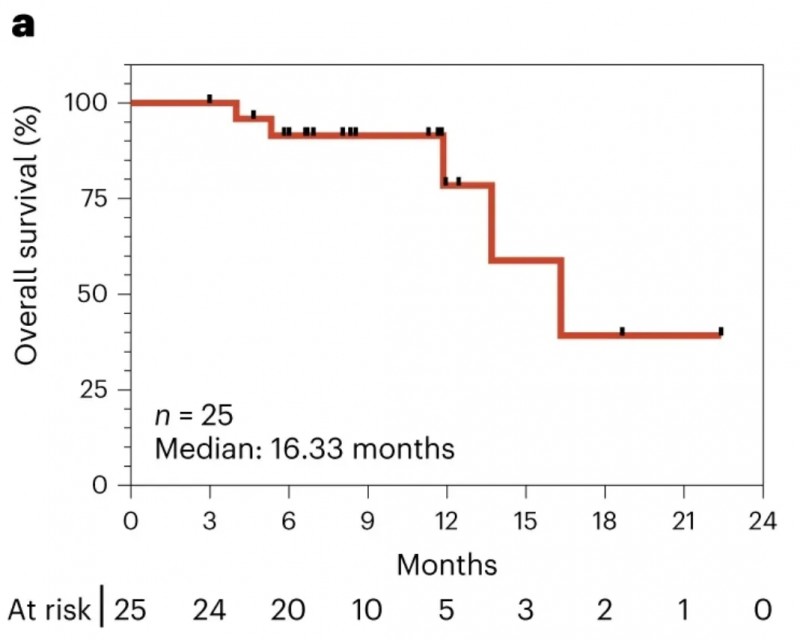
▲图源“nature medicine”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
小编寄语
2026版NCCN指南通过免疫细胞治疗的独立化管理、癌症疫苗的临床试验通道预留,结合基因检测“DNA+RNA+蛋白”全景化升级,构建起“检测-治疗-探索”的完整精准医疗链条。免疫细胞治疗的精细化毒性管理提升了安全性与可及性,癌症疫苗虽暂未落地常规治疗,但临床试验的定向引导为未来突破奠定基础,二者均以基因检测为核心支撑,共同推动肿瘤治疗从“经验医学”向“精准医学”深度转型。
但需提醒广大病友,癌症作为一种高度突变且极度狡猾的疾病,目前很难仅依靠单一疗法,达到预期治疗效果。现阶段理想的抗癌治疗,是依托于权威医院和权威专家的早期规范诊断,并在传统治疗(入手术、放化疗)的基础上,根据患者自身情况、疾病特点、经济状况等,辅以免疫细胞疗法(如CAR-T、TCR-T、TIL、NK、CAR-NK细胞疗法)、癌症疫苗、靶向药物、硼中子俘获疗法、质子治疗等抗癌新药/新技术,以预防癌症复发或转移、尽可能延长生存期、提高患者的生存质量。
对现阶段治疗方案不满意的患者,可将近期影像及病理检查报告、治疗经历等,提交至医学部,详细评估病情,或申请国内外抗癌专家会诊,寻求抗癌新药/新技术的帮助。
参考资料
[1]Ghobadi A,et al.Induced pluripotent stem-cell-derived CD19-directed chimeric antigen receptor natural killer cells in B-cell lymphoma: a phase 1, first-in-human trial[J]. The Lancet, 2025, 405(10473): 127-136.
https://www.thelancet.com/journals/lancet/article/PIIS0140-6736(24)02462-0/abstract
[2]https://www.globenewswire.com/news-release/2025/11/03/3179067/0/en/Iovance-Biotherapeutics-Reports-Potential-Best-in-Class-Clinical-Data-for-Lifileucel-TIL-Cell-Therapy-in-Advanced-Non-Small-Cell-Lung-Cancer-NSCLC.html
[3]Weber J S,et al.Individualised neoantigen therapy mRNA-4157 (V940) plus pembrolizumab versus pembrolizumab monotherapy in resected melanoma (KEYNOTE-942): a randomised, phase 2b study[J]. The Lancet, 2024, 403(10427): 632-644.
https://www.thelancet.com/journals/lancet/article/PIIS0140-6736(23)02268-7/abstract
[4]Yagawa Y,et al.Peritoneal Dissemination and Malignant Ascites in Duodenal Cancer Successfully Treated With Adoptive Cell Therapy Using WT1-and MUC1-Pulsed Dendritic Cells and Activated T Cells With No Adverse Effects: A Case Report[J]. Cureus, 2024, 16(11).
https://www.cureus.com/articles/308954-peritoneal-dissemination-and-malignant-ascites-in-duodenal-cancer-successfully-treated-with-adoptive-cell-therapy-using-wt1--and-muc1-pulsed-dendritic-cells-and-activated-t-cells-with-no-adverse-effects-a-case-report#!/
[5]Pant S,et al.Lymph-node-targeted, mKRAS-specific amphiphile vaccine in pancreatic and colorectal cancer: the phase 1 AMPLIFY-201 trial[J].Nature medicine,2024:1-12.
https://www.nature.com/articles/s41591-023-02760-3
[6]https://www.onclive.com/view/experts-unpack-the-most-notable-nccn-guideline-changes-heading-into-2026
扫描进患者病友群

肺癌|胃癌|肝癌|结直肠癌|胰腺癌
乳腺癌|脑瘤|淋巴瘤|儿童肿瘤等

相关推荐

“手术成功”不等于万事大吉,新型癌症疫苗
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

2026年靶向治疗抗癌风暴,突破困境,普
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

2026年这些肺癌疫苗正悄然改变患者的生
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
新一代NTRK基因融合突变靶向药TL11
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
实现33个月长生存!中国团队成功攻克&q
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

破解术后复发噩梦!NK细胞疗法让晚期胃癌
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05






![[field:title/]](/uploads/allimg/20200224/1-2002241I5262J.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241I3461D.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H94LK.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241HKW34.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H619327.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H34H52.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H22IH.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241G93O18.jpg)




