铂耐药卵巢癌迎新药!Relacorilant提交欧盟上市申请,1年无进展生存率提升12%!
2025年10月14日铂耐药卵巢癌新药Relacorilant向欧盟提交上市申请,1年无进展生存率提升12%
2025年10月14日,Corcept Therapeutics Incorporated公告称,已向欧洲药品管理局提交relacorilant用于治疗铂类耐药性卵巢癌患者的上市许可申请(MAA)。
与单独使用白蛋白结合型紫杉醇相比,relacorilant联合该药物治疗,能显著改善铂类耐药性卵巢癌患者的无进展生存期(PFS)与总生存期(OS),还可将疾病进展风险降低30%。
若此次申请顺利获批,relacorilant有望重新定义铂类耐药性卵巢癌的治疗格局,为这类患者带来全新治疗选择。

▲截图源自“OncLive”
卵巢癌多线治疗迎突破!Relacorilant口服疗法获FDA审查
Relacorilant是Corcept Therapeutics公司研发的口服选择性糖皮质激素受体(GR)拮抗剂(SGRA),其通过特异性结合GR调节皮质醇活性,且不作用于其他激素受体,进而增强肿瘤对化疗诱导细胞凋亡的敏感性,目前正针对卵巢癌、前列腺癌等适应症开展开发。
除了刚刚获得欧盟批准外,美国食品药品监督管理局(FDA)目前正审查relacorilant的新药申请(NDA),其审查决定预计将在2026年7月欧洲药品管理局(EMA)接收该药物上市授权申请后做出。
Relacorilant联合疗法3期数据两眼:卵巢癌12个月PFS率比单药高12%,中位总生存近16个月、ORR近37%
Relacorilant的新药申请(NDA)获关键性3期ROSELLA试验(NCT05257408)积极数据支持。该研究纳入381例既往接受过紫杉烷类和贝伐单抗治疗(其中61%曾接受PARP抑制剂治疗)的女性患者,随机分为两组:联合治疗组(relacorilant+白蛋白结合型紫杉醇,n=188)、白蛋白结合型紫杉醇单药组(n=193)。
结果显示:联合治疗组疗效显著优于单药组:中位无进展生存期(PFS)延长至6.54个月(95%CI,5.55-7.43),而单药组PFS仅为5.52个月(95%CI,3.94-5.88)(HR=0.70,P=0.0076),且PFS率也更高,6个月PFS率分别为52%(联合治疗组)vs 42%(单药治疗组),12个月PFS率分别为25%(联合治疗组)vs 13%(单药治疗组)。
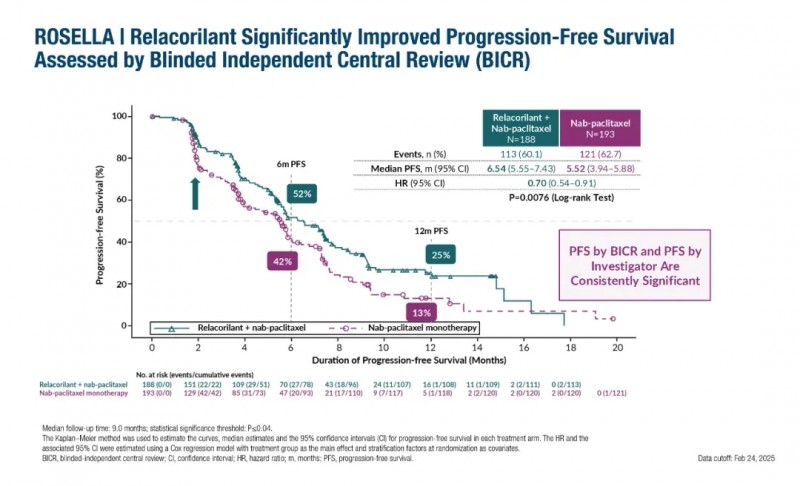
▲图源“JCO”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
中期分析显示,联合治疗组中位总生存期(OS)显著延长至15.97个月(95% CI,13.47-未达到),单药组仅为11.5个月(95% CI,10.02-13.57)(HR,0.69)。两组12个月OS率分别为60%(联合治疗组) vs 49%(单药组)。
此外,联合治疗组客观缓解率(ORR)在数值上更高,Relacorilant联合用药的ORR为36.9%,而白蛋白结合型紫杉醇单药治疗的ORR为30.1%,相当于改善了6.8%(P =0.17)。
多款卵巢癌新药/新技术研发再提速,国内多中心启动
相信看了上面的数据,卵巢癌患者一定燃起了新的希望!好消息是,目前我国正在开展多款针对卵巢癌的临床研究,现已有大量患者通过全球肿瘤医生网抗癌新药招募中心,成功入组接受抗癌新药/新技术的治疗!
CUD002注射液
新药简介
①药品名称:CUD002注射液。
②适应症:难治性/耐药复发性卵巢癌。
招募信息(部分)
1)女性,年龄在18-75周岁(含临界值),体重≥45.0 kg,并自愿签署知情同意书。
2)经病理组织学和/或细胞学检查确诊的卵巢癌患者,WT-1阳性且存在至少一处用RECIST 1.1标准可测量的病灶。
3)能提供足够、新鲜的肿瘤组织,满足基因检测要求。
DC05F01
新药简介
①药品名称:DC05F01(fascin蛋白抑制剂)。
②靶点:DC05F01(fascin蛋白抑制剂)。
③适应症:二线以上卵巢癌、二线内小细胞肺癌(局限期)。
招募信息(部分)
1)年龄≥18周岁,性别不限。
2)经组织学和/或细胞学确诊的复发/难治性卵巢癌等晚期恶性实体瘤患者,经标准治疗失败或无标准治疗方案或现阶段不适用标准治疗。
3)根据RECIST 1.1版,必须至少有一个通过影像学评估的可测量病灶
申请流程
想申请抗癌新药临床试验的患者,需将近期病理报告、基因检测报告等资料汇总后,提交至医学部,进行初步评估。
我们的专家将为您全面分析解读检测报告,预计一个工作日内电话联系推荐用药方案,并匹配适合患者入组的临床试验项目。注:全球肿瘤医生网作为国内权威的肿瘤患者服务平台,我们承诺对所有受试者的个人信息保密,并保证在整个过程中,遵循国家临床研究相关的法律法规。
小编寄语
近年来,卵巢癌的治疗已经取得了长足的进展,逆转了晚期患者的生存期,除了上面整理的内容,还有更多的新药正在研发中。如果您对现有治疗方案不满意,或想了解卵巢癌更多抗癌新药/新技术的更多讯息,可将治疗经历、近期病理检查报告、出院小结等,提交至医学部,进行初步评估。
参考资料
[1]Olawaiye A,et al. ROSELLA: A phase 3 study of relacorilant in combination with nab-paclitaxel versus nab-paclitaxel monotherapy in patients with platinum-resistant ovarian cancer (GOG-3073, ENGOT-ov72)[J]. 2025.
https://ascopubs.org/doi/10.1200/JCO.2025.43.17_suppl.LBA5507
[2]https://www.onclive.com/view/eu-approval-sought-for-relacorilant-in-platinum-resistant-ovarian-cancer
扫描进患者病友群

肺癌|胃癌|肝癌|结直肠癌|胰腺癌
乳腺癌|脑瘤|淋巴瘤|儿童肿瘤等

相关推荐

“手术成功”不等于万事大吉,新型癌症疫苗
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

2026年靶向治疗抗癌风暴,突破困境,普
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

2026年这些肺癌疫苗正悄然改变患者的生
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
新一代NTRK基因融合突变靶向药TL11
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
实现33个月长生存!中国团队成功攻克&q
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

破解术后复发噩梦!NK细胞疗法让晚期胃癌
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05






![[field:title/]](/uploads/allimg/20200224/1-2002241I5262J.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241I3461D.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H94LK.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241HKW34.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H619327.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H34H52.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H22IH.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241G93O18.jpg)




