肺癌首款ADC再下一城,乳腺癌新适应症获优先审评!pCR率超63%
2025年9月10日国家药监局将注射用瑞康曲妥珠单抗(艾维达、SHR-A1811)用于HER2阳性乳腺癌纳入优先评审
2025年9月10日,国家药品监督管理局药品审评中心(CDE)官网显示:我国首款用于HER2突变非小细胞肺癌的ADC药物——注射用瑞康曲妥珠单抗,一项新适应症拟被纳入优先审评,该适应症针对既往接受过一种及以上抗HER2药物治疗的局部晚期或转移性HER2阳性成人乳腺癌患者。
这一进展不仅标志着我国国产ADC药物在跨癌种治疗领域实现重要突破,更意味着众多耐药乳腺癌患者将有望更快迎来精准治疗新选择!
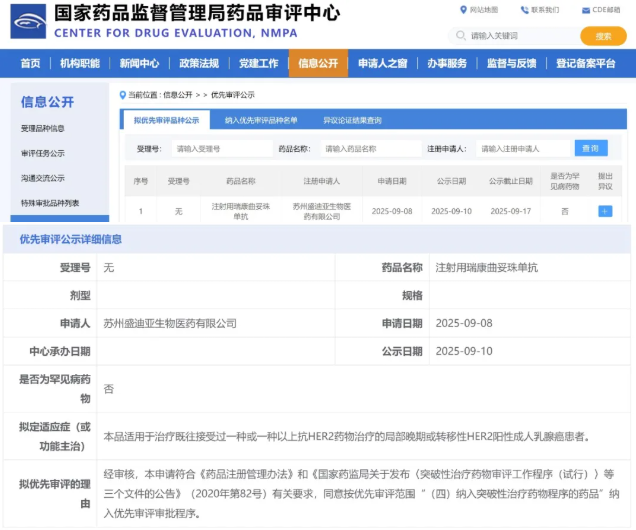
▲截图源自“NMPA”
肺癌首款HER2 ADC药物-瑞康曲妥珠单抗再下一城!乳腺癌新适应症火速纳入优先审评
注射用瑞康曲妥珠单抗(SHR-A1811,商品名:艾维达®)是恒瑞医药研发的一款靶向HER2的抗体偶联药物(ADC),同时也是我国首款用于HER2突变非小细胞肺癌的ADC药物,由曲妥珠单抗、可裂解连接子及拓扑异构酶I抑制剂有效载荷SHR169265巧妙组合而成。
2025年5月29日,该药获得国家药监局批准,单药用于成人存在HER2(ERBB2)激活突变且既往接受过至少一种系统治疗的不可切除的局部晚期或转移性非小细胞肺癌的治疗。
就在昨天(2025年9月10日),该药的新适应证被药监局纳入优先审评,用于局部晚期或转移性HER2阳性乳腺癌的治疗!
瑞康曲妥珠单抗单药暴击HER2阳性乳腺癌,pCR率达63.2%
人表皮生长因子受体2(HER2)阳性乳腺癌是一种具有侵袭性的亚型,约占所有乳腺癌的15%-20%。2025年欧洲肿瘤内科学会(ESMO)大会首次公布了第三代HER2靶向抗体偶联药物(ADC)单药或联合酪氨酸激酶抑制剂(TKI)用于HER2阳性乳腺癌新辅助治疗的研究成果,该研究(NCT05582499)也是首项公布第三代HER2靶向ADC在HER2阳性乳腺癌新辅助治疗中有效性与安全性的研究,相关数据同步发表于《肿瘤学年鉴》。
本次FASCINATE-N(NCT05582499)试验,旨在评估SHR-A1811(瑞康曲妥珠单抗)单药及SHR-A1811联合吡咯替尼的抗肿瘤活性与耐受性数据。研究共纳入265例年龄≥18岁的II-III期HER2阳性乳腺癌患者,其中约45%为激素受体(HR)阳性,70%为III期。患者按1∶1∶1比例随机分为三组:SHR-A1811单药组(n=87)、SHR-A1811联合吡咯替尼组(n=88)、PCbHP方案组(n=90,接受曲妥珠单抗+帕妥珠单抗治疗)。
结果显示:SHR-A1811单药治疗表现出高效性,病理完全缓解率(pCR)达63.2%(HR阳性组50%、HR阴性组74.5%);SHR-A1811联合吡咯替尼疗效与之相近,pCR率为62.5%(HR阳性组44.7%、HR阴性组76%);PCbHP方案组pCR率为64.4%(HR阳性组54.1%、HR阴性组71.7%)(详见下图)。
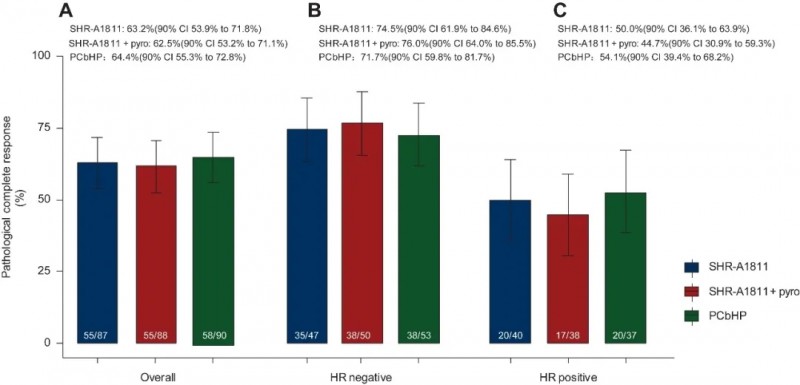
▲图源“ESMO”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
新一代HER2 ADC药物上市在即!国内多中心启动临床
相信看了上面的数据,HER2阳性乳腺癌或其他实体瘤患者,一定燃起了新的希望!好消息是,目前我国正在开展多项针对乳腺癌的临床研究,现已有大量患者通过抗癌新药招募中心,成功入组接受这款抗癌新药的治疗!
TQB2102
药品名称注射用TQB2102(ADC药物)针对癌种HER2、HER3适应证HR阴性/阳性、HER2低表达的局部晚期或转移性乳腺癌
招募信息(部分)
1)年龄:18-75 周岁(签署知情同意书时);ECOG PS 评分:0~1 分;预计生存期超过 3 个月。
2)经病理学证实的HER2 低表达、不可切除的局部晚期或转移性乳腺癌。
3)已明确激素受体(HR)状态。
JSKN003
药品名称注射用JSKN003针对癌种HER2适应证不可切除局部晚期或转移性HER2阳性乳腺癌
招募信息(部分)
1)≥18周岁。
2)经组织学或细胞学确诊的不可切除局部晚期或转移性乳腺癌。
3)组织样本经研究中心实验室检测确认为HER2阳性(IHC3+,或IHC2+且ISH阳性)。
HB0025
药品名称HB0025注射液针对癌种PD-L1适应证局部晚期、复发或转移性三阴性乳腺癌
招募信息(部分)
1)年龄在18~75周岁;
2)能充分理解并自愿签署知情同意书(ICF);
3)受试者需提供最近日期存档和/或新鲜肿瘤组织样本,经中心实验室通过组织学或细胞学证实的三阴性乳腺癌(TNBC)。
申请流程
想申请抗癌新药临床试验的患者,需将近期病理报告、基因检测报告等资料汇总后,提交至医学部,进行初步评估。
我们的专家将为您全面分析解读检测报告,预计一个工作日内电话联系推荐用药方案,并匹配适合患者入组的临床试验项目。注:为国内权威的肿瘤患者服务平台,我们承诺对所有受试者的个人信息保密,并保证在整个过程中,遵循国家临床研究相关的法律法规。
小编寄语
近年来,乳腺癌的治疗已经取得了长足的进展,逆转了晚期患者的生存期,除了上面整理的内容,还有更多的新药正在研发中。如果您对现有治疗方案不满意,或想了解乳腺癌更多抗癌新药/新技术的更多讯息,可将治疗经历、近期病理检查报告、出院小结等,提交至医学部,进行初步评估。
参考资料
[1]Li J J,et al.Efficacy and safety of neoadjuvant SHR-A1811 with or without pyrotinib in women with locally advanced or early HER2-positive breast cancer: a randomized, open-label, phase II trial[J]. Annals of Oncology, 2025.
https://www.annalsofoncology.org/article/S0923-7534(25)00082-1/fulltext
扫描进患者病友群

肺癌|胃癌|肝癌|结直肠癌|胰腺癌
乳腺癌|脑瘤|淋巴瘤|儿童肿瘤等

相关推荐

“手术成功”不等于万事大吉,新型癌症疫苗
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

2026年靶向治疗抗癌风暴,突破困境,普
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

2026年这些肺癌疫苗正悄然改变患者的生
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
新一代NTRK基因融合突变靶向药TL11
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
实现33个月长生存!中国团队成功攻克&q
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

破解术后复发噩梦!NK细胞疗法让晚期胃癌
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05






![[field:title/]](/uploads/allimg/20200224/1-2002241I5262J.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241I3461D.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H94LK.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241HKW34.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H619327.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H34H52.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H22IH.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241G93O18.jpg)




