绝境破冰!WT1-DC疫苗联合化疗攻克"癌王"耐药困局,晚期胰腺癌中位总生存超3年
DC-WT1疫苗联合化疗治疗胰腺癌,攻克"癌王"耐药困局,晚期胰腺癌中位总生存超3年
胰腺导管腺癌(PDAC)是一种死亡率极高的恶性肿瘤,其显著特征是对细胞毒性化疗和放射疗法存在固有耐药性。这一特性导致无法切除的胰腺导管腺癌(UR-PDAC)患者临床治疗效果不佳,因此,研发既针对肿瘤细胞、又能靶向肿瘤微环境(TME)的新型疗法,成为改善患者预后的迫切需求。
近日,《免疫肿瘤学杂志》报道了一项突破性研究:应用多功能 WT1-DC 疫苗治疗不可切除晚期胰腺导管腺癌(UR-PDAC)的 Ⅰ 期临床试验,公布了令人振奋的初步数据 —— 所有入组患者中位OS超3年、PFS超2年!WT1-DTH 长期阳性患者生存期更是达4.5 年!这一突破为长期困于治疗绝境的晚期胰腺癌患者点亮了跨越数年的生存希望,让难治性胰腺癌的治疗迎来了值得期待的新曙光!

▲截图源自“PMC”
WT1-DC疫苗联合化疗让晚期患者肿瘤负荷大降,生存期达3.52年,中位无进展生存期达2.23年
WT1是一种与血管生成、肿瘤进展、侵袭及转移密切相关的转录因子,在肿瘤发生中发挥致癌作用。它不仅表达于胰腺导管腺癌(PDAC)细胞,还存在于肿瘤微环境(TME)的癌症干细胞、髓系抑制细胞(MDSC)及肿瘤血管中,这使其成为极具潜力的癌症治疗靶点。而树突状细胞(DC)作为专业抗原呈递细胞,在启动和调节肿瘤相关抗原特异性免疫反应中起着关键作用。
基于此,研究团队开发出一种新型WT1肽脉冲树突状细胞(WT1-DC)疫苗,Ⅰ期临床研究数据同步发表于《免疫肿瘤学杂志》中。
该研究共纳入10例不可切除晚期胰腺导管腺癌(UR-PDAC)患者,包括6例局部晚期胰腺导管腺癌(LA-PDAC)、3例转移性胰腺导管腺癌(M-PDAC)、1例术后复发患者,均经病理确诊为腺癌,且表达WT1和MHCⅠ类分子。入组后,先接受白蛋白结合型紫杉醇+吉西他滨联合化疗,再接受WT1-DC疫苗治疗。
结果显示:在9例可评估预后的患者中,WT1肽特异性迟发型超敏反应(WT1-DTH)长期阳性患者(n=4)的临床疗效显著优于短期阳性患者(n=5),且所有WT1-DTH长期阳性患者的生存期均达到至少4.5年。此外,所有患者的肿瘤负荷均有下降(降幅0.0%-57.4%)(详见下图)。
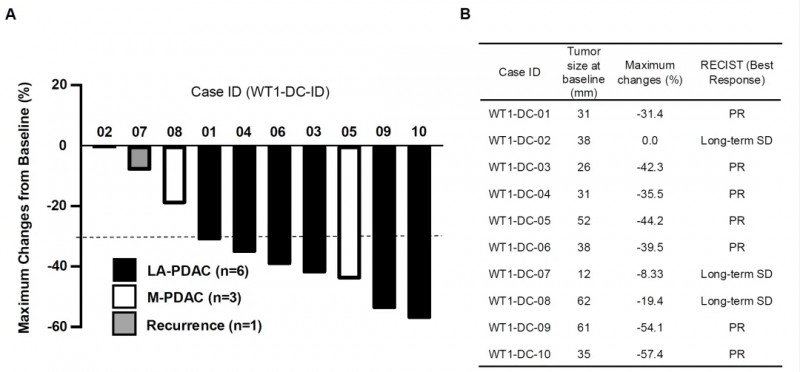
▲图源“J Immunother Cancer”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
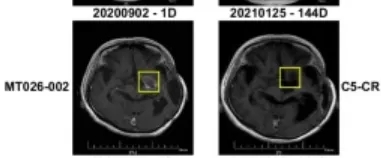
其中7例患者(6例局部晚期胰腺导管腺癌、1例转移性胰腺导管腺癌)实现部分缓解(PR),其余3例维持长期疾病稳定(SD)。治疗约6个月后,患者肿瘤最大标准摄取值(SUVmax)显著下降(p=0.006)。下图展示了4例不可切除晚期胰腺导管腺癌(UR-PDAC)患者(编号WT1-DC-01、WT1-DC-03、WT1-DC-05、WT1-DC-09),在接受治疗前后的CE-CT与¹⁸F-FDGPET/CT影像对比,清晰展示了治疗带来的变化。
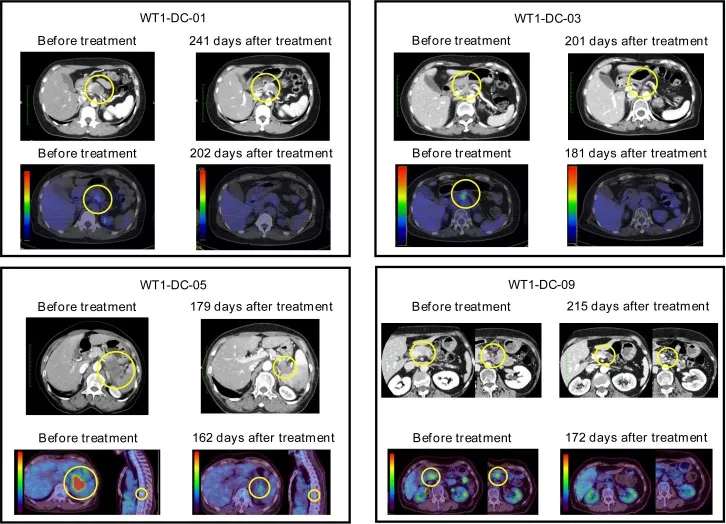
▲图源“J Immunother Cancer”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
此外,生存数据更为亮眼:9例患者的中位无进展生存期(PFS)达2.23年,中位总生存期(OS)达3.52年(详见下图A)。其中,5例局部晚期胰腺导管腺癌(LA-PDAC)患者的中位PFS为2.48年,总生存期尚未达到;而3例转移性胰腺导管腺癌(M-PDAC)患者的中位PFS达1.37年、中位OS达2.41年(详见下图B)。
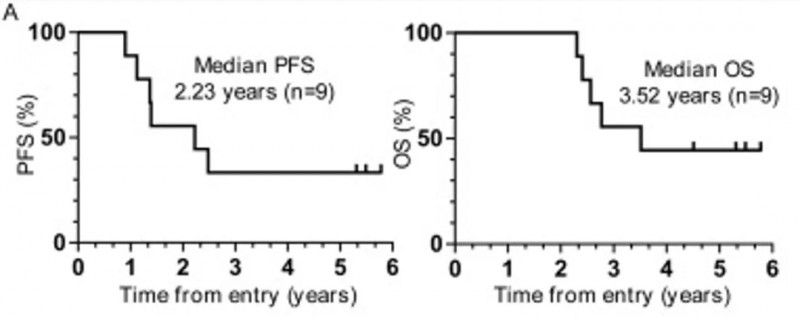
▲图源“J Immunother Cancer”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
综上,通过WT1-DC疫苗联合化疗的免疫治疗方案,可强效激活UR-PDAC患者的WT1特异性免疫反应,有望调节肿瘤微环境并为部分患者争取转化手术机会,最终带来显著的临床获益。
小编寄语
树突状细胞(DC)作为体内唯一能激活初始T细胞的抗原提呈细胞,在免疫反应中占据核心地位。目前,DC疫苗虽多数仍处于早期临床试验阶段,但已在部分国家正式应用于临床。对于早期肿瘤患者,术后采用DC疫苗联合放化疗的辅助治疗方案,可通过清除残留癌细胞、形成免疫记忆,降低复发转移风险。
树突状疫苗在日本、德国等,用于临床辅助治疗多种癌症,包括皮肤癌、肝癌、肺癌、肾癌、乳腺癌等,是癌症患者的新希望!值得欣慰的是,如今我国也有多款癌症疫苗正在开展临床研究,这也意味着中国患者也有机会寻求这款抗癌新技术的帮助!
对目前治疗方案不满意,或想寻求树突状细胞疫苗等抗癌新技术帮助的患者,可将近期病理报告、影像学检查资料、治疗经历等,提交至医学部,进行初步评估。
参考资料
[1]Koido S,et al.Dendritic cells pulsed with multifunctional Wilms' tumor 1 (WT1) peptides combined with multiagent chemotherapy modulate the tumor microenvironment and enable conversion surgery in pancreatic cancer. J Immunother Cancer. 2024 Oct 8;12(10):e009765.
https://pmc.ncbi.nlm.nih.gov/articles/PMC11474828/
扫描进患者病友群

肺癌|胃癌|肝癌|结直肠癌|胰腺癌
乳腺癌|脑瘤|淋巴瘤|儿童肿瘤等

相关推荐

“手术成功”不等于万事大吉,新型癌症疫苗
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

2026年靶向治疗抗癌风暴,突破困境,普
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

2026年这些肺癌疫苗正悄然改变患者的生
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
新一代NTRK基因融合突变靶向药TL11
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
实现33个月长生存!中国团队成功攻克&q
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

破解术后复发噩梦!NK细胞疗法让晚期胃癌
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05






![[field:title/]](/uploads/allimg/20200224/1-2002241I5262J.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241I3461D.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H94LK.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241HKW34.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H619327.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H34H52.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H22IH.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241G93O18.jpg)




