双重突破!47%完全缓解+病毒持续清除!国研TCR-T开启肝癌治愈新可能
国研TCR-T疗法SCG101治疗肝癌双重突破,47%完全缓解+病毒持续清除
近一半晚期肝癌患者肿瘤消退,23.5%的患者甚至实现了HBsAg(血清乙肝表面抗原)完全消失和持续清除!中国研发新型TCR-T疗法为肝癌患者开启治愈新可能!
肝癌,尤其是肝细胞癌(HCC),一直是全球癌症领域的难题。慢性乙型或丙型肝炎、大量饮酒、脂肪肝和其他黄曲霉素等毒性食物引起的肝损伤是导致肝癌的元凶,其中最为严峻的是HBV病毒性肝癌。据统计,全球每年有超过42万人发生与HBV相关的肝癌,至少占50%全球病例,而亚洲最为严重,至少80%的患者是HBV相关的肝癌!
尽管近年来针对晚期肝细胞癌的系统性治疗取得一定进展,靶向联合免疫治疗体系逐步建立,但HBV相关肝细胞癌的精准治疗仍存在巨大缺口。HBV相关肝细胞癌患者体内的HBV特异性T细胞往往功能性耗竭,导致自身免疫系统无法有效清除感染肝细胞和肝癌细胞,治疗陷入困境。临床上迫切需要针对这一广大人群的新疗法!
近日,2025年欧洲肝病研究协会大会上揭晓的一项I期临床试验(NCT06617000)数据显示,SCG101——一种自体乙肝病毒(HBV)特异性T细胞疗法,能够促使患者肿瘤缩小,并实现HBV-DNA和血清乙肝表面抗原(HBsAg)的持续清除的双重突破,引起巨大轰动!
双重突破!47%完全缓解+病毒持续清除!国研TCR-T开启肝癌治愈新可能
SCG101是一种自体T细胞受体(TCR)T细胞疗法,是专门针对乙肝表面抗原(HBsAg)特定表位而设计的,这种全新的疗法可以特异性地靶向HBV-HCC感染细胞,能够触发溶细胞和非溶细胞两种机制,不仅能够高效清除HBV感染的肝细胞,还能对癌前病变细胞和HBV-HCC细胞进行精准打击,一箭双雕!
2023年国际细胞与基因治疗学会(ISCT)会议上,同类首创自体HBsAg特异性T细胞受体工程化T细胞(TCR-T)疗法-SCG101的初步数据公布,引起巨大轰动!
SCG101显示出显著的抗肿瘤活性,一位患者接受单剂量SCG101单药治疗后肿瘤缩小74.5%(mRECIST)。数据截止报告显示,肿瘤反应可持续6.9个月以上。
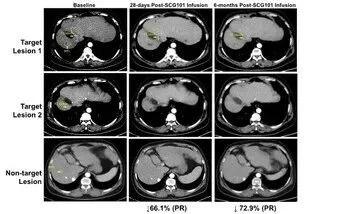
更值得一提的是,这位患者治疗后的活检显示肝脏中HBsAg+肝细胞100%被根除!
2024年的欧洲肝病研究协会(EASL)大会上,SCG101公布了首次人体的临床试验结果,非常振奋人心!
在刚刚过去的2025年欧洲肝病研究协会(EASL)大会上g公布了最新的临床数据:
SCG101在晚期HBV相关肝细胞癌(HCC)患者中展现出良好的抗病毒和抗肿瘤双重活性。在6例晚期HBV-HCC患者中,患者接受5.0×10^7~1.0×10^8TCR+T细胞/kg的SCG101治疗,客观缓解率(ORR)为33%。所有获得部分缓解(PR)的患者均维持缓解超过6个月,其中1名幸运的患者靶病灶完全缓解并维持无进展生存期27个月。
这项试验纳入的17名符合条件的乙肝相关肝细胞癌患者,这些患者都是既往做过各类治疗失败的晚期难治患者。令人惊喜的是,在接受单次SCG101输注后,所有患者的血清HBsAg水平均呈现迅猛下降趋势。尤为瞩目的是,94%的患者在短短28天内,HBsAg水平从1.0log₁₀急剧降至4.6log₁₀,并且在长达一年的时间内,始终维持在100IU/mL以下的低水平。此外,23.5%的患者甚至实现了HBsAg完全消失,这一成果在HBV相关疾病治疗中具有重大意义。
在抗肿瘤活性方面,SCG101同样表现出色。高达47%的患者在接受输注后,出现了可测量的肿瘤消退迹象。截至数据统计截止日期,患者的中位总生存期(OS)尚未达到,意味着该疗法有望为患者带来更长久的生存可能,极大地改善了患者的预后情况。
北京协和医院肝外科主任杜顺达医学博士在相关新闻稿中指出:“SCG101展现出的抗病毒和抗肿瘤双重功效,极具前景,特别是对于那些经历过大量前期治疗的患者而言。持续的HBsAg清除以及肿瘤缓解现象表明,SCG101很可能成为HBV相关肝细胞癌患者全新的免疫治疗选择,有望填补该领域长期以来尚未满足的重大临床需求。”
SCG细胞治疗公司首席执行官ChristyMa在新闻稿中补充道:“这些积极的数据,标志着SCG101研发进程中迈出了关键一步,也充分验证了我们利用精准T细胞疗法治疗慢性乙型肝炎(HBV)感染以及HBV相关肝癌的策略的正确性。SCG101作为首款在HBV相关肝细胞癌(HCC)患者中,同时证实能够实现病毒学清除和肿瘤消退的T细胞受体(TCR)T细胞疗法,这些数据让我们备受鼓舞。我们满怀期待,将通过进一步的临床开发,推动SCG101尽快应用于临床,为有需求的患者带来这种潜在的治愈性疗法。”
宣战肝癌的终极武器!全新TCR-T免疫疗法震撼登场
人体的免疫防御机制主要依靠体内的白细胞军团,作为白细胞的一种,T细胞有着不可替代的作用,它们是人体里面的特种兵,一旦发现癌细胞,T细胞首先主动出击,杀灭敌人,因此,它也被称为“杀手T细胞”。
大部分肿瘤患者体内没有足够能识别和杀伤肿瘤细胞的T细胞,对于这些患者,医生可以采用一种称为工程T细胞受体(TCR)治疗的方法。
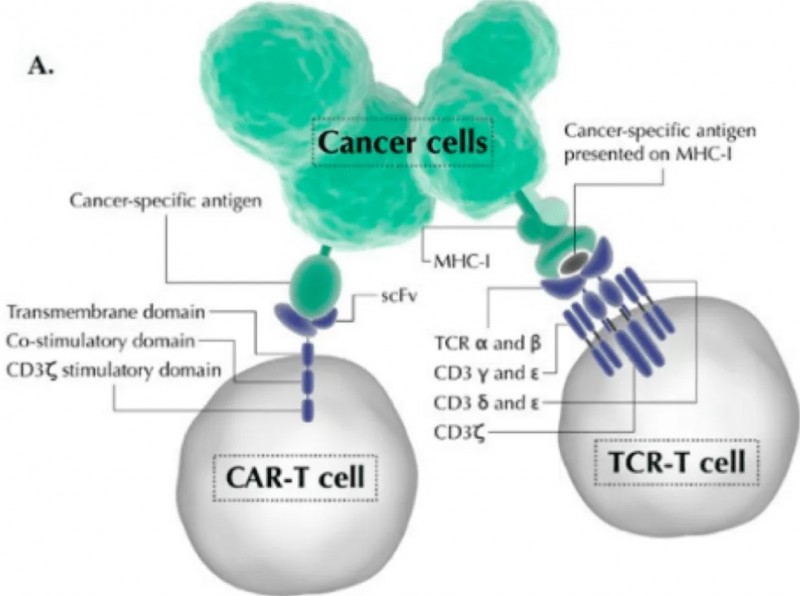
TCR-T技术,即T细胞受体(TCR)嵌合型T细胞技术,也叫亲和力增强的TCR”技术,需要从患者身上获取T细胞,为T细胞配备新的T细胞受体,使其能够靶向特定的癌症抗原的疗法,这种新型的疗法可以允许医生为每个患者的肿瘤和不同类型的T细胞选择最合适的靶点进行工程改造,使治疗个体化,并为患者提供更大的缓解希望。
这款疗法之所以备受期待,上市后引起全球轰动,开启实体瘤治疗新纪元,主要是因为以下三点:
1.扩增数量高达数十至上百亿的"活的"细胞疗法
与CAR-T疗法不同,TCR-T是通过收集患者自己的T细胞,并对其进行改造使其具有改良的TCR而制成的。这些TCR具有增强的识别肿瘤特异性抗原蛋白的能力,这种蛋白质在肝癌,滑膜肉瘤等一些癌细胞表面高表达。一旦经过改造并扩增到数十至上百亿级别,具有增强TCR的T细胞就会通过一次性治疗放回您的体内,精准识别并疯狂攻击表达特定的癌细胞。
2.肿瘤缩小甚至消失,有望治疗多种实体瘤
除了滑膜肉瘤,这款疗法在包括恶性程度极高的滑膜肉瘤,卵巢癌,头颈癌,胃癌,粘液样/圆形细胞脂肪肉瘤,非小细胞肺癌,尿路上皮癌,食道癌和黑色素瘤等各类临床上可以说是没有任何标准治疗方案的极晚期患者中显示出了卓越的潜力,众多接受了新型的TCR-T疗法的患者,产生了强烈的响应。
3."一针"即可清除肿瘤
与CAR-T和TIL一样,TCR-T疗法是一种一次性治疗。
步骤1:血液和肿瘤组织检测,确认HLA类型和MAGE-A4阳性
步骤2:T细胞采集,这些细胞将用于制造TECELRA。
步骤3:治疗前化疗(4天),您将接受淋巴细胞清除术。
步骤4:TECELRA给药(1个输液袋最长1小时)
步骤5:输注后监测(最长4周)
| CAR-T细胞疗法 | TCR-T细胞疗法 | |
| 结构体 | – 由细胞内和细胞外结构域组成的工程受体 | – 天然或最低限度工程化的 TCR |
| 目标 | – 仅针对细胞表面抗原 | – 针对 MHC 类分子呈现的细胞表面和细胞内抗原 |
| 优点 | – 细胞靶标不受 MHC 复合体限制。 – 血液癌症的良好治疗效果 | – 实现更多样化的靶标,因为它可以靶向细胞内抗原 – 允许与 MHC 进行高度敏感的结合相互作用实体瘤治疗中的令人鼓舞的结果 |
| 缺点 | – 对实体瘤影响不大 – 副作用如细胞因子释放综合征和神经毒性 | – 受 MHC 相容性限制 – 细胞因子释放综合征和神经毒性等副作用 |
| FDA状态 | – 批准治疗多种癌症 | – 预计上市时间(2024年8月) |
CAR-T和TCR-T疗法的区别
国内患者如何接受TCR-T疗法
除了SCG101,目前国内有包括香雪生物,百吉生物、来恩生物、华夏英泰、可瑞生物、天科雅、普瑞金、深圳宾德、泛恩生物、立凌生物等17家生物公司布局TCR-T赛道,其中50多个TCR-T在研项目已进入或者获批临床。其中,香雪生命科学的TAEST16001注射液是国内进度最快的产品之一,已进入II期临床阶段。此外,进度较快的还有华夏英泰的YT-E001,正在开展治疗Epstein-Barr病毒(EBV)相关鼻咽癌的II期临床。
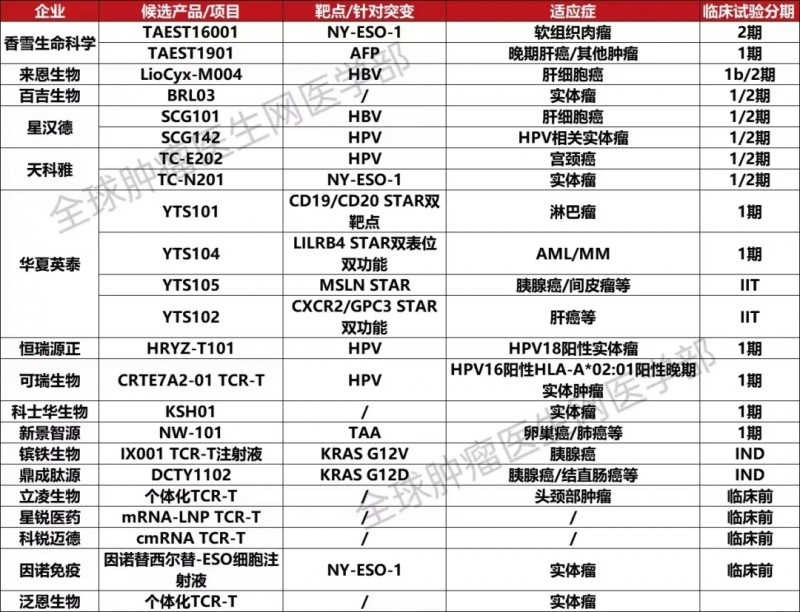
好消息是,目前多款针对肝癌,宫颈癌,胰腺癌,结直肠癌等各类实体瘤的临床试验正在进行中,很多患者已通过成功入组。
部分入组条件
●18-75岁,男女不限,无严重基础疾病;
●仅患一种恶性实体肿瘤,肝癌、头颈部鳞癌、宫颈癌、胰腺癌等实体瘤;
●经标准治疗失败或缺乏有效治疗方法;
●各项检查符合要求且至少1年的预期寿命。
想寻求TCR-T疗法及其他国内外新抗癌治疗帮助,且经济条件允许的情况下,可以先将病历提交至医学部进行初步评估,一旦审核通过,有机会获得”天价“疗法免费治疗的机会。
随着全球首款TCR-T细胞疗法的成功上市和国内企业的不断努力,全球范围内TCR-T细胞疗法领域有望迎来爆发式增长。预计在未来几年内,将有更多TCR-T细胞疗法产品获批上市,为患者提供更多样化、更精准的治疗选择。
越来越多的医生将有能力让合适的患者在正确的时间获得个体化”量体裁衣“式的治疗方案!相信这些效果好的抗癌疗法都会加快在我国上市和纳入医保的步伐,让更多的百姓获益,我们共同期待!随着更多治疗方案的发展,晚期肿瘤患者将迎来更多治疗选择和希望,我们期待人类攻克癌症的那一天早日到来。
扫描进患者病友群

肺癌|胃癌|肝癌|结直肠癌|胰腺癌
乳腺癌|脑瘤|淋巴瘤|儿童肿瘤等

相关推荐

“手术成功”不等于万事大吉,新型癌症疫苗
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

2026年靶向治疗抗癌风暴,突破困境,普
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

2026年这些肺癌疫苗正悄然改变患者的生
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
新一代NTRK基因融合突变靶向药TL11
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
实现33个月长生存!中国团队成功攻克&q
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

破解术后复发噩梦!NK细胞疗法让晚期胃癌
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05






![[field:title/]](/uploads/allimg/20200224/1-2002241I5262J.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241I3461D.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H94LK.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241HKW34.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H619327.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H34H52.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H22IH.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241G93O18.jpg)




