满格应答!国研新型CAR-T临床首秀实现100%客观缓解!多靶点疗法通杀血癌、肝癌、肠癌等
国研CT071临床首秀实现100%客观缓解!多靶点CAR-T细胞疗法通杀血癌、肝癌、肠癌等
CT071是一款针对G蛋白偶联受体C类第5组D成员(GPRC5D)的新型全人源自体嵌合抗原受体(CAR)T细胞疗法,且具备快速生产能力。
2025年10月,CT071在《柳叶刀》杂志重磅公布其在中国开展的首例人体I期临床试验(NCT05838131)数据:入组的23例多发性骨髓瘤患者中,客观缓解率高达100%!这一突破性成果不仅彰显了我国在CAR-T细胞疗法领域的强劲实力,更为肿瘤患者带来了全新的生存希望!

▲截图源自“THE LANCET Haematology”
《柳叶刀》十月重磅发布:CT071向难治性多发性骨髓瘤宣战,客观缓解率达100%
这项首例人体、单中心、单组I期临床试验,共纳入23例18岁及以上的复发或难治性多发性骨髓瘤患者,中位年龄为63.0岁(IQR:53.0–65.5)。这些患者需满足以下条件:既往接受过三线及以上治疗(含蛋白酶体抑制剂和免疫调节剂),或接受过双线难治性治疗且在最后一线治疗中病情进展。入组后均接受CT071CAR-T细胞回输治疗。
结果显示:客观缓解率(ORR)达100%(95%CI:83.2-100),完全缓解及以上率为50%(10例/20例)。
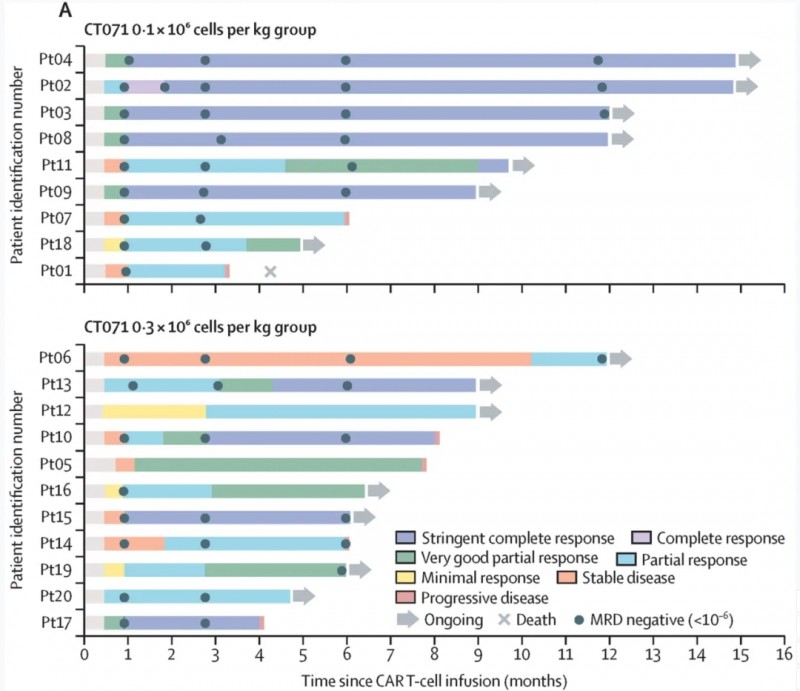
▲图源“THE LANCET Haematology”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
综上,CT071在复发或难治性多发性骨髓瘤患者中展现出令人鼓舞的安全性和显著的治疗活性。
从三线到二线!liso-cel CAR-T凭实力开启淋巴瘤治疗新赛道,18个月无进展生存率为72%
对于复发或难治性(R/R)大B细胞淋巴瘤(LBCL)患者,治疗选择存在明显差异且困境突出:不适合接受高剂量化疗(HDCT)/造血干细胞移植(HSCT)的患者,历来治疗选项有限且疗效较差;而对于适合移植的患者,近年研究已证实,二线治疗中嵌合抗原受体(CAR)T细胞疗法的生存获益优于HDCT/HSCT。
lisocabtagene maraleucel(liso-cel,Breyanzi®)是一款自体、靶向CD19的4-1BB CAR-T细胞产品,其安全性和有效性已在多种血液肿瘤中得到充分验证,包括复发或难治性大B细胞淋巴瘤(R/R LBCL)、慢性淋巴细胞白血病、套细胞淋巴瘤及滤泡性淋巴瘤(FL)。作为新型治疗方案,liso-cel已重新定义LBCL的治疗格局,数据显示其相比历史标准治疗(SOC)不仅具有更显著的生存优势,且毒性特征更优。目前已有两项重要研究为liso-cel的应用提供支撑:
2025年10月21日,OncLive最新报道了liso-cel的1期TRANSCEND NHL 001试验(NCT02631044)的数据,该数据集支持FDA批准liso-cel用于三线治疗。
除此之外,《Blood Adv》还发布了针对不适合造血干细胞移植(HSCT)的R/R LBCL患者开展的2期PILOT研究(NCT03483103)最终结果。该研究共纳入61例复发或难治性大B细胞淋巴瘤(R/R LBCL)患者,均接受过一线治疗且符合≥1次HSCT非预期标准。结果显示如下:
1、总体缓解率(ORR):患者总体缓解率(ORR)达80%(49/61,95%CI:68-89),其中54%(33/61,95%CI:41-67)达到完全缓解(CR)。
2、中位缓解持续时间(DOR):缓解持久性同样优异,中位缓解持续时间(DOR)为23.3个月[95%CI:6.2-未达到(NR)],18个月DOR率53%(95%CI,37-66),而达到CR的患者中位DOR为NR(95%CI,21.7至NR),18个月DOR率高达72%(95%CI,53-84;详见下图A)。
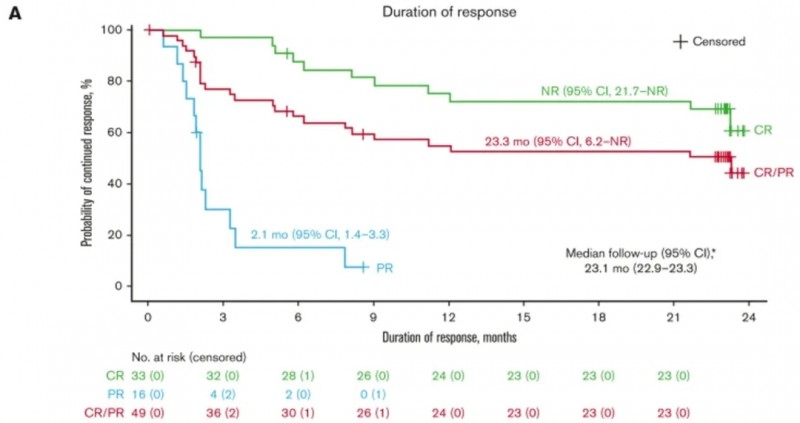
▲图源“Blood Adv”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
3、中位无进展生存期(PFS):长期生存获益也十分显著,患者中位无进展生存期(PFS)为9.0个月(95%CI,4.2-NR),18个月PFS率43%(95%CI,30-55),达到CR的患者18个月PFS率为72%(详见下图B)。
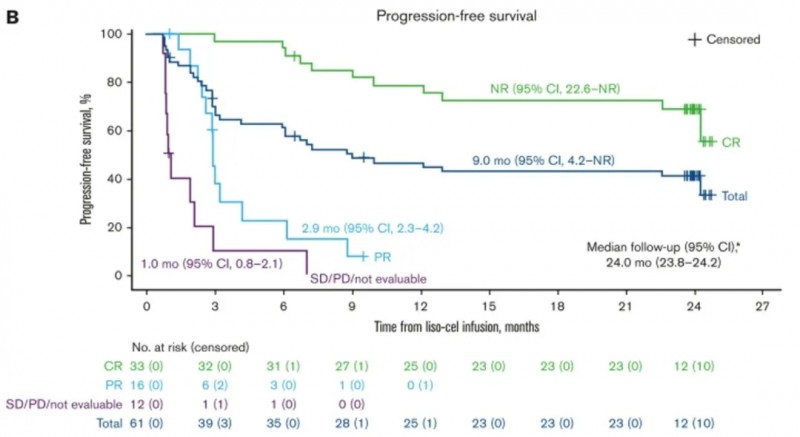
▲图源“Blood Adv”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
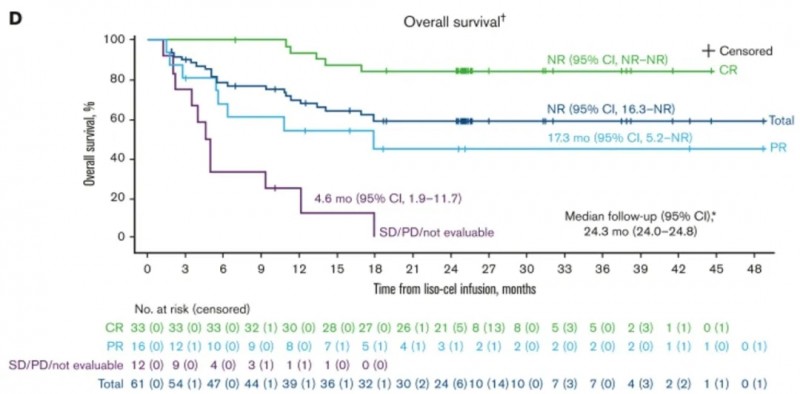
4、中位总生存期(OS):中位OS为NR(95%CI,16.3-NR),18个月OS率59%(95%CI,45-70;详见下图D)。
▲图源“Blood Adv”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
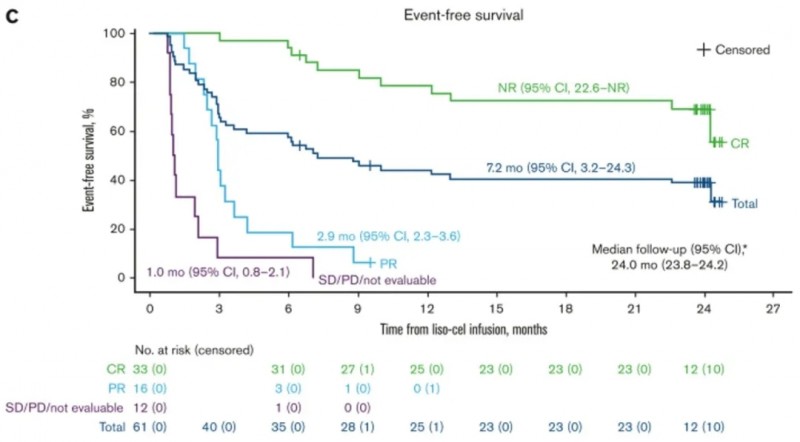
5、中位无事件生存期(EFS):中位EFS为7.2个月(95%CI,3.2-24.3),18个月EFS率40%(95%CI,28-52),达到CR的患者18个月EFS率亦为72%(95%CI,53-84,详见下图C)。
▲图源“Blood Adv”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
C-CAR031 CAR-T疗法携"分子盾"暴击肝癌,肿瘤持续缩小超12个月
CAR-T细胞疗法除了治疗血液肿瘤外,近年来也被尝试用于实体瘤领域。比如C-CAR031就是一款靶向GPC3(肝癌黄金靶标)的CAR-T细胞疗法,由阿斯利康基于其TGFβRII(转化生长因子-β受体II)显性负装甲发现平台设计,西比曼生物负责中国地区的生产并联合开发。其核心优势在于双重靶向机制:一方面特异性结合肝癌、肺癌等实体瘤高表达的GPC3;另一方面搭载TGFβ信号通路阻断“分子盾”,可突破肿瘤微环境的免疫抑制。
2024年美国临床肿瘤学会(ASCO)年会上,西比曼生物公布了C-CAR031首次人体临床研究(IIT)的惊艳数据。针对先前接受1-6线治疗的多线治疗失败晚期肝癌(HCC)患者,该疗法展现出可控的安全性与显著的抗肿瘤活性。其中两例患者(C023与C010)接受治疗后,均呈现肿瘤持续退缩的振奋疗效。
具体来看,C010号患者(DL3)的疗效更为持久,经12个月以上跟踪,肿瘤持续稳定缩小;另一例C023号患者(DL4)治疗仅1.5个月,肺转移病灶便出现深度应答,影像学可见肿瘤显著缩小。
▼C010号患者治疗前后影像学对比
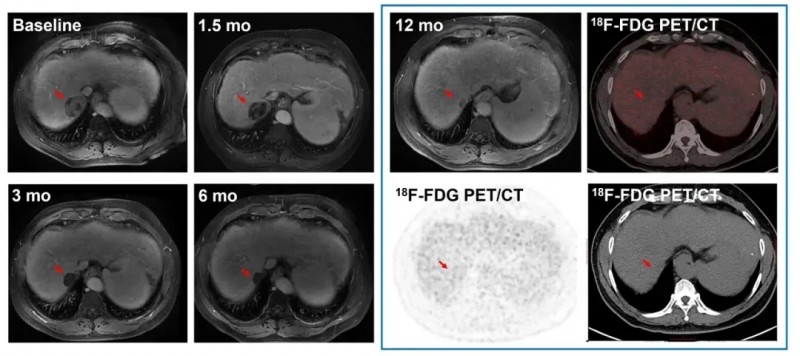
▼C023号患者治疗前后影像学对比
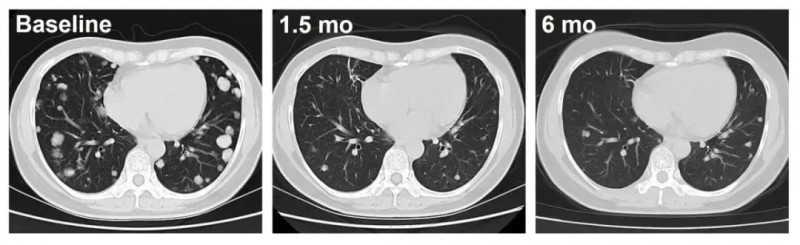
▲图源“ASCO”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
CEA CAR-T精准狙击结直肠癌,70%患者病情稳定
癌胚抗原(CEA)是胃肠道癌症的高敏感性标志物,在结直肠癌(CRC)的组织及血清中广泛表达。其独特优势在于,除胃肠道外,CEA仅在上皮细胞面向管腔的顶端膜面低水平表达,而该区域难以被免疫细胞触及——这一特性使其成为CAR-T疗法的理想靶点。该疗法的优先适用人群包括治疗失败、术后担忧复发及CEA指标异常的患者,适用癌种涵盖结直肠癌、非小细胞肺癌、乳腺癌、胃癌、胰腺癌等。我国曾开展一项CEA CAR-T细胞疗法I期临床试验(NCT02349724),旨在治疗CEA阳性结直肠癌患者。
试验数据同样振奋:10例既往治疗进展(PD)的患者中,7例治疗后达到病情稳定(SD),肿瘤直径仅轻微变化,其中2例患者的稳定状态持续超30周(7.5个月)。典型病例的疗效尤为亮眼:P10患者接受DL4剂量治疗后,MRI证实其肝内一处病灶明显缩小(详见下图)。
▼P10患者在CAR-T治疗前(左图)、治疗4周后(右图)的MRI对比
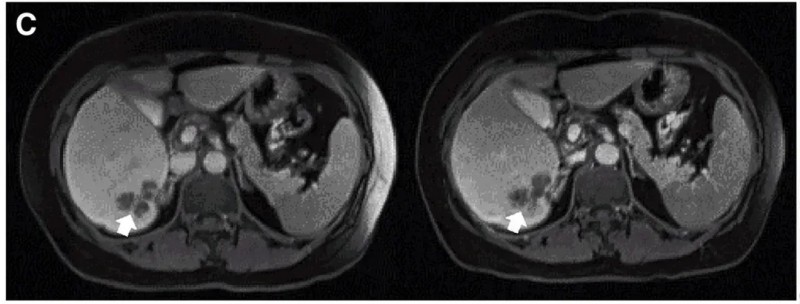
▲图源“Molecular Therapy”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
百万疗法免费招募!中国成功研发多款CAR-T疗法,国内多家中心启动招募
曾经,CAR-T这项先进的治疗技术一直掌握在医疗水平发达的国家,很多病友在苦苦等待中遗憾离开。值得中国病友们振奋的是,“天价”疗法不再遥不可及,中国已成功研发出多款针对多款血液肿瘤及实体瘤的CAR-T疗法,并在国内多家知名癌症中心启动临床,很多晚期患者已通过全球肿瘤医生网,成功入组接受治疗!目前有多款CAR-T临床实验正在火热招募中,主要针对以下靶点及肿瘤类型:
1、血液肿瘤
①CD19:用于淋巴瘤、白血病、B细胞急性淋巴细胞白血病等;
②BCMA:用于多发性骨髓瘤等;
③CD20:用于淋巴瘤、B细胞非霍奇金淋巴瘤、弥漫大B细胞淋巴瘤等;
④CD33:用于急性髓细胞白血病等;
⑤CD3:用于多发性骨髓瘤等;
⑥CD7:用于外周T细胞淋巴瘤等;
⑦CD4:用于淋巴瘤等;
⑧CLL-1:用于急性髓细胞白血病等;
⑨EBV:用于淋巴瘤等。
2、实体瘤
①GPC3:用于肝癌等;
②GUCY2C:用于结直肠癌的治疗;
③PSMA:用于治疗前列腺癌等;
④Claudin18.2:用于胰腺癌、胃癌等;
⑤EGFRvII:用于治疗神经胶质瘤、头颈部肿瘤等;
⑥MUC-1:用于治疗肺癌、胃癌、胰腺癌、肝癌、结肠癌等;
⑦CEA:用于治疗胰腺癌、肺癌、结肠癌、胃癌、乳腺癌等;
⑧间皮素(mesothelin):用于治疗间皮瘤、胰腺癌、卵巢癌、肺癌等;
⑨B7-H3:用于治疗尤文肉瘤、髓母细胞瘤、肾母细胞瘤、神经母细胞瘤、横纹肌肉瘤、特别难以治疗的脑干肿瘤(DIPG)等。
申请流程
想寻求CAR-T疗法帮助的患者,可将近期影像学检查、病理检查、治疗经历等资料,提交至医学部,进行初步评估或了解详细的入排标准。
小编寄语
CAR-T细胞疗法经过数十年的发展,已成为肿瘤治疗领域的新兴支柱,作为肿瘤免疫细胞疗法中的佼佼者,在治疗血液肿瘤方面的成绩有目共睹。如今CAR-T技术也已发展到了第五代,国内外相继有13款产品获批上市。CAR-T疗法的出现打破了传统的肿瘤治疗模式,肿瘤免疫疗法也成为了继手术、放化疗后的第四类肿瘤治疗方法。期待其在血液肿瘤和实体瘤的治疗领域,能取得更大的突破,并早日纳入医保范畴,让越来越多的癌症患者能得到这款“天价”疗法的帮助!
想明确自身靶点或寻求CAR-T等新型疗法帮助的患者,可将完整的病理报告、治疗经历等资料,提交至医学部,进行初步评估,或申请国外内抗癌专家会诊。
参考资料
[1]Jin L,et al.GPRC5D-targeted CAR T-cell therapy (CT071) in patients with relapsed or refractory multiple myeloma: a first-in-human, single-centre, single-arm, phase 1 trial[J]. The Lancet Haematology, 2025, 12(10): e798-e807.
https://www.thelancet.com/journals/lanhae/article/PIIS2352-3026(25)00176-0/abstract
[2]Sehgal A,et al.Lisocabtagene maraleucel for R/R LBCL in patients not intended for HSCT: final results of the phase 2 PILOT study. Blood Adv. 2025 Aug 12;9(15):3694-3705.
https://pmc.ncbi.nlm.nih.gov/articles/PMC12305224/
[3]Zhang Q,et al.Phase I study of C-CAR031, a GPC3-specific TGFβRIIDN armored autologous CAR-T, in patients with advanced hepatocellular carcinoma (HCC)[J]. 2024.
https://meetings.asco.org/abstracts-presentations/234377
[4]https://www.onclive.com/view/liso-cel-data-confirm-durable-efficacy-and-confer-broad-use-in-r-r-lbcl
扫描进患者病友群

肺癌|胃癌|肝癌|结直肠癌|胰腺癌
乳腺癌|脑瘤|淋巴瘤|儿童肿瘤等

相关推荐

癌症治疗本就不应千篇一律,揭秘mRNA癌
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
“不限癌种”新突破,NTRK基因融合的靶
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
肺癌疫苗重大突破,晚期患者多了一个新的选
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

“手术成功”不等于万事大吉,新型癌症疫苗
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

2026年靶向治疗抗癌风暴,突破困境,普
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

2026年这些肺癌疫苗正悄然改变患者的生
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05






![[field:title/]](/uploads/allimg/20200224/1-2002241I5262J.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241I3461D.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H94LK.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241HKW34.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H619327.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H34H52.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H22IH.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241G93O18.jpg)




