2年总生存率70%!瑞基奥仑赛新适应症申报上市!国产CAR-T多线爆发,横扫血癌、肝癌、肠癌、胃癌等
瑞基奥仑赛新适应症申报上市,国产CAR-T多线爆发,横扫血癌、肝癌、肠癌、胃癌等
2025年5月24日,国家药监局药品审评中心(CDE)官网传来重磅喜讯——药明巨诺旗下明星CAR-T产品——瑞基奥仑赛注射液(倍诺达®,Carteyva®)正式提交第四项适应症上市申请!拟用于一线治疗失败后不适合大剂量化疗与自体干细胞移植的成人复发/难治性侵袭性B细胞非霍奇金淋巴瘤(r/rB-NHL)的治疗,为生命续航再添新希望!
作为中国首个覆盖三大癌种适应症的CAR-T标杆产品,瑞基奥仑赛此次向第四项适应症发起冲刺,不仅标志着国产细胞治疗技术的跨越式突破,更意味着国产CAR-T疗法正式开启“一药多用”的治疗新时代——从单一病种到多线覆盖,从“精准打击”到“更广普惠”,其背后是中国创新药企研发实力的全面跃升。未来,随着该适应症的落地,有望为更多患者带来新的希望与更多选择!
▲截图源自“NMPA”
瑞基奥仑赛:中国首个拥有三款适应证的CAR-T产品,开启国产CAR-T多癌种治疗新时代
瑞基奥仑赛注射液(relma-cel,relmacabtagene autoleucel,倍诺达®,Carteyva®,)是一款靶向CD19的CAR-T细胞治疗产品,作为中国首个获批用于治疗复发或难治性套细胞淋巴瘤(r/r MCL)的CAR-T细胞疗法,也是国内首个拥有三款适应症的CAR-T产品。其研发进展如下:

1、2021年9月:首次在中国获批上市,适应症为成人二线及以上治疗后的复发或难治性大B细胞淋巴瘤(r/rLBCL)。
2、2022年10月:新适应症在我国获批,用于复发或难治性滤泡性淋巴瘤(r/rFL)的治疗。
3、2024年8月27日:国家药品监督管理局(NMPA)批准该药的补充生物制品许可申请(sBLA),用于成人复发或难治性套细胞淋巴瘤(r/rMCL)的治疗。临床数据显示,近七成r/rMCL患者经该疗法治疗后,可获得完全缓解。
而此次新适应症的申报,标志着瑞基奥仑赛在血液肿瘤治疗领域的进一步拓展,有望为更多难治性B细胞淋巴瘤患者提供新的治疗选择!
《Nature》子刊力证:瑞基奥仑赛2年随访数据惊艳!B细胞非霍奇金淋巴瘤ORR高达85%,2年总生存率达70%
全球知名期刊《Nature》子刊《骨髓移植》杂志,曾发表过“瑞基奥仑赛注射液(relma-cel)治疗复发/难治性(R/R)B细胞非霍奇金淋巴瘤(B-NHL),I期临床试验长达2年的疗效与安全性随访数据”。
该研究纳入23例患者,其中60.9%为弥漫大B细胞淋巴瘤(DLBCL),26.1%为滤泡性淋巴瘤(FL)。这些患者入组后先接受淋巴细胞清除化疗,随后单次输注瑞基奥仑赛注射液,中位随访时间达24.2个月。
结果显示:在20例可评估疗效的患者中,客观缓解率(ORR)高达85.0%,最佳完全缓解率(CRR)达75.0%,2年无进展生存率(PFS率)为60.0%,2年总生存率(OS率)达70.0%。
▲图源“Bone Marrow Transplantation”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
综上,该研究证实了瑞基奥仑赛注射液在复发/难治性B细胞非霍奇金淋巴瘤中持久的疗效与良好的安全性,为CAR-T细胞疗法在血液肿瘤中的长期应用提供了关键临床证据。
如何寻求CAR-T细胞疗法免费申请机会
好消息是,目前CAR-T疗法已启动临床招募,主要针对胃癌、胰腺癌、肠癌、脑胶质瘤、淋巴瘤、骨髓瘤、白血病等多款癌种。
想寻求CAR-T或其他抗癌新技术帮助的病友,也可将治疗经历、病理检查结果、近期检查报告(如影像学检查、血液检查等)、基因检测报告等资料,提交至医学部,初步评估能否有机会接受CAR-T疗法的帮助。
国研CT017 CAR-T:50%疾病控制率改写GPC3阳性肝癌治疗困局,最长生存超18个月
晚期肝细胞癌(HCC)的全身治疗虽能改善预后,但长期临床获益仍有限。而靶向磷脂酰肌醇蛋白聚糖-3(GPC3)的CAR-T细胞疗法,因其可精准清除GPC3阳性肿瘤细胞的特性,有望成为这类患者治疗的新选择。
而近期中国浙江大学开展了一项“应用CT017CAR-GPC3T细胞,治疗GPC3阳性肝细胞癌的I期临床试验(NCT03980288)”,并公布了关键数据。CT017是一种经基因工程改造的CAR-T细胞疗法,可共表达CAR-GPC3和Runt相关转录因子3(RUNX3),通过诱导CD8+T细胞浸润肿瘤微环境发挥抗肿瘤作用。
该研究共纳入6例既往接受过多线治疗的GPC3阳性肝细胞癌(HCC)患者,中位年龄为50.5岁(范围:36-66岁),均有乙肝病史,5例合并肝硬化。治疗方案包括:2例接受CT017单药治疗,4例采用CT017+瑞戈非尼或索拉非尼联合治疗,中位随访时间为7.87个月。
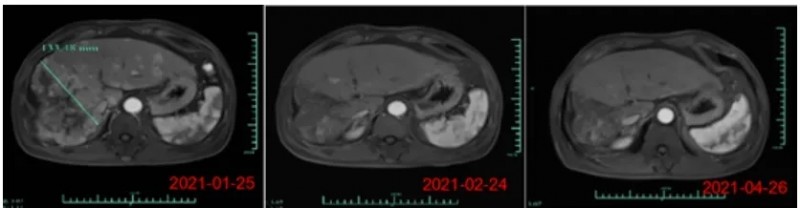
结果显示:在6例可评估疗效的患者中,客观缓解率(ORR)达16.7%,疾病控制率(DCR)高达50%。其中1例患者达到部分缓解(PR)(详见下图),缓解持续时间为4.6个月。2例达到病情稳定(SD)。
▼一例达到PR患者靶病灶的放射影像学评估
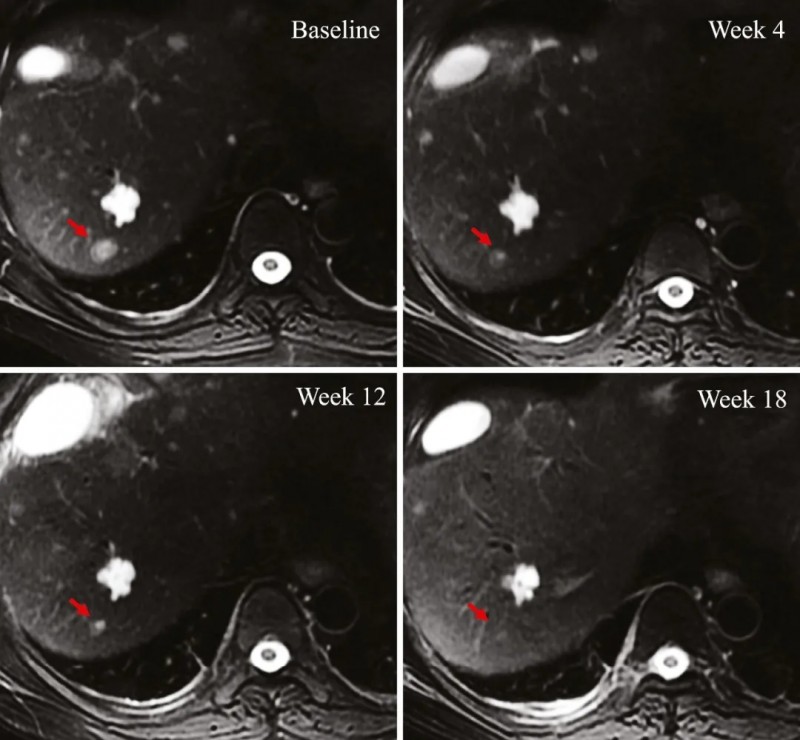
▲图源“EClinical Medicine”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
此外,中位无进展生存期(PFS)3.5个月(95%CI,0.9-4.9)。中位总生存期(OS)为7.9个月,最长OS达18.2个月。
▼PFS(mITT分析集)游泳图
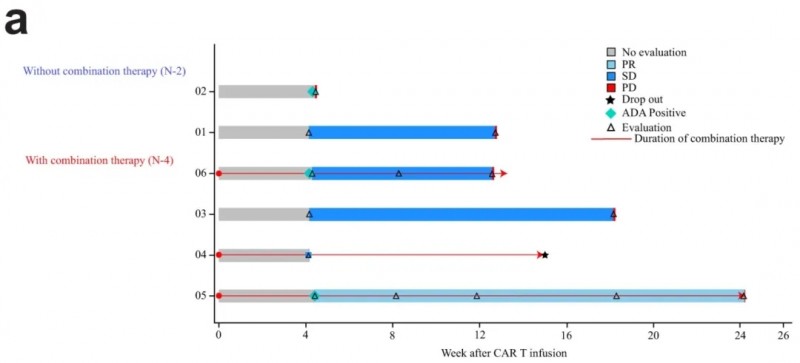
▲图源“EClinical Medicine”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
新型huCART19-IL18细胞暴击难治性淋巴瘤,完全缓解率达52%,1例患者无癌超2年
2025年5月7日,《新英格兰医学杂志》报道了一款新兴“装甲”抗CD19增强型CAR-T细胞产品——huCART19-IL18,针对复发或难治性B细胞淋巴瘤的Ⅰ期临床研究(NCT04684563)的突破性数据,并引起了广泛关注,该疗法将传统CAR-T细胞9~14天的生产周期缩短至仅3天,为癌症患者争取到了宝贵的治疗时间窗口!
该研究共入组21例复发或难治性B细胞淋巴瘤患者,包括弥漫大B细胞淋巴瘤(8例)、滤泡性淋巴瘤(6例)、套细胞淋巴瘤(3例)等。这些患者平均接受过7种其他癌症治疗,其中20例曾接受过现有CAR-T疗法但均告失败,临床治疗难度非常高。
结果显示:在输注huCART19-IL18三个月后,81%的患者(90%CI:62~93)症状得到改善,其中52%(90%CI:33~71)达到完全缓解(CR),29%(90%CI,13~49)实现部分缓解(PR)。所有淋巴瘤亚型均观察到响应,其中,滤泡性淋巴瘤和套细胞淋巴瘤患者缓解率达100%(详见下图),大B细胞淋巴瘤患者为67%。中位缓解持续时间为9.6个月(90%CI:5.5~未达到),中位无进展生存期(PFS)8.7个月(90%CI:5.4~未达到);15个月总生存率估计为86%(90%CI:61~96)。
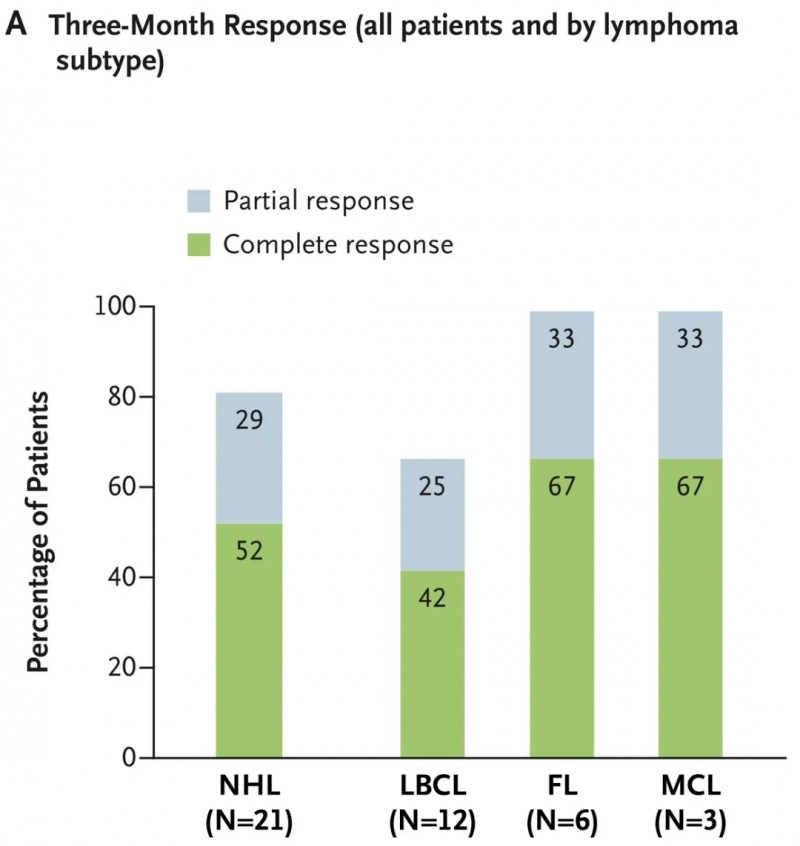
▲图源“N Engl J Med”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
值得一提的是,其中一例滤泡性淋巴瘤患者的疗效尤为瞩目:该患者曾对Yescarta及双特异性抗体治疗耐药,在接受huCART19-IL18治疗后3个月即达完全缓解(CR),肿瘤全面消退,且缓解状态持久维持,自首次输注至今已超过24个月。
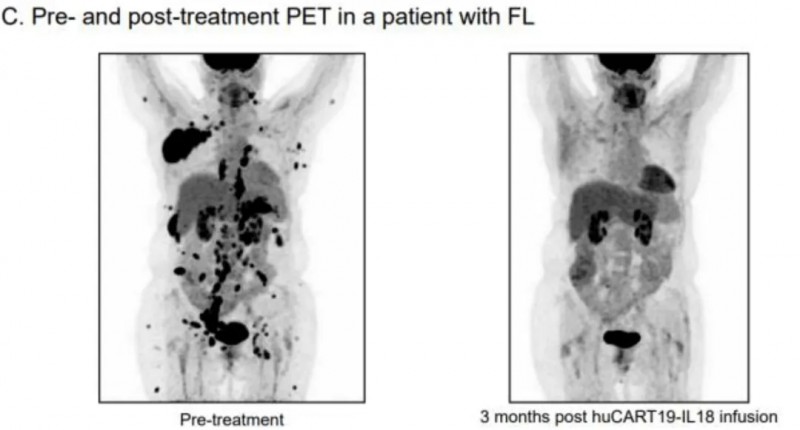
▲图源“N Engl J Med”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
多款国研CAR-T蓄势待发,剑指胃癌、肝癌、肠癌等
1、舒瑞基奥仑赛注射液(CT041)
目前全球唯一一款在中国和美国获得临床试验许可(IND)的CLDN18.2 CAR-T细胞疗法,2025年5月20日,该药被中国国家药监局药品审评中心(CDE)纳入优先评审,拟用于CLDN18.2表达阳性、且经至少二线治疗失败的晚期胃/食管胃结合部腺癌的治疗,有望成为全球首个上市的实体瘤CAR-T产品!
2024年ASCO大会上公布的数据显示:舒瑞基奥仑赛注射液治疗CLDN18.2阳性晚期胃肠道肿瘤的总缓解率(ORR)为38.8%,疾病控制率(DCR)高达91.8%。
2、C-CAR031疗法
C-CAR031是一种自体新型GPC3靶向CAR-T细胞疗法。针对晚期/不可切除肝细胞癌(HCC)的I期临床研究(NCT05155189)数据显示:疾病控制率(DCR)高达91.3%,客观缓解率(ORR)达56.5%,中位总生存期(mOS)为11.14个月(95%CI,7.56-NE)。
3、Ori-C101疗法
一款靶向GPC3的CAR-T细胞疗法,拟用于成人晚期肝细胞癌的治疗。2021年ASCO大会上,公布了其治疗复发/难治性肝细胞癌(HCC)的最新数据。结果显示:客观缓解率(ORR)为44.4%,疾病控制率(DCR)达77.8%。其中一例患者(患者007)在接受CAR-T输注1个月,肿瘤体积缩小了80%以上(详见下图),截至统计时止,该患者部分缓解(PR)持续超过6个月。
4、GCC19CAR-T
是一款针对肠癌细胞“黄金”靶标——鸟苷三磷酸化酶(GUCY2C,GCC)的CAR-T细胞疗法。2024年《JAMA肿瘤学》发布了GCC19CAR-T治疗肠癌的临床研究数据。结果显示:客观缓解率(ORR)为40%,中位总生存期(OS)为22.8个月。阅
小编寄语
近些年来,以CAR-T疗法为代表的免疫细胞疗法已取得了长足的进展,为复发/难治性肿瘤患者带来了新的希望与选择!我国的CAR-T研发热度空前高涨,相继有驯鹿医疗、科济生物、传奇生物、复星凯特等20多家制药巨头纷纷投身CAR-T的研发大军中,我国也成为了继美国之后的又一CAR-T“大国”,相继有多款产品获批上市,并在世界顶级癌症大会中“崭露头角”!
好消息是,目前有多款CAR-T疗法的临床研究正在招募中,对此感兴趣的患者,可将近期影像学检查、治疗经历、病理检查报告等资料,提交至医学部,了解详细的入排标准或进行初步评估。
参考资料
[1]Ying Z,et al.Efficacy and safety of relmacabtagene autoleucel, an anti-CD19 chimeric antigen receptor T cell, in relapsed/refractory B-cell non-Hodgkin’s lymphoma: 2-year results of a phase 1 trial[J]. Bone Marrow Transplantation, 2023, 58(3): 288-294.
https://www.nature.com/articles/s41409-022-01888-z
[2]Fu Q,et al.RUNX-3-expressing CAR T cells targeting glypican-3 in patients with heavily pretreated advanced hepatocellular carcinoma: a phase Ⅰ trial [J/OL]. EClinicalMedicine, 2023, 63: 102175 [2024-02-10][EB/OL].(2023)
https://www.thelancet.com/journals/eclinm/article/PIIS2589-5370(23)00352-8/fulltext
[3]Svoboda J,et al.Enhanced CAR T-Cell Therapy for Lymphoma after Previous Failure[J]. New England Journal of Medicine, 2025, 392(18): 1824-1835.
https://www.nejm.org/doi/10.1056/NEJMoa2408771?url_ver=Z39.88-2003
扫描进患者病友群

肺癌|胃癌|肝癌|结直肠癌|胰腺癌
乳腺癌|脑瘤|淋巴瘤|儿童肿瘤等

相关推荐

癌症治疗本就不应千篇一律,揭秘mRNA癌
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
“不限癌种”新突破,NTRK基因融合的靶
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
肺癌疫苗重大突破,晚期患者多了一个新的选
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

“手术成功”不等于万事大吉,新型癌症疫苗
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

2026年靶向治疗抗癌风暴,突破困境,普
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

2026年这些肺癌疫苗正悄然改变患者的生
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05






![[field:title/]](/uploads/allimg/20200224/1-2002241I5262J.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241I3461D.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H94LK.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241HKW34.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H619327.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H34H52.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H22IH.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241G93O18.jpg)




