2年生存率近80%!沙特紧急授孤儿药资格,国产CAR-T成功出海中东!多疗法亮剑胃癌、肝癌、肠癌等
沙特紧急授中国CAR-T细胞疗法孤儿药资格,国产CAR-T成功出海中东!多疗法亮剑胃癌、肝癌、肠癌等
据“驯鹿官网”2025年5月9日消息,沙特阿拉伯王国食品药品监督管理局(SFDA)正式授予驯鹿医疗自主研发的靶向BCMA的CAR-T细胞治疗产品伊基奥仑赛注射液(FUCASO)孤儿药资格认定(ODD),用于治疗既往接受至少三线治疗后出现疾病进展(至少使用过一种蛋白酶体抑制剂及免疫调节剂)的复发或难治性多发性骨髓瘤(R/R MM)成人患者。这意味着该疗法可直接递交新药上市申请(NDA),审批周期将大幅缩短,中东地区饱受病痛折磨的患者即将迎来新的治疗希望!
此刻,我们无比自豪地见证:国产CAR-T疗法再次以实力获得国际认可,伊基奥仑赛注射液的“出海”突破,是中国肿瘤免疫治疗发展的重要里程碑——它不仅让中国原研药成功跻身全球罕见病治疗的核心赛道,更向世界展示了中国在细胞治疗领域的创新力量,为更多中国创新药走向国际市场奠定了坚实基础!小编也在此呼吁广大癌友,及时了解已获批上市/正在研发中的中国自研CAR-T细胞疗法,为抗癌治疗增添更多选择与希望!

▲截图源自“SFDA”
伊基奥仑赛两次成功"出海",96.4%ORR开启骨髓瘤长生存时代
从"中国首款"到"全球标杆",中国原研CAR-T闪耀国际舞台
伊基奥仑赛注射液(Equecabtagene Autoleucel Injection,,eque-cel,福可苏®,研发代号:CT103A/IBI326)由驯鹿生物与信达生物联合研发,是全球首款全人源B细胞成熟抗原(BCMA)靶向的CAR-T细胞疗法。其核心优势在于通过全人源抗体设计降低免疫原性,为复发/难治性多发性骨髓瘤(R/R MM)患者提供精准治疗选择。

早在2023年6月30日,伊基奥仑赛就已获中国国家药品监督管理局(NMPA)批准,用于复发/难治性多发性骨髓瘤(R/R MM)的治疗,成为中国首款获批的BCMA CAR-T疗法,同时也是全球首款全人源BCMA靶向的CAR-T疗法,填补了该领域的临床空白。
2025年1月29日,新加坡卫生科学局(HSA)受理其新药上市申请(NDA),适用于已接受过≥3种既往治疗的复发和/或难治性多发性骨髓瘤(R/R MM)的治疗,标志着“出海”首站落地。
同年5月,沙特阿拉伯食品药品监督管理局(SFDA)授予其孤儿药资格认定(ODD),用于经至少三线治疗(含蛋白酶体抑制剂及免疫调节剂)失败的成人R/R MM患者,进一步加速中东地区临床可及性。
近4年随访数据震撼发布!伊基奥仑赛ORR达96.4%,深度缓解患者2年生存率近80%
2025年5月16日,《转化医学杂志》发表了伊基奥仑赛的长期临床疗效(2017年3月-2023年12月)数据,该研究纳入65例长期临床疗效患者(中位年龄56岁,范围:51-61岁),中位随访39.6个月(范围:1.0-69.3个月)。
结果显示:总有效率(ORR)达96.4%,其中80.4%(45例)患者达到完全缓解(CR)或严格完全缓解(sCR),96.4%(54/56例)的患者,实现微小残留病阴性(MRD-)。中位缓解持续时间(DOR)为30.8个月,中位无进展生存期(PFS)30.1个月,总生存期(OS)未达到(NR)。
CAR-T细胞持续存在≥6个月且MRD-的患者预后更佳,维持MRD阴性达12、24、36个月者,中位PFS分别为58个月、64个月、未达到(NR)。此外,45名达到CR或严格完全缓解(sCR)的患者,其2年无进展生存(PFS)率为70.0%、总生存(OS)率为78.9%,显著高于未达到CR的患者(p <0.05),提示早期干预促进深度缓解可显著改善生存结局。

▲截图源自“BMC”
中国患者如何获得CAR-T细胞疗法免费申请机会
好消息是,目前CAR-T疗法已启动临床招募,主要针对胃癌、胰腺癌、肠癌、脑胶质瘤、淋巴瘤、骨髓瘤、白血病等多款癌种。阅读原文了解详情:百万疗法免费申请机会来啦!十大CAR-T疗法启动招募,惠及胃癌,肠癌,淋巴瘤等
想寻求CAR-T或其他抗癌新技术帮助的病友,也可将治疗经历、病理检查结果、近期检查报告(如影像学检查、血液检查等)、基因检测报告等资料,提交至医学部,初步评估能否有机会接受CAR-T疗法的帮助。
国产CAR-T出海再传捷报!首个FDA批准BCMA靶向疗法西达基奥仑赛震撼登场,多发性骨髓瘤ORR高达89.6%
除伊基奥仑赛外,另一款成功“出海”的国产CAR-T疗法是西达基奥仑赛。作为首个获FDA批准的国产BCMA靶向CAR-T细胞疗法,其适应症为成人复发或难治性多发性骨髓瘤(R/R MM)。
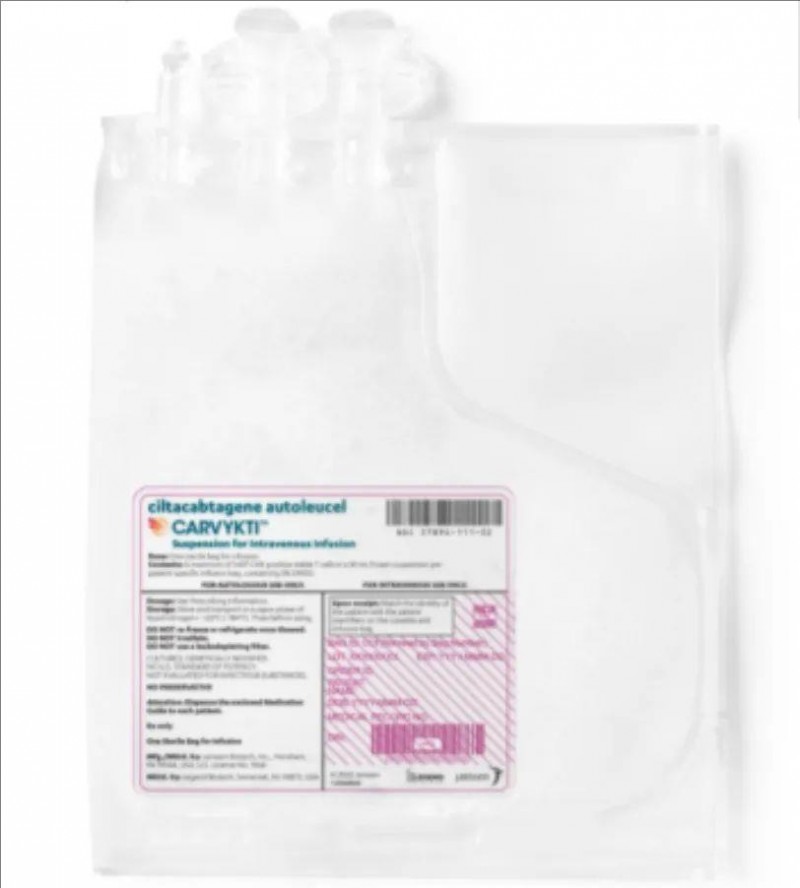
在中国开展的Ⅱ期CARTIFAN-1临床研究(NCT03758417)中,共入组48例中位年龄61岁的R/RMM患者,接受西达基奥仑赛回输治疗。
结果显示:客观缓解率(ORR)达89.6%(95%CI:77.3~96.5),其中77.1%患者(95%CI:62.7~88.0)实现完全缓解或更高疗效。12个月无进展生存率(PFS)为77.0%(95%CI:62.3~86.5),18个月PFS率66.8%(95%CI:49.4~79.4)。18个月总生存率(OS)达78.7%(95%CI:64.0~88.0)。
综上,西达基奥仑赛的国际化突破与临床数据,彰显了国产CAR-T疗法在多发性骨髓瘤领域的全球竞争力。
中国已获批上市的CAR-T产品
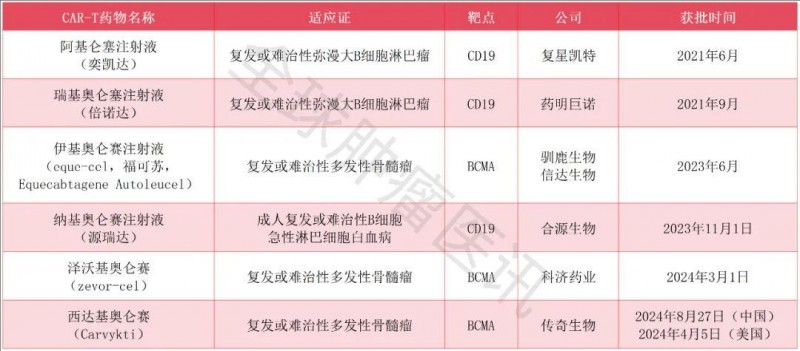
我国在研的其他备受瞩目的CAR-T疗法
1、全球首个CAR-GPC3 T细胞:肝癌中位总生存达278天
《Clinical Cancer Research》报道了中国团队关于靶向GPC3的CAR-T细胞,治疗肝细胞癌的全球首个临床试验数据,中国CAR-T研究成果再次在世界舞台崭露头角。
结果显示:在13例晚期、GPC3抗原阳性的肝细胞癌(HCC)患者中,2例获得部分缓解(PR),肿瘤病灶显著缩小;3年、1年、6个月生存率分别为10.5%、42.0%和50.3%;中位生存时间(OS)长达278天(95%CI:48~615天)。
2、CT071(靶向GPRC5D CAR-T):多发性骨髓瘤总缓解率高达94.1%
CT071是由科济药业自主研发的一款靶向GPRC5D的自体CAR-T细胞候选产品,采用快速CAR celerate®平台生产,可使生产时间缩短至30小时左右,大大减少了从单采到回输的时间,节省了患者的等待时间。
在2024ASH大会上,展示了“CT071治疗难治性/复发性多发性骨髓瘤,首次应用于人体的I期探索性临床试验(NCT05838131)的初步研究结果”。
结果显示:总体缓解率(ORR)高达94.1%(16/17),严格完全缓解(sCR)率为52.9%(9/17),88.2%(15/17)的患者在10−6阈值下,达到MRD阴性。其中,一名基线肿瘤直径为125mm×99mm的患者,治疗26周后肿瘤缩小38.2%,血清M蛋白较基线下降93.0%。
3、CT041(靶向CLDN18.2 CAR-T):胃癌及前列腺癌治疗取得突破性数据
CT041(satri-cel,satricabtageneautoleucel)是我国自主研发的一款靶向CLDN18.2的CAR-T细胞疗法,同时也是全球首个且唯一获得中美双报临床试验许可(IND)的靶向CLDN18.2的CAR-T细胞疗法,主要针对胃癌等消化系统肿瘤。
2024年美国临床肿瘤学会(ASCO)大会披露的1b/2期研究(NCT04404595)数据显示:全部入组患者的最佳客观缓解率(ORR)为26.3%,中位缓解持续时间(DOR)为3.7个月,临床获益率(CBR)为42.1%。
其中,胃癌/胃食管结合部癌(GC/GEJ)组(n=7),客观缓解率(ORR)为42.9%(3/7),中位缓解持续时间(DOR)为6.9个月,临床获益率(CBR)为57.1%。
而在前列腺癌(PC)组(n=12):ORR为16.7%(2/12),中位DOR为3.4个月,CBR为33.3%。
4、国产CEA CAR-T疗法:70%转移性结直肠癌达病情稳定
我国曾开展过一项针对CEA阳性结直肠癌(CRC)患者的I期临床试验(NCT02349724),入组10例伴肝、肺转移的难治性患者,入组接受静脉输注CEACAR-T细胞治疗。
结果显示:10例在既往治疗中,出现疾病进展(PD)的患者中,有7例在CAR-T治疗后病情稳定(SD),肿瘤直径无显著进展。其中2例患者(Ps3和Ps5)病情持续稳定超过30周。
小编寄语
近年来,随着多款CAR-T疗法相继获批上市,我国CAR-T的研发领域也迎来了属于自己的高光时刻!目前我国已有20多家制药巨头,如驯鹿医疗、传奇生物、复星凯特、科济生物等纷纷布局CAR-T的研发,力争在精确调控、新靶点设计、通用CAR-T细胞等方面,取得突破性进展。这两年,更是有多款CAR-T产品登上国际舞台。全球肿瘤医学部小编也期望随着越来越多明星靶点的涌现、技术的不断革新,CAR-T疗法可以早日突破价格和癌症治疗的瓶颈,造福更多的癌症晚期患者,实现长期带瘤生存、降低复发风险的美好愿景!
如果您对目前的治疗方案不满意,或想寻求CAR-T、CAR-NK、TCR-T、TIL疗法等国内外抗癌新技术的帮助,可将治疗经历、近期影像学检查、病理检查报告等资料汇总后,提交至医学部,进行初步评估,或申请国内外抗癌专家会诊。
参考资料
[1]An N,et al.Key predictors of long-term outcomes in BCMA-targeted CAR-T therapy for relapsed/refractory multiple myeloma[J]. Journal of Translational Medicine, 2025, 23(1): 1-13.
https://translational medicine.biomedcentral.com/articles/10.1186/s12967-025-06543-x
[2]Mi J Q,et al.Phase II, open-label study of ciltacabtagene autoleucel, an anti–B-cell maturation antigen chimeric antigen receptor–T-cell therapy, in chinese patients with relapsed/refractory multiple myeloma (CARTIFAN-1)[J]. Journal of Clinical Oncology, 2023, 41(6): 1275-1284.
https://ascopubs.org/doi/10.1200/JCO.22.00690?url_ver=Z39.88-2003&rfr_id=ori:rid:crossref.org&rfr_dat=cr_pub%20%200pubmed
[3]https://cn.iasobio.com/phone/info.php?id=326
扫描进患者病友群

肺癌|胃癌|肝癌|结直肠癌|胰腺癌
乳腺癌|脑瘤|淋巴瘤|儿童肿瘤等

相关推荐

癌症治疗本就不应千篇一律,揭秘mRNA癌
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
“不限癌种”新突破,NTRK基因融合的靶
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
肺癌疫苗重大突破,晚期患者多了一个新的选
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

“手术成功”不等于万事大吉,新型癌症疫苗
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

2026年靶向治疗抗癌风暴,突破困境,普
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

2026年这些肺癌疫苗正悄然改变患者的生
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05






![[field:title/]](/uploads/allimg/20200224/1-2002241I5262J.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241I3461D.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H94LK.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241HKW34.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H619327.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H34H52.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H22IH.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241G93O18.jpg)




